18.07.2022
Autor:
Renata Dolata
Źródło: United European Gastroenterology Journal https://onlinelibrary.wiley.com/doi/10.1002/ueg2.12270
Xifaxan z silną rekomendacją w najnowszych wytycznych leczenia IBS

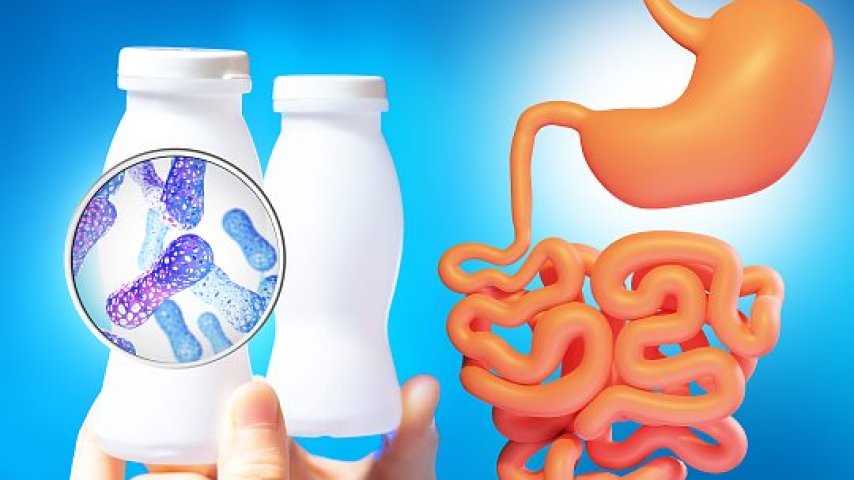
Zespół jelita nadwrażliwego z biegunką (IBS-D) i biegunka czynnościowa to dwa główne zaburzenia czynnościowe jelit charakteryzujące się występowaniem biegunki u pacjentów. Pomimo dużej częstości występowania, obie choroby wzbudzają wiele wątpliwości, szczególnie w zakresie optymalnej diagnostyki i postępowania z chorymi.
W związku z tym panel ekspertów dwóch europejskich towarzystw medycznych – United European Gastroenterology i European Society for Neurogastroenterology and Motility dokonał podsumowania literatury oraz przeprowadził głosowanie nad 31 zaleceniami, a jego wyniki zostały zebrane i przedstawione jako konsensus Delphi. Oba towarzystwa medyczne z wysokim poziomem zgodności (96 proc.) silnie rekomendują zastosowanie rifaksyminy u pacjentów z biegunkową postacią IBS.
Rifaksymina, wprowadzona na rynek w 1985 r. we Włoszech, jest dostępna w 33 krajach pod różnymi nazwami handlowymi (w Polsce Xifaxan, Alfasigma). Lek również został zatwierdzony przez Amerykańską Agencję ds. Żywności i Leków (FDA) do leczenia pacjentów z biegunkową postacią IBS. Uzasadnienie stosowania rifaksyminy w tym wskazaniu oparte jest na fakcie, że u pacjentów z biegunkową postacią choroby stwierdza się zaburzenia mikrobioty jelitowej (dysbiozę) i stan zapalny w jelicie o niskim nasileniu. Rifaksymina wykazuje działanie przeciwbakteryjne, nieodwracalnie wiążąc się z podjednostką beta bakteryjnej DNA-zależnej polimerazy RNA, wskutek tego hamuje syntezę bakteryjnego RNA i białek; ma działanie "eubiotyczne” poprzez promowanie wzrostu bakterii komensalnych o korzystnych dla organizmu właściwościach oraz działanie przeciwzapalne poprzez specyficzną dla jelita aktywację receptora pregnanu X.
Zastosowanie rifaksyminy w leczeniu biegunkowej postaci IBS jest poparte licznymi badaniami klinicznymi o najwyższym stopniu dowodu naukowego RCT. W dwóch identycznie zaprojektowanych badaniach III fazy (Target 1 i Target 2), randomizowanych, kontrolowanych placebo, udowodniono skuteczność rifaksyminy w dawce 1650 mg/d podawanej przez dwa tygodnie. Rifaksymina zmniejszała lub znosiła takie objawy, jak ogólne objawy IBS, wzdęcie, ból brzucha oraz luźne stolce. Wyniki obu badań wykazały, że u 40,8 proc. pacjentów leczonych rifaksyminą wystąpiła statystycznie istotna poprawa zarówno w zakresie bólu brzucha, jak i konsystencji stolca w porównaniu z 31,7 proc. pacjentów leczonych placebo (p < 0,001). W kolejnym badaniu (Target 3) oceniano skuteczność rifaksyminy u osób uprzednio leczonych rifaksyminą, u których doszło do nawrotu objawów IBS. W pierwszej, otwartej fazie badania rifaksyminę podano 1074 pacjentom. U 44 proc. badanych nastąpiła poprawa objawów. Po 18 tygodniach u 64 proc. chorych, którzy w fazie otwartej odpowiedzieli na rifaksyminę, nastąpił nawrót choroby i te osoby otrzymały dwa kolejne 14-dniowe cykle leczenia rifaksyminą lub placebo. Odsetek badanych, którzy uzyskali odpowiedź na punkty końcowe w zakresie poprawy objawów IBS zdefiniowane przez FDA, był istotnie wyższy w przypadku rifaksyminy niż placebo.
Niedawno opublikowana metaanaliza pięciu randomizowanych badań kontrolowanych placebo skuteczności i bezpieczeństwa zastosowania rifaksyminy w leczeniu IBS wykazała istotną korzyść w poprawie objawów po zastosowania rifaksyminy, a liczba NNT (number needed to treat) wyniosła 9. W kilku badaniach RCT wykazano wysoki poziom bezpieczeństwa terapii rifaksyminą ze względu na miejscowe działanie w jelicie (znikome wchłanianie ogólnoustrojowe) i eubiotyczny efekt działania (brak istotnych modyfikacji struktury mikrobioty jelitowej). .
Rifaksymina, wprowadzona na rynek w 1985 r. we Włoszech, jest dostępna w 33 krajach pod różnymi nazwami handlowymi (w Polsce Xifaxan, Alfasigma). Lek również został zatwierdzony przez Amerykańską Agencję ds. Żywności i Leków (FDA) do leczenia pacjentów z biegunkową postacią IBS. Uzasadnienie stosowania rifaksyminy w tym wskazaniu oparte jest na fakcie, że u pacjentów z biegunkową postacią choroby stwierdza się zaburzenia mikrobioty jelitowej (dysbiozę) i stan zapalny w jelicie o niskim nasileniu. Rifaksymina wykazuje działanie przeciwbakteryjne, nieodwracalnie wiążąc się z podjednostką beta bakteryjnej DNA-zależnej polimerazy RNA, wskutek tego hamuje syntezę bakteryjnego RNA i białek; ma działanie "eubiotyczne” poprzez promowanie wzrostu bakterii komensalnych o korzystnych dla organizmu właściwościach oraz działanie przeciwzapalne poprzez specyficzną dla jelita aktywację receptora pregnanu X.
Zastosowanie rifaksyminy w leczeniu biegunkowej postaci IBS jest poparte licznymi badaniami klinicznymi o najwyższym stopniu dowodu naukowego RCT. W dwóch identycznie zaprojektowanych badaniach III fazy (Target 1 i Target 2), randomizowanych, kontrolowanych placebo, udowodniono skuteczność rifaksyminy w dawce 1650 mg/d podawanej przez dwa tygodnie. Rifaksymina zmniejszała lub znosiła takie objawy, jak ogólne objawy IBS, wzdęcie, ból brzucha oraz luźne stolce. Wyniki obu badań wykazały, że u 40,8 proc. pacjentów leczonych rifaksyminą wystąpiła statystycznie istotna poprawa zarówno w zakresie bólu brzucha, jak i konsystencji stolca w porównaniu z 31,7 proc. pacjentów leczonych placebo (p < 0,001). W kolejnym badaniu (Target 3) oceniano skuteczność rifaksyminy u osób uprzednio leczonych rifaksyminą, u których doszło do nawrotu objawów IBS. W pierwszej, otwartej fazie badania rifaksyminę podano 1074 pacjentom. U 44 proc. badanych nastąpiła poprawa objawów. Po 18 tygodniach u 64 proc. chorych, którzy w fazie otwartej odpowiedzieli na rifaksyminę, nastąpił nawrót choroby i te osoby otrzymały dwa kolejne 14-dniowe cykle leczenia rifaksyminą lub placebo. Odsetek badanych, którzy uzyskali odpowiedź na punkty końcowe w zakresie poprawy objawów IBS zdefiniowane przez FDA, był istotnie wyższy w przypadku rifaksyminy niż placebo.
Niedawno opublikowana metaanaliza pięciu randomizowanych badań kontrolowanych placebo skuteczności i bezpieczeństwa zastosowania rifaksyminy w leczeniu IBS wykazała istotną korzyść w poprawie objawów po zastosowania rifaksyminy, a liczba NNT (number needed to treat) wyniosła 9. W kilku badaniach RCT wykazano wysoki poziom bezpieczeństwa terapii rifaksyminą ze względu na miejscowe działanie w jelicie (znikome wchłanianie ogólnoustrojowe) i eubiotyczny efekt działania (brak istotnych modyfikacji struktury mikrobioty jelitowej). .