Jak nie dopuścić u pacjenta z nadciśnieniem tętniczym do przerostu mięśnia lewej komory i albuminurii

O dwóch najczęstszych powikłaniach narządowych nadciśnienia tętniczego mówią w „Kurierze Medycznym” prof. dr hab. n. med. Aleksander Prejbisz, pełniący obowiązki kierownika Zakładu Epidemiologii, Prewencji Chorób Układu Krążenia i Promocji Zdrowia Narodowego Instytutu Kardiologii, oraz prof. dr hab. n. med. Piotr Dobrowolski, kierownik Samodzielnej Poradni Lipidowej, z Zakładu Epidemiologii, Prewencji Chorób Układu Krążenia i Promocji Zdrowia Narodowego Instytutu Kardiologii.
Lepiej zapobiegać, niż leczyć. To nie truizm, ale fakt. Dlatego tak niezwykle ważna jest ocena ryzyka sercowo-naczyniowego.
Piotr Dobrowolski: – To prawda. Na pewno łatwiej zapobiegać, niż leczyć jawne klinicznie choroby sercowo-naczyniowe na podłożu miażdżycy. Dlatego ocena ryzyka sercowo-naczyniowego jest kluczowym elementem postępowania. Powinniśmy je oceniać zarówno podczas wizyt pierwszorazowych, jak i na każdym etapie postępowania farmakologicznego. W 2021 r. ukazały się wytyczne europejskie dotyczące prewencji chorób sercowo-naczyniowych. Zgodnie z nimi u pacjentów bez rozpoznanej choroby sercowo-naczyniowej do oceny ryzyka należy wykorzystać kartę SCORE2 bądź SCORE2-OP w przypadku osób powyżej 70. roku życia. Jest to bardzo dobre narzędzie, które powinno być powszechnie stosowane do wstępnej oceny ryzyka u wszystkich pacjentów. Niestety ta skala nie jest pozbawiona wad. Ocenie podlega tylko pięć czynników: wartość skurczowego ciśnienia tętniczego, stężenie cholesterolu nie-HDL w osoczu, palenie/niepalenie tytoniu, płeć i wiek. Na tej podstawie tak naprawdę jesteśmy w stanie tylko z grubsza ocenić ryzyko sercowo-naczyniowe. Tymczasem, jak wiemy, u pacjentów ze źle leczonym lub nieleczonym nadciśnieniem tętniczym często dochodzi do subklinicznych powikłań narządowych. Najczęściej są to przerost mięśnia lewej komory serca (left ventricular hipertrophy – LVH) i zwiększenie wydalania białka z moczem, czyli albuminuria. To dwa główne powikłania narządowe związane z nadciśnieniem tętniczym. Jeśli one występują u pacjenta, od razu wiemy, że cechuje go dużo większe ryzyko sercowo-naczyniowe niż oszacowane na podstawie kart SCORE2. Przykładowo, jeśli w skali SCORE2 ocenimy, że pacjent ma umiarkowane ryzyko sercowo-naczyniowe, to stwierdzenie jednego z powikłań narządowych – LVH lub albuminurii umiarkowanego stopnia – automatycznie przesuwa go do wyższej klasy ryzyka. Jeśli stwierdzimy obydwa powikłania, to ryzyko będzie jeszcze większe. Dlatego tak ważne jest, by nie dopuścić do rozwoju tych powikłań. W tym celu powinniśmy wdrożyć odpowiednią terapię farmakologiczną od samego początku leczenia chorych z nadciśnieniem tętniczym. Pamiętamy przy tym o pozostałych czynnikach ryzyka sercowo-naczyniowego prowadzących do narastania blaszki miażdżycowej, której pęknięcie może doprowadzić do zawału serca lub udaru mózgu.
Czy można łatwo wykryć istnienie tych dwóch najczęstszych powikłań nadciśnienia tętniczego, czyli LVH i albuminurii?
Aleksander Prejbisz: – Zmiany, które zachodzą w podstawowej opiece zdrowotnej, polegające na wprowadzeniu do niej opieki koordynowanej czy Krajowej Sieci Kardiologicznej, dają większe możliwości oceny tych powikłań narządowych już na tym etapie. Oczywiście powikłań nadciśnienia tętniczego jest więcej – wzrost sztywności naczyń, rozwój miażdżycy tętnic kończyn dolnych, ale dwa omawiane, czyli LVH i albuminuria, są łatwe w ocenie. Poza tym nie tylko korelują z ryzykiem sercowo-naczyniowym, lecz także są wykładnikami skuteczności leczenia. Jeżeli chory ma już jakieś cechy przerostu mięśnia lewej komory czy zwiększoną albuminurię, skuteczne leczenie będzie prowadziło do regresji tych powikłań. Jest to zatem ważny element dodatkowej kontroli skuteczności terapii nadciśnienia tętniczego przyczyniający się do zmniejszenia ryzyka sercowo-naczyniowego. Oczywiście karta SCORE2 powinna być wykorzystywana, ale w wielu przypadkach należy wykraczać poza nią i indywidualizować ocenę ryzyka sercowo-naczyniowego poprzez wykorzystanie markerów ryzyka, które mają absolutne uzasadnienie w wytycznych. Dzięki opiece koordynowanej dostępność tych markerów dla lekarzy podstawowej opieki zdrowotnej, a przede wszystkim dla pacjentów jest większa.
Jak często stwierdza się LVH u chorych na nadciśnienie tętnicze?
P.D.: – W badaniu Framingham w obserwowanej populacji ogólnej LVH oceniany echokardiograficznie był obecny u 37 proc. osób. U pacjentów z opornym nadciśnieniem tętniczym występuje on znacznie częściej. W ocenie echokardiograficznej, w zależności od przyjętych kryteriów, stwierdzano go u 55–81 proc. pacjentów. Najczęstszy jest łagodny przerost w postaci tzw. koncentrycznej przebudowy lewej komory, gdy dojdzie do nasilenia przebudowy, mówimy o koncentrycznym przeroście mięśnia lewej komory. Już od badania Framingham wiemy, że każde zwiększenie masy mięśnia lewej komory jest związane z gorszym rokowaniem sercowo-naczyniowym. Gdy dojdzie do koncentrycznego przerostu, chory ma największe ryzyko sercowo-naczyniowe.
Jakimi metodami można stwierdzić LVH?
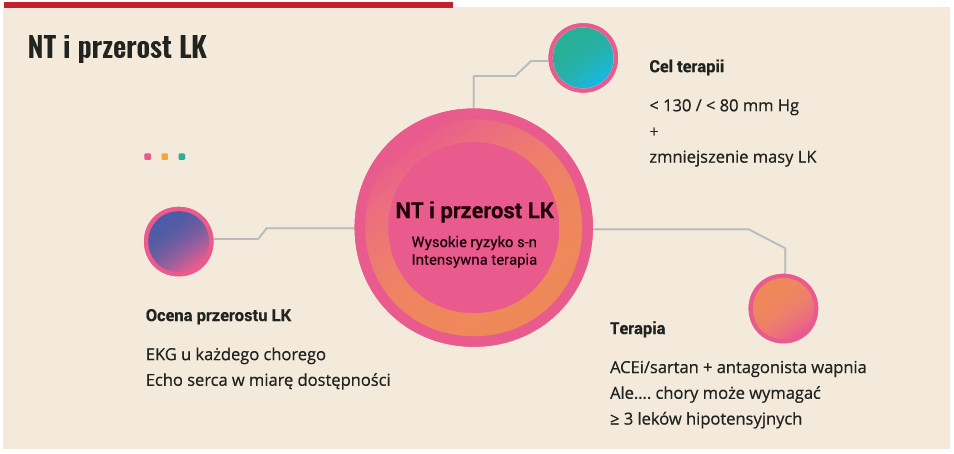
P.D.: – Najprostszą metodą jest badanie elektrokardiograficzne, czyli EKG. Jest kilka wskaźników pozwalających na rozpoznanie LVH, jednak należy pamiętać, że EKG ma niską czułość, ale wysoką swoistość. To znaczy, że jeśli rozpoznamy w tym badaniu LVH, istnieje duże prawdopodobieństwo jego potwierdzenia w badaniu echokardiograficznym. Jeśli natomiast wykluczymy w EKG obecność LVH, nie jest konieczne wykonanie badania echokardiograficznego w celu potwierdzenia. Badanie echokardiograficzne pozwala ocenić grubość tylnej ściany mięśnia, przegrody międzykomorowej oraz wielkość lewej komory. Na tej podstawie szacujemy indeksowaną masę mięśnia lewej komory i współczynnik RWT (stosunek grubości ściany lewej komory do promienia zewnętrznego lewej komory) i szacujemy ryzyko LVH oraz typ przerostu. Złotym standardem w ocenie mięśnia lewej komory jest rezonans magnetyczny, jednak ze względu na ograniczoną dostępność i koszty nie będzie on często wykorzystywany do oceny mięśnia lewej komory.
A jak to jest z albuminurią?
A.P.: – Albuminuria jest bardzo prostym do oceny markerem. Wystarczy porcja moczu. Nie musi to być mocz poranny, może być przygodny. Oznaczamy zarówno stężenie albuminy, jak i kreatyniny, które następnie wyrażamy w postaci ilorazu albuminy do kreatyniny w miligramach na gram. Wynik mówi o nasileniu albuminurii. Albuminuria jest bardzo cennym markerem. Przerost mięśnia lewej komory informuje o przeciążeniowym wpływie ciśnienia tętniczego na mięsień sercowy oraz układ naczyniowy, który powoduje zmiany strukturalne. Albuminuria wskazuje na zmiany funkcjonalne. Sygnalizuje nie tylko uszkodzenie nerek, lecz także uszkodzenie śródbłonka naczyniowego w całym organizmie. Tak więc jest to prosty do oceny, bardzo dobry, powtarzalny marker, korelujący od najniższych wartości do najwyższych z ryzykiem sercowo-naczyniowym. Chciałbym wyjaśnić jeszcze jedną kwestię. Przyzwyczailiśmy się do nazwy mikroalbuminuria, ale obecnie staram się używać innych określeń nieznacznie zwiększonej albuminurii i umiarkowanie zwiększonej, czyli dawnej mikroalbuminurii. Jeżeli wydalanie albuminy z moczem przekracza 30 mg/g, mamy do czynienia z umiarkowanym zwiększeniem albuminurii, dawniej mikroalbuminurią. Pacjenci, u których wydalanie albumin wynosi 10–30 mg/g, a te wartości mieszczą się jeszcze w prawidłowych zakresach, mają nieznacznie zwiększoną albuminurię i nieco większe ryzyko sercowo-naczyniowe niż pacjenci z albuminurią poniżej 10 mg/g.
Jaki jest mechanizm powodujący, że niekontrolowane, źle leczone nadciśnienie tętnicze prowadzi do uszkodzenia mięśnia lewej komory?
P.D.: – Wysokie wartości ciśnienia tętniczego zdecydowanie zwiększają obciążenie mięśnia sercowego. W konsekwencji mięsień lewej komory musi generować większą siłę, żeby przepompować krew do aorty. To skutkuje jego pogrubieniem. Każde podwyższenie wartości ciśnienia tętniczego przekłada się zatem w dłuższej perspektywie na wystąpienie LVH. Dlatego ważna jest skuteczna kontrola ciśnienia tętniczego. Obowiązujące wytyczne podkreślają, że u chorych z LVH konieczne jest obniżenie ciśnienia tętniczego do wartości < 130/80 mm Hg. Ważne jest wykorzystanie w terapii leków hamujących układ renina–angiotensyna–aldosteron. Oczywiście nie będzie to monoterapia, tylko leczenie skojarzone. W tym przypadku preferujemy preparaty złożone oparte na tej grupie leków i antagonistach wapnia.
Co bezpośrednio powoduje albuminurię?
A.P.: – Bezpośrednią przyczyną jest wzrost ciśnienia środkłębuszkowego. Albuminuria jest również skutkiem uszkodzenia śródbłonka, do którego dochodzi m.in. z powodu nadciśnienia tętniczego. Również cukrzyca może prowadzić do upośledzenia funkcji śródbłonka i wzrostu przepuszczalności kłębuszka nerkowego. Jeśli już mówimy o mechanizmach, które prowadzą do albuminurii, to ważne są również mechanizmy terapeutyczne. Zarówno wytyczne europejskie, jak i rodzime wskazują, jak należy dobierać terapię nadciśnienia tętniczego, by uchronić pacjentów przed albuminurią. Mamy badania pokazujące, że niektóre leki hipotensyjne zapobiegają wystąpieniu umiarkowanie zwiększonej albuminurii, czyli dawnej mikroalbuminurii. Są to badania z lekami hamującymi układ renina–angiotensyna–aldosteron, np. z olmesartanem. W badaniu ROADMAP wykazano, że ten sartan zapobiega rozwojowi albuminurii u chorych na cukrzycę. Z drugiej strony wytyczne polskie wskazują, że w obrębie innych grup leków hipotensyjnych również są cząsteczki, które charakteryzują się lepszą od pozostałych redukcją ryzyka albuminurii. Na przykład wśród antagonistów wapnia jest to lerkanidypina, która według badań wpływa zarówno na kanaliki doprowadzające, jak i odprowadzające kłębuszka nerkowego, przez co równoważy ciśnienie środkłębuszkowe i dzięki temu ogranicza ryzyko rozwoju albuminurii. Mówiąc o lekach działających na śródbłonek, nie sposób pominąć nebiwololu, który jest β-adrenolitykiem nie tylko kardioselektywnym, lecz także uwalniającym tlenek azotu, a więc wazodylatacyjnym, korzystnie wpływającym na śródbłonek.
Po które leki hipotensyjne warto sięgać, żeby uchronić pacjenta z nadciśnieniem tętniczym przed LVH lub doprowadzić do jego regresu?
P.D.: – Jak powiedziałem, każde podwyższenie ciśnienia tętniczego będzie skutkowało zwiększeniem masy mięśnia lewej komory. I odwrotnie – każde obniżenie wartości będzie się przyczyniało do zmniejszenia masy mięśnia. A więc każdy lek obniżający wartość ciśnienia będzie zmniejszał masę mięśnia lewej komory, czyli będzie zmniejszał przerost. Ale są leki o szczególnej skuteczności hipotensyjnej wykazanej w badaniach. Mam na myśli leki hamujące układ renina–angiotensyna–aldosteron, czyli antagonistów konwertazy angiotensyny i sartany. Przywołam tutaj badania z olmesartanem, silnie i długo działającym sartanem. Wykazały one, że lek ten zmniejsza LVH, prowadzi do regresu przerostu lewej komory przez blokowanie układu renina–angiotensyna–aldosteron. Jest też wiele badań pokazujących, że stosowanie najnowszych kardioselektywnych β-adrenolitykow, do których należy nebiwolol – działający wazodylatacyjnie, bardzo dobrze obniżający wartości ciśnienia tętniczego, wpływający na częstość rytmu serca – sprzyja zmniejszeniu masy mięśnia lewej komory, a więc również obniżeniu ryzyka sercowo-naczyniowego.
Czym grozi LVH? Jaki może być ciąg dalszy? Nadciśnienie tętnicze, następnie przerost lewej komory i…
P.D.: – To jest kontinuum sercowe. Nadciśnienie tętnicze, powodując przerost lewej komory i narastanie blaszki miażdżycowej, będzie odpowiadało za wystąpienie choroby sercowo-naczyniowej na podłożu miażdżycy, czyli dawnej choroby niedokrwiennej serca, choroby wieńcowej. Przerost mięśnia lewej komory może spowodować niedokrwienie mięśnia sercowego, a także być substratem dla poważnych arytmii zagrażających życiu. Najczęściej arytmii komorowych i nadkomorowych, ale również bardzo często migotania przedsionków. Wysokie wartości ciśnienia tętniczego powodują zmiany strukturalne lewej komory przekładające się na powiększenie lewego przedsionka i w następstwie jego przebudowę, co sprzyja migotaniu przedsionków.
Tekst pochodzi z „Kuriera Medycznego” 1/2023.

Piotr Dobrowolski: – To prawda. Na pewno łatwiej zapobiegać, niż leczyć jawne klinicznie choroby sercowo-naczyniowe na podłożu miażdżycy. Dlatego ocena ryzyka sercowo-naczyniowego jest kluczowym elementem postępowania. Powinniśmy je oceniać zarówno podczas wizyt pierwszorazowych, jak i na każdym etapie postępowania farmakologicznego. W 2021 r. ukazały się wytyczne europejskie dotyczące prewencji chorób sercowo-naczyniowych. Zgodnie z nimi u pacjentów bez rozpoznanej choroby sercowo-naczyniowej do oceny ryzyka należy wykorzystać kartę SCORE2 bądź SCORE2-OP w przypadku osób powyżej 70. roku życia. Jest to bardzo dobre narzędzie, które powinno być powszechnie stosowane do wstępnej oceny ryzyka u wszystkich pacjentów. Niestety ta skala nie jest pozbawiona wad. Ocenie podlega tylko pięć czynników: wartość skurczowego ciśnienia tętniczego, stężenie cholesterolu nie-HDL w osoczu, palenie/niepalenie tytoniu, płeć i wiek. Na tej podstawie tak naprawdę jesteśmy w stanie tylko z grubsza ocenić ryzyko sercowo-naczyniowe. Tymczasem, jak wiemy, u pacjentów ze źle leczonym lub nieleczonym nadciśnieniem tętniczym często dochodzi do subklinicznych powikłań narządowych. Najczęściej są to przerost mięśnia lewej komory serca (left ventricular hipertrophy – LVH) i zwiększenie wydalania białka z moczem, czyli albuminuria. To dwa główne powikłania narządowe związane z nadciśnieniem tętniczym. Jeśli one występują u pacjenta, od razu wiemy, że cechuje go dużo większe ryzyko sercowo-naczyniowe niż oszacowane na podstawie kart SCORE2. Przykładowo, jeśli w skali SCORE2 ocenimy, że pacjent ma umiarkowane ryzyko sercowo-naczyniowe, to stwierdzenie jednego z powikłań narządowych – LVH lub albuminurii umiarkowanego stopnia – automatycznie przesuwa go do wyższej klasy ryzyka. Jeśli stwierdzimy obydwa powikłania, to ryzyko będzie jeszcze większe. Dlatego tak ważne jest, by nie dopuścić do rozwoju tych powikłań. W tym celu powinniśmy wdrożyć odpowiednią terapię farmakologiczną od samego początku leczenia chorych z nadciśnieniem tętniczym. Pamiętamy przy tym o pozostałych czynnikach ryzyka sercowo-naczyniowego prowadzących do narastania blaszki miażdżycowej, której pęknięcie może doprowadzić do zawału serca lub udaru mózgu.
Czy można łatwo wykryć istnienie tych dwóch najczęstszych powikłań nadciśnienia tętniczego, czyli LVH i albuminurii?
Aleksander Prejbisz: – Zmiany, które zachodzą w podstawowej opiece zdrowotnej, polegające na wprowadzeniu do niej opieki koordynowanej czy Krajowej Sieci Kardiologicznej, dają większe możliwości oceny tych powikłań narządowych już na tym etapie. Oczywiście powikłań nadciśnienia tętniczego jest więcej – wzrost sztywności naczyń, rozwój miażdżycy tętnic kończyn dolnych, ale dwa omawiane, czyli LVH i albuminuria, są łatwe w ocenie. Poza tym nie tylko korelują z ryzykiem sercowo-naczyniowym, lecz także są wykładnikami skuteczności leczenia. Jeżeli chory ma już jakieś cechy przerostu mięśnia lewej komory czy zwiększoną albuminurię, skuteczne leczenie będzie prowadziło do regresji tych powikłań. Jest to zatem ważny element dodatkowej kontroli skuteczności terapii nadciśnienia tętniczego przyczyniający się do zmniejszenia ryzyka sercowo-naczyniowego. Oczywiście karta SCORE2 powinna być wykorzystywana, ale w wielu przypadkach należy wykraczać poza nią i indywidualizować ocenę ryzyka sercowo-naczyniowego poprzez wykorzystanie markerów ryzyka, które mają absolutne uzasadnienie w wytycznych. Dzięki opiece koordynowanej dostępność tych markerów dla lekarzy podstawowej opieki zdrowotnej, a przede wszystkim dla pacjentów jest większa.
Jak często stwierdza się LVH u chorych na nadciśnienie tętnicze?
P.D.: – W badaniu Framingham w obserwowanej populacji ogólnej LVH oceniany echokardiograficznie był obecny u 37 proc. osób. U pacjentów z opornym nadciśnieniem tętniczym występuje on znacznie częściej. W ocenie echokardiograficznej, w zależności od przyjętych kryteriów, stwierdzano go u 55–81 proc. pacjentów. Najczęstszy jest łagodny przerost w postaci tzw. koncentrycznej przebudowy lewej komory, gdy dojdzie do nasilenia przebudowy, mówimy o koncentrycznym przeroście mięśnia lewej komory. Już od badania Framingham wiemy, że każde zwiększenie masy mięśnia lewej komory jest związane z gorszym rokowaniem sercowo-naczyniowym. Gdy dojdzie do koncentrycznego przerostu, chory ma największe ryzyko sercowo-naczyniowe.
Jakimi metodami można stwierdzić LVH?
P.D.: – Najprostszą metodą jest badanie elektrokardiograficzne, czyli EKG. Jest kilka wskaźników pozwalających na rozpoznanie LVH, jednak należy pamiętać, że EKG ma niską czułość, ale wysoką swoistość. To znaczy, że jeśli rozpoznamy w tym badaniu LVH, istnieje duże prawdopodobieństwo jego potwierdzenia w badaniu echokardiograficznym. Jeśli natomiast wykluczymy w EKG obecność LVH, nie jest konieczne wykonanie badania echokardiograficznego w celu potwierdzenia. Badanie echokardiograficzne pozwala ocenić grubość tylnej ściany mięśnia, przegrody międzykomorowej oraz wielkość lewej komory. Na tej podstawie szacujemy indeksowaną masę mięśnia lewej komory i współczynnik RWT (stosunek grubości ściany lewej komory do promienia zewnętrznego lewej komory) i szacujemy ryzyko LVH oraz typ przerostu. Złotym standardem w ocenie mięśnia lewej komory jest rezonans magnetyczny, jednak ze względu na ograniczoną dostępność i koszty nie będzie on często wykorzystywany do oceny mięśnia lewej komory.
A jak to jest z albuminurią?
A.P.: – Albuminuria jest bardzo prostym do oceny markerem. Wystarczy porcja moczu. Nie musi to być mocz poranny, może być przygodny. Oznaczamy zarówno stężenie albuminy, jak i kreatyniny, które następnie wyrażamy w postaci ilorazu albuminy do kreatyniny w miligramach na gram. Wynik mówi o nasileniu albuminurii. Albuminuria jest bardzo cennym markerem. Przerost mięśnia lewej komory informuje o przeciążeniowym wpływie ciśnienia tętniczego na mięsień sercowy oraz układ naczyniowy, który powoduje zmiany strukturalne. Albuminuria wskazuje na zmiany funkcjonalne. Sygnalizuje nie tylko uszkodzenie nerek, lecz także uszkodzenie śródbłonka naczyniowego w całym organizmie. Tak więc jest to prosty do oceny, bardzo dobry, powtarzalny marker, korelujący od najniższych wartości do najwyższych z ryzykiem sercowo-naczyniowym. Chciałbym wyjaśnić jeszcze jedną kwestię. Przyzwyczailiśmy się do nazwy mikroalbuminuria, ale obecnie staram się używać innych określeń nieznacznie zwiększonej albuminurii i umiarkowanie zwiększonej, czyli dawnej mikroalbuminurii. Jeżeli wydalanie albuminy z moczem przekracza 30 mg/g, mamy do czynienia z umiarkowanym zwiększeniem albuminurii, dawniej mikroalbuminurią. Pacjenci, u których wydalanie albumin wynosi 10–30 mg/g, a te wartości mieszczą się jeszcze w prawidłowych zakresach, mają nieznacznie zwiększoną albuminurię i nieco większe ryzyko sercowo-naczyniowe niż pacjenci z albuminurią poniżej 10 mg/g.
Jaki jest mechanizm powodujący, że niekontrolowane, źle leczone nadciśnienie tętnicze prowadzi do uszkodzenia mięśnia lewej komory?
P.D.: – Wysokie wartości ciśnienia tętniczego zdecydowanie zwiększają obciążenie mięśnia sercowego. W konsekwencji mięsień lewej komory musi generować większą siłę, żeby przepompować krew do aorty. To skutkuje jego pogrubieniem. Każde podwyższenie wartości ciśnienia tętniczego przekłada się zatem w dłuższej perspektywie na wystąpienie LVH. Dlatego ważna jest skuteczna kontrola ciśnienia tętniczego. Obowiązujące wytyczne podkreślają, że u chorych z LVH konieczne jest obniżenie ciśnienia tętniczego do wartości < 130/80 mm Hg. Ważne jest wykorzystanie w terapii leków hamujących układ renina–angiotensyna–aldosteron. Oczywiście nie będzie to monoterapia, tylko leczenie skojarzone. W tym przypadku preferujemy preparaty złożone oparte na tej grupie leków i antagonistach wapnia.
Co bezpośrednio powoduje albuminurię?
A.P.: – Bezpośrednią przyczyną jest wzrost ciśnienia środkłębuszkowego. Albuminuria jest również skutkiem uszkodzenia śródbłonka, do którego dochodzi m.in. z powodu nadciśnienia tętniczego. Również cukrzyca może prowadzić do upośledzenia funkcji śródbłonka i wzrostu przepuszczalności kłębuszka nerkowego. Jeśli już mówimy o mechanizmach, które prowadzą do albuminurii, to ważne są również mechanizmy terapeutyczne. Zarówno wytyczne europejskie, jak i rodzime wskazują, jak należy dobierać terapię nadciśnienia tętniczego, by uchronić pacjentów przed albuminurią. Mamy badania pokazujące, że niektóre leki hipotensyjne zapobiegają wystąpieniu umiarkowanie zwiększonej albuminurii, czyli dawnej mikroalbuminurii. Są to badania z lekami hamującymi układ renina–angiotensyna–aldosteron, np. z olmesartanem. W badaniu ROADMAP wykazano, że ten sartan zapobiega rozwojowi albuminurii u chorych na cukrzycę. Z drugiej strony wytyczne polskie wskazują, że w obrębie innych grup leków hipotensyjnych również są cząsteczki, które charakteryzują się lepszą od pozostałych redukcją ryzyka albuminurii. Na przykład wśród antagonistów wapnia jest to lerkanidypina, która według badań wpływa zarówno na kanaliki doprowadzające, jak i odprowadzające kłębuszka nerkowego, przez co równoważy ciśnienie środkłębuszkowe i dzięki temu ogranicza ryzyko rozwoju albuminurii. Mówiąc o lekach działających na śródbłonek, nie sposób pominąć nebiwololu, który jest β-adrenolitykiem nie tylko kardioselektywnym, lecz także uwalniającym tlenek azotu, a więc wazodylatacyjnym, korzystnie wpływającym na śródbłonek.
Po które leki hipotensyjne warto sięgać, żeby uchronić pacjenta z nadciśnieniem tętniczym przed LVH lub doprowadzić do jego regresu?
P.D.: – Jak powiedziałem, każde podwyższenie ciśnienia tętniczego będzie skutkowało zwiększeniem masy mięśnia lewej komory. I odwrotnie – każde obniżenie wartości będzie się przyczyniało do zmniejszenia masy mięśnia. A więc każdy lek obniżający wartość ciśnienia będzie zmniejszał masę mięśnia lewej komory, czyli będzie zmniejszał przerost. Ale są leki o szczególnej skuteczności hipotensyjnej wykazanej w badaniach. Mam na myśli leki hamujące układ renina–angiotensyna–aldosteron, czyli antagonistów konwertazy angiotensyny i sartany. Przywołam tutaj badania z olmesartanem, silnie i długo działającym sartanem. Wykazały one, że lek ten zmniejsza LVH, prowadzi do regresu przerostu lewej komory przez blokowanie układu renina–angiotensyna–aldosteron. Jest też wiele badań pokazujących, że stosowanie najnowszych kardioselektywnych β-adrenolitykow, do których należy nebiwolol – działający wazodylatacyjnie, bardzo dobrze obniżający wartości ciśnienia tętniczego, wpływający na częstość rytmu serca – sprzyja zmniejszeniu masy mięśnia lewej komory, a więc również obniżeniu ryzyka sercowo-naczyniowego.
Czym grozi LVH? Jaki może być ciąg dalszy? Nadciśnienie tętnicze, następnie przerost lewej komory i…
P.D.: – To jest kontinuum sercowe. Nadciśnienie tętnicze, powodując przerost lewej komory i narastanie blaszki miażdżycowej, będzie odpowiadało za wystąpienie choroby sercowo-naczyniowej na podłożu miażdżycy, czyli dawnej choroby niedokrwiennej serca, choroby wieńcowej. Przerost mięśnia lewej komory może spowodować niedokrwienie mięśnia sercowego, a także być substratem dla poważnych arytmii zagrażających życiu. Najczęściej arytmii komorowych i nadkomorowych, ale również bardzo często migotania przedsionków. Wysokie wartości ciśnienia tętniczego powodują zmiany strukturalne lewej komory przekładające się na powiększenie lewego przedsionka i w następstwie jego przebudowę, co sprzyja migotaniu przedsionków.

Tekst pochodzi z „Kuriera Medycznego” 1/2023.