Jakie błędy występują w leczeniu astmy w Polsce?

W Polsce ponad 4 mln osób ma objawy astmy, ale tylko 2,2 mln jest aktywnie leczonych. Ponad 7 lat mija od pierwszych objawów astmy do rozpoznania. Stosując leki wziewne, 75% chorych popełnia błędy krytyczne, praktycznie uniemożliwiające skuteczną aerozoloterapię. Tylko 20% chorych osiąga pełną kontrolę, ponad połowa ma niepełną kontrolę, a 30% nie kontroluje choroby, co często doprowadza do zaostrzeń. Dzięki edukacji poprawia się przestrzeganie zaleceń terapeutycznych przez chorych, co przekłada się na zwiększenie skuteczności terapii.
Autorzy: Piotr Dąbrowiecki, Andrzej Dąbrowski, Radosław Gawlik, Wojciech Barg, Grażyna Bochenek, Grzegorz Brożek, Rafał Dobek, Marek Leszek Kowalski, Aleksandra Kucharczyk, Maciej Kupczyk, Izabela Kupryś-Lipińska, Agnieszka Mastalerz-Migas
Wstęp
Astma jest obecnie jedną z najczęściej stwierdzanych przewlekłych chorób cywilizacyjnych, występującą w różnych grupach – zarówno dzieci, jak i dorosłych. Obecnie u większości z nich można uzyskać dobrą kontrolę objawów choroby i zapobiegać występowaniu jej zaostrzeń.
Należy zwrócić uwagę, że wielu chorych z typowymi objawami astmy (kaszel, świsty, duszności) długo nie ma ustalonego rozpoznania [1]. W Polsce, podobnie jak np. w Hiszpanii i Irlandii, chorzy czekają średnio ponad 7 lat na rozpoznanie astmy pomimo objawów wskazujących na tę chorobę. Upływ czasu do ustalenia rozpoznania działa na niekorzyść pacjenta, powoduje nieodwracalne pogorszenie przebiegu choroby.
Pomocą w wyborze metod diagnostyki, leczenia i kontroli astmy są publikowane od wielu lat i powszechnie stosowane wytyczne, np. raport GINA 2020 [2]. Wytyczne GINA dotyczą też uwzględnienia konieczności włączenia chorych w proces leczenia astmy poprzez przekazywanie informacji o jej przyczynach i zależności przebiegu nie tylko od skuteczności wybranej indywidualnie dla pacjenta strategii leczenia farmakologicznego, ale w dużej mierze również od aktywnej współpracy chorego. Zachowania chorych w czasie zaplanowanego przez lekarza długoterminowego leczenia astmy decydują o jego klinicznej efektywności.
Decydujący wpływ na zachowania chorych na astmę mają relacje z lekarzem prowadzącym leczenie i organizującym jego warunki systemem opieki medycznej, umożliwiającym np. dostęp do leków i koniecznych badań. Kluczem do uzyskania adherencji chorego do długoterminowego leczenia i dobrej efektywności opieki medycznej jest utrzymanie właściwej komunikacji z pacjentem. Dotyczy to nie tylko relacji chorego z lekarzem, lecz także pozostałymi profesjonalnymi członkami systemu opieki, np. pielęgniarkami, fizjoterapeutami, farmaceutami. Od jakości tych relacji zależy budowanie motywacji chorego do przewlekłego stosowania leczenia i poprawa jego umiejętności prawidłowego posługiwania się różnymi technikami podawania leków wziewnie. Indywidualny dobór urządzenia dostarczającego lek do oskrzeli jest równie ważny jak strategia leczenia.
Adherencja
Astma należy do chorób przewlekłych o słabej adherencji chorych do zaleceń. Wykazano, że tylko 8–13% chorych, którym przepisano leki, kontynuuje realizację nowych zleceń po roku, a ci, którzy kontynuują leczenie, stosują mniej niż 50% przepisywanych dawek leków [3, 4].
Najczęściej zła adherencja chorego do przepisanego leczenia wynika z zapominania złożonego algorytmu lub niezrozumienia jego celów, koniecznych technik użycia leków wziewnych oraz lęku przed ich ewentualnymi działaniami niepożądanymi. Popełniane błędy zwiększają ryzyko zaostrzeń astmy, obniżają jakość życia chorych i przyczyniają się do zwiększenia kosztów opieki medycznej. Dlatego konieczna jest ocena w czasie wizyt kontrolnych, czy zalecenia są stosowane zgodnie z planem leczenia i w jakim stopniu można pomóc choremu w pokonywaniu indywidualnie występujących trudności. Właściwa opieka nad chorym na astmę musi też uwzględniać dostosowaną do możliwości pacjenta lub jego opiekuna edukację o astmie i celach leczenia oraz poprawiać technikę aplikowania leków wziewnie. Obecnie w wielu krajach stosowane są w tym celu dostępne już dla większości chorych metody komunikacji i uzyskiwania informacji o astmie oparte na technikach interaktywnych z wykorzystaniem programów komputerowych i smartfonów. Nowe technologie komunikacji tworzą nowe formy relacji pomiędzy chorym a systemem opieki medycznej. Jedną z nich są funkcjonujące już powszechnie i akceptowane przez chorych teleporady. Powstają też grupy pacjentów komunikujących się na platformach internetowych i uzyskujących tą drogą nie tylko informacje o astmie i jej leczeniu, lecz także wsparcie psychologiczne i pomoc w podtrzymaniu adherencji do leczenia [5].
Obecnie w Polsce w ramach Projektu Astma Zero prowadzona jest analiza leczenia astmy na podstawie danych uzyskanych z preskrypcji recept realizowanych w reprezentatywnej grupie 5600 aptek z uwzględnieniem: klasy leków, wieku chorych, położenia terytorialnego i specjalizacji lekarzy wystawiających recepty. Szczególnym przedmiotem analizy tysięcy danych jest wykorzystywanie leków wziewnych stosowanych doraźnie do leczenia zaostrzeń astmy – krótko działających β2-mimetyków (short acting β-agonists – SABA) oraz leków przeciwzapalnych – glikokortykosterydów (wGKS), zarówno osobno, jak i w połączeniu z długo działającymi β2-mimetykami (long acting β-agonists – LABA) oraz GKS stosowanymi systemowo.
Projekt Astma Zero wykazał, że w Polsce u chorych stosujących SABA średnia liczba realizowanych recept wynosi 3,6 opakowania na rok, a aż 6% pacjentów zużywa ponad 12 opakowań SABA rocznie [1]. Jednocześnie aż 22% pacjentów przyjmujących SABA stosowało te leki w monoterapii. Stosowanie SABA w Polsce jest zróżnicowane regionalnie (ryc. 1).

W naszym badaniu obserwowaliśmy zużycie większej ilości niż 3 opakowania SABA rocznie w zachodnich regionach kraju, co może wskazywać na nadużywanie SABA w leczeniu.
Ważnym elementem terapii jest przedstawienie choremu zasad leczenia astmy, dawkowania leków, a w przypadku stosowania inhalatorów – pokazanie prawidłowej techniki ich stosowania. Pacjent pozostawiony sam sobie dąży do uzyskania choćby chwilowej poprawy komfortu oddychania. To sprawia, że chory czuje się dobrze, stosując jednocześnie kilka wziewów SABA tygodniowo, a zdarza się, że dziennie. Takie postępowanie umyka uwadze lekarzy podczas wizyt kontrolnych, co wykazało nasze badanie [6]. Lekarze POZ stosowali SABA w monoterapii u 8,8% chorych na astmę. Niestety aż 40% chorych na astmę epizodyczną i wysiłkową miało zlecone SABA w monoterapii. Obserwowaliśmy też, że wraz z nasilaniem się dolegliwości z powodu astmy zwiększa się głównie dawka leków ratunkowych. Wykazano, że najwięcej SABA przepisywano pacjentom na wyższych stopniach leczenia astmy.
Pacjenci popełniają istotne błędy podczas stosowania inhalatorów, pomimo że są one powszechnie wykorzystywane w leczeniu astmy i POChP. Powoduje to, że inhalowany lek w niewielkim odsetku dociera do płuc, nie działa zatem efektywnie. Ocenia się, że w najlepszym przypadku do płuc trafia 45% leku, a w najgorszym tylko 4% [7].
Nadmierne poleganie przez chorych na SABA wiąże się z prawie dwukrotnym wzrostem ryzyka ciężkiego zaostrzenia astmy, definiowanego jako hospitalizacja, wizyta na SOR-ze lub konieczność systemowego stosowania GKS. W przeprowadzonej analizie konsekwencją nadużywania SABA był znaczny odsetek wizyt nieplanowanych (24,6% pacjentów) oraz interwencji pogotowia ratunkowego, porad doraźnych na SOR-ze i hospitalizacji (odpowiednio 5,4–6% i 5,4%) z powodu zaostrzeń astmy [8].
Nieskuteczność inhalacji (w wyniku błędów popełnianych przez chorego podczas stosowania inhalatora) skłania do przyjmowania kolejnych dawek leków, często z różnych rodzajów inhalatorów. Używanie różnych rodzajów inhalatorów sprzyja popełnianiu błędów. Pacjenci chętniej wybierają terapie łączone z zastosowaniem jednego inhalatora (np. wGKS z formoterolem), co poprawia compliance i adherencję [9].
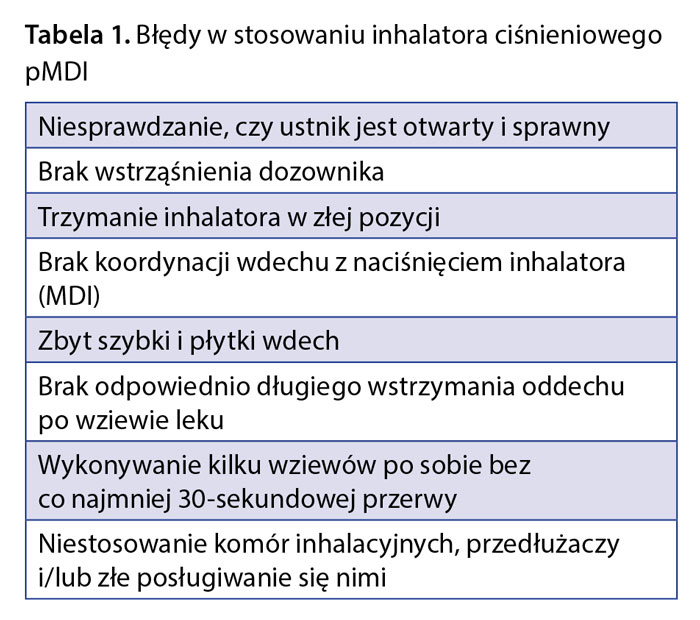
W tabelach 1 i 2 przedstawiono najczęściej popełniane błędy przy stosowaniu leków wziewnie.

Czynniki systemowe
Na sposób leczenia astmy wpływają także czynniki organizacyjne oraz kryteria refundacyjne. Zarówno brak aktualnego zaświadczenia od specjalisty o sposobie leczenia astmy, jak i jego treść kształtują decyzje terapeutyczne lekarzy rodzinnych. Bez zaświadczenia od specjalisty lub gdy zaświadczenie straci ważność (po roku), lekarze POZ mogą się obawiać przepisywać pacjentom leki z refundacją. Dlatego często przepisują leki ze 100-procentową odpłatnością i starają się wybierać preparaty tanie, co może prowadzić do wyboru SABA.
W wyniku analizy leczenia astmy w Polsce w ramach Programu Astma Zero wiemy, że 40% lekarzy POZ jest proszonych przez pacjentów o przepisanie tylko salbutamolu, a 18% tylko fenoterolu. Sytuacja taka zawsze wymaga wyjaśnienia i może wskazywać na słabą adherencję do zaleceń. Wybór połączenia wGKS i formoterolu rozwiązuje problem unikania przez chorych stosowania przewlekle wGKS. Stosując lek doraźnie, uwalniają się od objawów choroby (formoterol) oraz działają przeciwzapalnie (wGKS).
Należy zwrócić uwagą na dawne, ale wciąż obecne w ChPL zapisy, powstałe jeszcze w czasie postrzegania astmy jako choroby skurczowej oskrzeli, zalecające stosowanie SABA jako profilaktyki przed wysiłkiem w astmie wysiłkowej i/lub przed spodziewanym kontaktem z alergenem wywołującym zwykle duszności. Doraźne stosowanie SABA (bez wGKS) nie odpowiada aktualnym wytycznym GINA.
Glikokortykosteroidy w leczeniu astmy
Podstawą leczenia astmy są wGKS. Niechęć chorych do ich stosowania wynika z niezrozumienia znaczenia ich działania przeciwzapalnego w leczeniu podtrzymującym astmy oraz z obaw o występowanie objawów niepożądanych, przede wszystkim przyrostu masy ciała. Co więcej, w przeciwieństwie do SABA i formoterolu, wGKS nie powodują szybkiego ustąpienia duszności. Są więc często postrzegane przez chorych jako leki mniej skuteczne i mniej przydatne w leczeniu astmy w porównaniu z lekami ratunkowymi. Dlatego najczęstszym błędem popełnianym przez chorych jest samowolne przerywanie leczenia wGKS. Ma to tym większe znaczenie, że odstawienie wGKS po okresie ich regularnego stosowania nie powoduje nagłego zaostrzenia objawów. Objawy zaczynają stopniowo narastać zwykle dopiero po kilku tygodniach, nie są więc wiązane przez chorego z zaprzestaniem leczenia przeciwzapalnego, a traktowane jako naturalny i nieunikniony przebieg astmy. Dlatego bardzo korzystne jest używanie preparatów złożonych – typu combo – zawierających wGKS i formoterol, stosowanych w terapii doraźnej i podtrzymującej. Chory jest wówczas „nagradzany” ustąpieniem lub co najmniej zmniejszeniem objawów bezpośrednio po przyjęciu leków i nie ma wątpliwości co do ich skuteczności. Taka kombinacja nie tylko wymusza regularne stosowanie wGKS, lecz także automatycznie powoduje zwiększenie dawki wGKS w razie nasilenia choroby i częstszego sięgania po lek ratunkowy.
Mniej częstą, ale istotną przyczyną niestosowania wGKS są miejscowe objawy niepożądane, przede wszystkim zapalenia jamy ustnej i chrypka. Wynikają one z niewłaściwego stosowania lub z właściwości fizycznych zaordynowanego wGKS. Problem zazwyczaj udaje się rozwiązać poprzez płukanie jamy ustnej po inhalacji wGKS, ewentualnie zmianę preparatu wGKS na mniej drażniący miejscowo.
W badaniu Astma Zero wykazano częste stosowanie doustnie GKS (dGKS), aż u 6% chorych na astmę w wieku 12–44 lat. Brak terapii kontrolującej i oznaki słabej kontroli astmy, takie jak nadużywanie SABA lub GKS w nebulizacji (GKS-neb), znacznie zwiększają ryzyko otrzymania dGKS. Ponad 2/3 tych chorych otrzymały jedno lub dwa opakowania dGKS w roku, ale z ostatnio opublikowanych dużych badań populacyjnych wiadomo, że nawet tak niewielkie dawki dGKS znacząco zwiększają ryzyko wystąpienia poważnych działań niepożądanych, przede wszystkim zapaleń płuc, cukrzycy typu 2, osteoporozy, chorób sercowo-naczyniowych, depresji i zaćmy [10, 11].
Zgodnie z aktualnymi wytycznymi GINA stosowanie dGKS powinno być ograniczone jedynie do najcięższych postaci astmy. Należy przyjąć zasadę, że konieczność zastosowania nawet krótkiego kursu dGKS z powodu astmy powinna powodować konsultację specjalistyczną w celu rozważenia kwalifikacji chorego do leczenia biologicznego w ramach oferowanych przez NFZ programów lekowych. W badaniu Astma Zero obserwowano również zróżnicowanie regionalne stosowania dGKS. Mapa na rycinie 2 pokazuje okolice, w których więcej niż 9% chorych na astmę stosowało dGKS co najmniej jeden raz w roku.

Tereny te rozciągają się szerokim pasem od województwa podkarpackiego i małopolskiego poprzez świętokrzyskie, łódzkie, wielkopolskie aż do zachodniopomorskiego. Trudno jednoznacznie wyjaśnić przyczyny tak dużych różnic regionalnych w stosowaniu dGKS. Najpewniej wynikają one z nawyków terapeutycznych oraz niedostatecznej wiedzy na temat aktualnych zasad leczenia astmy wśród tamtejszych lekarzy.
Badanie Astma Zero wskazuje na jeszcze dwie inne nieprawidłowości leczenia astmy u młodzieży (12–18 lat) i młodych dorosłych (18–44 lata) – częste przyjmowanie doraźne GKS-neb oraz szerokie stosowanie leków antyleukotrienowych (leukotriene receptor antagonist – LTRA). Nieregularne leczenie przy użyciu GKS-neb dotyczyło aż 33% młodzieży i 11% młodych dorosłych. Takie stosowanie GKS-neb wskazuje na złą kontrolę astmy – brak lub niewystarczające stosowanie leków przeciwzapalnych. W badanej populacji 8% chorych stosuje LTRA jako jedyną terapię kontrolującą, dotyczy to 6% dorosłych i aż 17% młodzieży. Ponadto aż 1/3 młodzieży i ponad 1/4 dorosłych przyjmowała LTRA jako dodatkowe leki kontrolujące. Zwraca też uwagę, że 12% nastolatków i 5% dorosłych spośród stosujących dGKS nie zażywało innych leków kontrolujących poza LTRA. Tak powszechne stosowanie GKS-neb i LTRA sugeruje bezrefleksyjną kontynuację terapii astmy dziecięcej w późniejszym wieku.
Propozycje rozwiązań
Pacjenci, u których rozpoznajemy astmę, powinni przejść szkolenie dotyczące praktycznych zasad postępowania z chorobą. Pakiet minimum powinien obejmować wyjaśnienie, że astma jest chorobą zapalną i dlatego chory powinien stosować wGKS. Pokazanie i sprawdzenie, jak pacjent przyjmuje leki wziewne, stanowi niezbędny element edukacji, bez którego trudno osiągnąć sukces terapeutyczny. Ponad 75% chorych przyjmuje leki wziewne w sposób nieprawidłowy. Sprawdzenie poprawności aerozoloterapii i wskazanie błędów, które popełnia chory, poprawia kontrolę choroby [12]. Ważne jest nauczenie chorego na astmę prawidłowej techniki inhalacji. Sama ustna instrukcja nie wystarczy, należy pokazać, a następnie wraz z chorym przećwiczyć prawidłową technikę, oceniając jej wykonanie. To wszystko wymaga przynajmniej kilkunastominutowego instruktażu. Jak to zrealizować w naszych warunkach udzielania porady medycznej? Pomocne dla chorego mogą być łatwo dostępne aplikacje prezentujące prawidłowe techniki użycia różnych inhalatorów (dostępne online: https://use-inhalers.com/pl, https://dlapacjentow.pta.med.pl/, https://szkolaastmy.mp.pl/). Dodatkowym problemem, z którym muszą się mierzyć pacjenci, jest brak pisemnego planu leczenia astmy. Niestety tylko 20% chorych posiada taki plan [13], który jest bardzo pomocny w trakcie zaostrzenia. Pacjenci z objawową astmą wymagający terapii w stopniu GINA 3–5 powinni być wyposażeni dodatkowo w mierniki szczytowego przepływu wydechowego (pikflometry), które w istotny sposób ułatwiają kontrolę choroby, szczególnie u chorych z zaburzoną percepcją odczucia duszności.
W przypadku braku pewności co do rozpoznania astmy monitorowanie zmian szczytowego przepływu wydechowego (peak expiratory flow – PEF) w ciągu dnia może pomóc ustalić to rozpoznanie.
Wyniki badania PEF typowe dla astmy: 1) dobowa zmienność PEF > 10% (średnia z 1–2 tygodni pomiarów), najlepiej powyżej 20%, 2) po 4 tygodniach leczenia przeciwzapalnego wGKS – przyrost PEF o 20% w porównaniu z wartością wyjściową, 3) spadek PEF o 15% po wysiłku w porównaniu z wartością wyjściową.
Monitorowanie PEF pozwala również ustalić, którzy chorzy nie osiągnęli wymaganej kontroli choroby (duża zmienność okołodobowa wartości PEF > 20%). Polecając choremu urządzenie do pomiarów PEF, powinniśmy uwzględnić jego indywidualne preferencje. Z punktu widzenia pacjenta wygodniejsze wydają się urządzenia elektroniczne. Po podłączeniu do smartfona automatycznie zapisują wyniki w pamięci urządzenia, umożliwiają wizualizację wykresu oraz automatycznie kwalifikują wynik do 3 stref: zielonej – bezpiecznej, żółtej – nakazującej działanie, oraz czerwonej – wskazującej na zaostrzenie [14]. W niektórych nowoczesnych pikflometrach elektronicznych, np. Smart Peak Flow, pacjent może dodać krótki komentarz do wyniku badania (pozwalający zobiektywizować przyczynę wystąpienia duszności), wpisać liczbę przyjętych leków doraźnych, a następnie udostępnić te dane online swojemu lekarzowi. Co więcej, zainstalowane oprogramowanie przypomni choremu o konieczności wykonania badania PEF w kolejnych dniach.
Analizując badania, możemy stwierdzić, że 94% chorych na astmę chciałoby żyć bez objawów choroby, ale aż do 78% osób z tej grupy nie przestrzega zaleceń lekarskich [15]. Ten ewidentny konflikt zachowań rodzi problemy. Najczęstszą przyczyną braku współpracy chorego jest skomplikowany algorytm leczenia, trudności z użyciem inhalatora oraz niezrozumienie celów terapii. Brak edukacji chorych w zakresie leczenia i potencjalnych powikłań stwarza zagrożenia, którym może zapobiec dobra komunikacja z lekarzem [9].
Podsumowanie
Błędem jest zwlekanie z rozpoznaniem astmy u chorych z przewlekłymi objawami świadczącymi o tej chorobie. Zapominanie o konieczności edukacji powoduje, że chorzy przerywają leczenie i nie mogą uzyskać kontroli choroby. W konsekwencji nadużywają SABA. Ze względu na brak pisemnego planu leczenia astmy nie można osiągnąć optimum terapeutycznego, a w przypadku zaostrzenia choroby pacjent działa intuicyjnie, nadużywając SABA (tab. 3).

Obecnie tylko 30% chorych w Polsce osiąga pełną kontrolę astmy, ponad połowa ma objawy świadczące o niepełnej kontroli choroby, a 20% ma stałe objawy świadczące o braku kontroli i zbliżającym się zaostrzeniu astmy [16]. Chorzy mający problem z uzyskaniem kontroli astmy powinni być kierowani na konsultacje do specjalisty. Opisane w artykule nieprawidłowości możemy zmienić. Przeczytajmy wspólnie najnowsze wytyczne GINA w zakresie leczenia astmy i wprowadźmy je w naszej codziennej praktyce lekarskiej.
Piśmiennictwo
1. Kupczyk M, Barg W, Bochenek G i wsp. Overprescription of short-acting beta2-agonists in asthma management? Pharmacy reports from 91,673 patients in Poland. Eur Respir J 2019; 54: OA2107.
2. https://ginasthma.org/gina-reports/2020
3. Borrelli B, Riekert KA, Wenstein A i wsp. Brief motivational interviewing as a clinical strategy to promote asthma medication adherence. J Allergy Clin Immunol 2007; 120: 1023-1030.
4. Bender BG. Advancing the science of adherence measurment: implications for the clinician. J Allergy Clin Immunol Pract 2013; 1: 92-93.
5. Chongmelaxme B, Lee SS, Dhippayom T i wsp. The effect of telemedicine on asthma control and patient quality of life in adults: a systematic review and metaanalysis. J Allergy Clin Immunol Pract 2019; l7: 199-209.
6. Gawlik R, Bochenek G, Brzostek D i wsp. Overestimation of asthma control and misperception of short-acting ß2-agonists (SABA) use among physicians in Poland. Eur Respir J 2020; 56: 958.
7. Sanchis J, Corrigan C, Levy ML i wsp. Inhaler devices – from theory to practice. Respir Med 2013; 107: 495-502.
8. Stanford RH, Shah MB, D’Souza AO i wsp. Short-acting β-agonist use and its ability to predict future asthma-related outcomes. Ann Allergy Asthma Immunol 2012; 199: 403-407.
9. Makela MJ, Backer V, Hedegaard M i wsp. Adherence to inhaled therapies, health outcomes and costs in patients with asthma and COPD. Respir Med 2013; 107: 1481-1490.
10. Dalal AA, Duh MS, Gozalo L i wsp. Dose-response relationship between long-term systemic corticosteroid use and related complications in patients with severe asthma. J Manag Care Spec Pharm 2016; 22: 833-847.
11. Price DB, Trudo F, Voorham J i wsp. Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy 2018; 11: 193-204.
12. Aksu F, Şahin AD, Şengezer T i wsp. Effect of training by a physician on dynamics of the use of inhaler devices to improve technique in patients with obstructive lung diseases. Allergy Asthma Proc 2016; 37: 98-102.
13. https://efanet.online/ACCESS 2019
14. Pinnock H. Supported self-management for asthma. Breathe (Sheff) 2015; 11: 98-109.
15. Kang MG, Kim JY, Jung JW i wsp. Lost to follow-up in asthmatics does not mean treatment failure: causes and clinical outcomes of non-adherence to outpatient treatment in adult asthma. Allergy Asthma Immunol Res 2013; 5: 357-364.
16. Chazan R. Rozpoznawanie i postępowanie w astmie w 2012 roku. Pneumonol Alergol Pol 2012; 80: 375-382.
17. Haughney J, Fletcher M, Wolfe S i wsp. Features of asthma management: quantifying the patient perspective. BMC Pulm Med 2007; 7: 16-24.
Wstęp
Astma jest obecnie jedną z najczęściej stwierdzanych przewlekłych chorób cywilizacyjnych, występującą w różnych grupach – zarówno dzieci, jak i dorosłych. Obecnie u większości z nich można uzyskać dobrą kontrolę objawów choroby i zapobiegać występowaniu jej zaostrzeń.
Należy zwrócić uwagę, że wielu chorych z typowymi objawami astmy (kaszel, świsty, duszności) długo nie ma ustalonego rozpoznania [1]. W Polsce, podobnie jak np. w Hiszpanii i Irlandii, chorzy czekają średnio ponad 7 lat na rozpoznanie astmy pomimo objawów wskazujących na tę chorobę. Upływ czasu do ustalenia rozpoznania działa na niekorzyść pacjenta, powoduje nieodwracalne pogorszenie przebiegu choroby.
Pomocą w wyborze metod diagnostyki, leczenia i kontroli astmy są publikowane od wielu lat i powszechnie stosowane wytyczne, np. raport GINA 2020 [2]. Wytyczne GINA dotyczą też uwzględnienia konieczności włączenia chorych w proces leczenia astmy poprzez przekazywanie informacji o jej przyczynach i zależności przebiegu nie tylko od skuteczności wybranej indywidualnie dla pacjenta strategii leczenia farmakologicznego, ale w dużej mierze również od aktywnej współpracy chorego. Zachowania chorych w czasie zaplanowanego przez lekarza długoterminowego leczenia astmy decydują o jego klinicznej efektywności.
Decydujący wpływ na zachowania chorych na astmę mają relacje z lekarzem prowadzącym leczenie i organizującym jego warunki systemem opieki medycznej, umożliwiającym np. dostęp do leków i koniecznych badań. Kluczem do uzyskania adherencji chorego do długoterminowego leczenia i dobrej efektywności opieki medycznej jest utrzymanie właściwej komunikacji z pacjentem. Dotyczy to nie tylko relacji chorego z lekarzem, lecz także pozostałymi profesjonalnymi członkami systemu opieki, np. pielęgniarkami, fizjoterapeutami, farmaceutami. Od jakości tych relacji zależy budowanie motywacji chorego do przewlekłego stosowania leczenia i poprawa jego umiejętności prawidłowego posługiwania się różnymi technikami podawania leków wziewnie. Indywidualny dobór urządzenia dostarczającego lek do oskrzeli jest równie ważny jak strategia leczenia.
Adherencja
Astma należy do chorób przewlekłych o słabej adherencji chorych do zaleceń. Wykazano, że tylko 8–13% chorych, którym przepisano leki, kontynuuje realizację nowych zleceń po roku, a ci, którzy kontynuują leczenie, stosują mniej niż 50% przepisywanych dawek leków [3, 4].
Najczęściej zła adherencja chorego do przepisanego leczenia wynika z zapominania złożonego algorytmu lub niezrozumienia jego celów, koniecznych technik użycia leków wziewnych oraz lęku przed ich ewentualnymi działaniami niepożądanymi. Popełniane błędy zwiększają ryzyko zaostrzeń astmy, obniżają jakość życia chorych i przyczyniają się do zwiększenia kosztów opieki medycznej. Dlatego konieczna jest ocena w czasie wizyt kontrolnych, czy zalecenia są stosowane zgodnie z planem leczenia i w jakim stopniu można pomóc choremu w pokonywaniu indywidualnie występujących trudności. Właściwa opieka nad chorym na astmę musi też uwzględniać dostosowaną do możliwości pacjenta lub jego opiekuna edukację o astmie i celach leczenia oraz poprawiać technikę aplikowania leków wziewnie. Obecnie w wielu krajach stosowane są w tym celu dostępne już dla większości chorych metody komunikacji i uzyskiwania informacji o astmie oparte na technikach interaktywnych z wykorzystaniem programów komputerowych i smartfonów. Nowe technologie komunikacji tworzą nowe formy relacji pomiędzy chorym a systemem opieki medycznej. Jedną z nich są funkcjonujące już powszechnie i akceptowane przez chorych teleporady. Powstają też grupy pacjentów komunikujących się na platformach internetowych i uzyskujących tą drogą nie tylko informacje o astmie i jej leczeniu, lecz także wsparcie psychologiczne i pomoc w podtrzymaniu adherencji do leczenia [5].
Obecnie w Polsce w ramach Projektu Astma Zero prowadzona jest analiza leczenia astmy na podstawie danych uzyskanych z preskrypcji recept realizowanych w reprezentatywnej grupie 5600 aptek z uwzględnieniem: klasy leków, wieku chorych, położenia terytorialnego i specjalizacji lekarzy wystawiających recepty. Szczególnym przedmiotem analizy tysięcy danych jest wykorzystywanie leków wziewnych stosowanych doraźnie do leczenia zaostrzeń astmy – krótko działających β2-mimetyków (short acting β-agonists – SABA) oraz leków przeciwzapalnych – glikokortykosterydów (wGKS), zarówno osobno, jak i w połączeniu z długo działającymi β2-mimetykami (long acting β-agonists – LABA) oraz GKS stosowanymi systemowo.
Projekt Astma Zero wykazał, że w Polsce u chorych stosujących SABA średnia liczba realizowanych recept wynosi 3,6 opakowania na rok, a aż 6% pacjentów zużywa ponad 12 opakowań SABA rocznie [1]. Jednocześnie aż 22% pacjentów przyjmujących SABA stosowało te leki w monoterapii. Stosowanie SABA w Polsce jest zróżnicowane regionalnie (ryc. 1).

W naszym badaniu obserwowaliśmy zużycie większej ilości niż 3 opakowania SABA rocznie w zachodnich regionach kraju, co może wskazywać na nadużywanie SABA w leczeniu.
Ważnym elementem terapii jest przedstawienie choremu zasad leczenia astmy, dawkowania leków, a w przypadku stosowania inhalatorów – pokazanie prawidłowej techniki ich stosowania. Pacjent pozostawiony sam sobie dąży do uzyskania choćby chwilowej poprawy komfortu oddychania. To sprawia, że chory czuje się dobrze, stosując jednocześnie kilka wziewów SABA tygodniowo, a zdarza się, że dziennie. Takie postępowanie umyka uwadze lekarzy podczas wizyt kontrolnych, co wykazało nasze badanie [6]. Lekarze POZ stosowali SABA w monoterapii u 8,8% chorych na astmę. Niestety aż 40% chorych na astmę epizodyczną i wysiłkową miało zlecone SABA w monoterapii. Obserwowaliśmy też, że wraz z nasilaniem się dolegliwości z powodu astmy zwiększa się głównie dawka leków ratunkowych. Wykazano, że najwięcej SABA przepisywano pacjentom na wyższych stopniach leczenia astmy.
Pacjenci popełniają istotne błędy podczas stosowania inhalatorów, pomimo że są one powszechnie wykorzystywane w leczeniu astmy i POChP. Powoduje to, że inhalowany lek w niewielkim odsetku dociera do płuc, nie działa zatem efektywnie. Ocenia się, że w najlepszym przypadku do płuc trafia 45% leku, a w najgorszym tylko 4% [7].
Nadmierne poleganie przez chorych na SABA wiąże się z prawie dwukrotnym wzrostem ryzyka ciężkiego zaostrzenia astmy, definiowanego jako hospitalizacja, wizyta na SOR-ze lub konieczność systemowego stosowania GKS. W przeprowadzonej analizie konsekwencją nadużywania SABA był znaczny odsetek wizyt nieplanowanych (24,6% pacjentów) oraz interwencji pogotowia ratunkowego, porad doraźnych na SOR-ze i hospitalizacji (odpowiednio 5,4–6% i 5,4%) z powodu zaostrzeń astmy [8].
Nieskuteczność inhalacji (w wyniku błędów popełnianych przez chorego podczas stosowania inhalatora) skłania do przyjmowania kolejnych dawek leków, często z różnych rodzajów inhalatorów. Używanie różnych rodzajów inhalatorów sprzyja popełnianiu błędów. Pacjenci chętniej wybierają terapie łączone z zastosowaniem jednego inhalatora (np. wGKS z formoterolem), co poprawia compliance i adherencję [9].
W tabelach 1 i 2 przedstawiono najczęściej popełniane błędy przy stosowaniu leków wziewnie.


Czynniki systemowe
Na sposób leczenia astmy wpływają także czynniki organizacyjne oraz kryteria refundacyjne. Zarówno brak aktualnego zaświadczenia od specjalisty o sposobie leczenia astmy, jak i jego treść kształtują decyzje terapeutyczne lekarzy rodzinnych. Bez zaświadczenia od specjalisty lub gdy zaświadczenie straci ważność (po roku), lekarze POZ mogą się obawiać przepisywać pacjentom leki z refundacją. Dlatego często przepisują leki ze 100-procentową odpłatnością i starają się wybierać preparaty tanie, co może prowadzić do wyboru SABA.
W wyniku analizy leczenia astmy w Polsce w ramach Programu Astma Zero wiemy, że 40% lekarzy POZ jest proszonych przez pacjentów o przepisanie tylko salbutamolu, a 18% tylko fenoterolu. Sytuacja taka zawsze wymaga wyjaśnienia i może wskazywać na słabą adherencję do zaleceń. Wybór połączenia wGKS i formoterolu rozwiązuje problem unikania przez chorych stosowania przewlekle wGKS. Stosując lek doraźnie, uwalniają się od objawów choroby (formoterol) oraz działają przeciwzapalnie (wGKS).
Należy zwrócić uwagą na dawne, ale wciąż obecne w ChPL zapisy, powstałe jeszcze w czasie postrzegania astmy jako choroby skurczowej oskrzeli, zalecające stosowanie SABA jako profilaktyki przed wysiłkiem w astmie wysiłkowej i/lub przed spodziewanym kontaktem z alergenem wywołującym zwykle duszności. Doraźne stosowanie SABA (bez wGKS) nie odpowiada aktualnym wytycznym GINA.
Glikokortykosteroidy w leczeniu astmy
Podstawą leczenia astmy są wGKS. Niechęć chorych do ich stosowania wynika z niezrozumienia znaczenia ich działania przeciwzapalnego w leczeniu podtrzymującym astmy oraz z obaw o występowanie objawów niepożądanych, przede wszystkim przyrostu masy ciała. Co więcej, w przeciwieństwie do SABA i formoterolu, wGKS nie powodują szybkiego ustąpienia duszności. Są więc często postrzegane przez chorych jako leki mniej skuteczne i mniej przydatne w leczeniu astmy w porównaniu z lekami ratunkowymi. Dlatego najczęstszym błędem popełnianym przez chorych jest samowolne przerywanie leczenia wGKS. Ma to tym większe znaczenie, że odstawienie wGKS po okresie ich regularnego stosowania nie powoduje nagłego zaostrzenia objawów. Objawy zaczynają stopniowo narastać zwykle dopiero po kilku tygodniach, nie są więc wiązane przez chorego z zaprzestaniem leczenia przeciwzapalnego, a traktowane jako naturalny i nieunikniony przebieg astmy. Dlatego bardzo korzystne jest używanie preparatów złożonych – typu combo – zawierających wGKS i formoterol, stosowanych w terapii doraźnej i podtrzymującej. Chory jest wówczas „nagradzany” ustąpieniem lub co najmniej zmniejszeniem objawów bezpośrednio po przyjęciu leków i nie ma wątpliwości co do ich skuteczności. Taka kombinacja nie tylko wymusza regularne stosowanie wGKS, lecz także automatycznie powoduje zwiększenie dawki wGKS w razie nasilenia choroby i częstszego sięgania po lek ratunkowy.
Mniej częstą, ale istotną przyczyną niestosowania wGKS są miejscowe objawy niepożądane, przede wszystkim zapalenia jamy ustnej i chrypka. Wynikają one z niewłaściwego stosowania lub z właściwości fizycznych zaordynowanego wGKS. Problem zazwyczaj udaje się rozwiązać poprzez płukanie jamy ustnej po inhalacji wGKS, ewentualnie zmianę preparatu wGKS na mniej drażniący miejscowo.
W badaniu Astma Zero wykazano częste stosowanie doustnie GKS (dGKS), aż u 6% chorych na astmę w wieku 12–44 lat. Brak terapii kontrolującej i oznaki słabej kontroli astmy, takie jak nadużywanie SABA lub GKS w nebulizacji (GKS-neb), znacznie zwiększają ryzyko otrzymania dGKS. Ponad 2/3 tych chorych otrzymały jedno lub dwa opakowania dGKS w roku, ale z ostatnio opublikowanych dużych badań populacyjnych wiadomo, że nawet tak niewielkie dawki dGKS znacząco zwiększają ryzyko wystąpienia poważnych działań niepożądanych, przede wszystkim zapaleń płuc, cukrzycy typu 2, osteoporozy, chorób sercowo-naczyniowych, depresji i zaćmy [10, 11].
Zgodnie z aktualnymi wytycznymi GINA stosowanie dGKS powinno być ograniczone jedynie do najcięższych postaci astmy. Należy przyjąć zasadę, że konieczność zastosowania nawet krótkiego kursu dGKS z powodu astmy powinna powodować konsultację specjalistyczną w celu rozważenia kwalifikacji chorego do leczenia biologicznego w ramach oferowanych przez NFZ programów lekowych. W badaniu Astma Zero obserwowano również zróżnicowanie regionalne stosowania dGKS. Mapa na rycinie 2 pokazuje okolice, w których więcej niż 9% chorych na astmę stosowało dGKS co najmniej jeden raz w roku.

Tereny te rozciągają się szerokim pasem od województwa podkarpackiego i małopolskiego poprzez świętokrzyskie, łódzkie, wielkopolskie aż do zachodniopomorskiego. Trudno jednoznacznie wyjaśnić przyczyny tak dużych różnic regionalnych w stosowaniu dGKS. Najpewniej wynikają one z nawyków terapeutycznych oraz niedostatecznej wiedzy na temat aktualnych zasad leczenia astmy wśród tamtejszych lekarzy.
Badanie Astma Zero wskazuje na jeszcze dwie inne nieprawidłowości leczenia astmy u młodzieży (12–18 lat) i młodych dorosłych (18–44 lata) – częste przyjmowanie doraźne GKS-neb oraz szerokie stosowanie leków antyleukotrienowych (leukotriene receptor antagonist – LTRA). Nieregularne leczenie przy użyciu GKS-neb dotyczyło aż 33% młodzieży i 11% młodych dorosłych. Takie stosowanie GKS-neb wskazuje na złą kontrolę astmy – brak lub niewystarczające stosowanie leków przeciwzapalnych. W badanej populacji 8% chorych stosuje LTRA jako jedyną terapię kontrolującą, dotyczy to 6% dorosłych i aż 17% młodzieży. Ponadto aż 1/3 młodzieży i ponad 1/4 dorosłych przyjmowała LTRA jako dodatkowe leki kontrolujące. Zwraca też uwagę, że 12% nastolatków i 5% dorosłych spośród stosujących dGKS nie zażywało innych leków kontrolujących poza LTRA. Tak powszechne stosowanie GKS-neb i LTRA sugeruje bezrefleksyjną kontynuację terapii astmy dziecięcej w późniejszym wieku.
Propozycje rozwiązań
Pacjenci, u których rozpoznajemy astmę, powinni przejść szkolenie dotyczące praktycznych zasad postępowania z chorobą. Pakiet minimum powinien obejmować wyjaśnienie, że astma jest chorobą zapalną i dlatego chory powinien stosować wGKS. Pokazanie i sprawdzenie, jak pacjent przyjmuje leki wziewne, stanowi niezbędny element edukacji, bez którego trudno osiągnąć sukces terapeutyczny. Ponad 75% chorych przyjmuje leki wziewne w sposób nieprawidłowy. Sprawdzenie poprawności aerozoloterapii i wskazanie błędów, które popełnia chory, poprawia kontrolę choroby [12]. Ważne jest nauczenie chorego na astmę prawidłowej techniki inhalacji. Sama ustna instrukcja nie wystarczy, należy pokazać, a następnie wraz z chorym przećwiczyć prawidłową technikę, oceniając jej wykonanie. To wszystko wymaga przynajmniej kilkunastominutowego instruktażu. Jak to zrealizować w naszych warunkach udzielania porady medycznej? Pomocne dla chorego mogą być łatwo dostępne aplikacje prezentujące prawidłowe techniki użycia różnych inhalatorów (dostępne online: https://use-inhalers.com/pl, https://dlapacjentow.pta.med.pl/, https://szkolaastmy.mp.pl/). Dodatkowym problemem, z którym muszą się mierzyć pacjenci, jest brak pisemnego planu leczenia astmy. Niestety tylko 20% chorych posiada taki plan [13], który jest bardzo pomocny w trakcie zaostrzenia. Pacjenci z objawową astmą wymagający terapii w stopniu GINA 3–5 powinni być wyposażeni dodatkowo w mierniki szczytowego przepływu wydechowego (pikflometry), które w istotny sposób ułatwiają kontrolę choroby, szczególnie u chorych z zaburzoną percepcją odczucia duszności.
W przypadku braku pewności co do rozpoznania astmy monitorowanie zmian szczytowego przepływu wydechowego (peak expiratory flow – PEF) w ciągu dnia może pomóc ustalić to rozpoznanie.
Wyniki badania PEF typowe dla astmy: 1) dobowa zmienność PEF > 10% (średnia z 1–2 tygodni pomiarów), najlepiej powyżej 20%, 2) po 4 tygodniach leczenia przeciwzapalnego wGKS – przyrost PEF o 20% w porównaniu z wartością wyjściową, 3) spadek PEF o 15% po wysiłku w porównaniu z wartością wyjściową.
Monitorowanie PEF pozwala również ustalić, którzy chorzy nie osiągnęli wymaganej kontroli choroby (duża zmienność okołodobowa wartości PEF > 20%). Polecając choremu urządzenie do pomiarów PEF, powinniśmy uwzględnić jego indywidualne preferencje. Z punktu widzenia pacjenta wygodniejsze wydają się urządzenia elektroniczne. Po podłączeniu do smartfona automatycznie zapisują wyniki w pamięci urządzenia, umożliwiają wizualizację wykresu oraz automatycznie kwalifikują wynik do 3 stref: zielonej – bezpiecznej, żółtej – nakazującej działanie, oraz czerwonej – wskazującej na zaostrzenie [14]. W niektórych nowoczesnych pikflometrach elektronicznych, np. Smart Peak Flow, pacjent może dodać krótki komentarz do wyniku badania (pozwalający zobiektywizować przyczynę wystąpienia duszności), wpisać liczbę przyjętych leków doraźnych, a następnie udostępnić te dane online swojemu lekarzowi. Co więcej, zainstalowane oprogramowanie przypomni choremu o konieczności wykonania badania PEF w kolejnych dniach.
Analizując badania, możemy stwierdzić, że 94% chorych na astmę chciałoby żyć bez objawów choroby, ale aż do 78% osób z tej grupy nie przestrzega zaleceń lekarskich [15]. Ten ewidentny konflikt zachowań rodzi problemy. Najczęstszą przyczyną braku współpracy chorego jest skomplikowany algorytm leczenia, trudności z użyciem inhalatora oraz niezrozumienie celów terapii. Brak edukacji chorych w zakresie leczenia i potencjalnych powikłań stwarza zagrożenia, którym może zapobiec dobra komunikacja z lekarzem [9].
Podsumowanie
Błędem jest zwlekanie z rozpoznaniem astmy u chorych z przewlekłymi objawami świadczącymi o tej chorobie. Zapominanie o konieczności edukacji powoduje, że chorzy przerywają leczenie i nie mogą uzyskać kontroli choroby. W konsekwencji nadużywają SABA. Ze względu na brak pisemnego planu leczenia astmy nie można osiągnąć optimum terapeutycznego, a w przypadku zaostrzenia choroby pacjent działa intuicyjnie, nadużywając SABA (tab. 3).

Obecnie tylko 30% chorych w Polsce osiąga pełną kontrolę astmy, ponad połowa ma objawy świadczące o niepełnej kontroli choroby, a 20% ma stałe objawy świadczące o braku kontroli i zbliżającym się zaostrzeniu astmy [16]. Chorzy mający problem z uzyskaniem kontroli astmy powinni być kierowani na konsultacje do specjalisty. Opisane w artykule nieprawidłowości możemy zmienić. Przeczytajmy wspólnie najnowsze wytyczne GINA w zakresie leczenia astmy i wprowadźmy je w naszej codziennej praktyce lekarskiej.
Piśmiennictwo
1. Kupczyk M, Barg W, Bochenek G i wsp. Overprescription of short-acting beta2-agonists in asthma management? Pharmacy reports from 91,673 patients in Poland. Eur Respir J 2019; 54: OA2107.
2. https://ginasthma.org/gina-reports/2020
3. Borrelli B, Riekert KA, Wenstein A i wsp. Brief motivational interviewing as a clinical strategy to promote asthma medication adherence. J Allergy Clin Immunol 2007; 120: 1023-1030.
4. Bender BG. Advancing the science of adherence measurment: implications for the clinician. J Allergy Clin Immunol Pract 2013; 1: 92-93.
5. Chongmelaxme B, Lee SS, Dhippayom T i wsp. The effect of telemedicine on asthma control and patient quality of life in adults: a systematic review and metaanalysis. J Allergy Clin Immunol Pract 2019; l7: 199-209.
6. Gawlik R, Bochenek G, Brzostek D i wsp. Overestimation of asthma control and misperception of short-acting ß2-agonists (SABA) use among physicians in Poland. Eur Respir J 2020; 56: 958.
7. Sanchis J, Corrigan C, Levy ML i wsp. Inhaler devices – from theory to practice. Respir Med 2013; 107: 495-502.
8. Stanford RH, Shah MB, D’Souza AO i wsp. Short-acting β-agonist use and its ability to predict future asthma-related outcomes. Ann Allergy Asthma Immunol 2012; 199: 403-407.
9. Makela MJ, Backer V, Hedegaard M i wsp. Adherence to inhaled therapies, health outcomes and costs in patients with asthma and COPD. Respir Med 2013; 107: 1481-1490.
10. Dalal AA, Duh MS, Gozalo L i wsp. Dose-response relationship between long-term systemic corticosteroid use and related complications in patients with severe asthma. J Manag Care Spec Pharm 2016; 22: 833-847.
11. Price DB, Trudo F, Voorham J i wsp. Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy 2018; 11: 193-204.
12. Aksu F, Şahin AD, Şengezer T i wsp. Effect of training by a physician on dynamics of the use of inhaler devices to improve technique in patients with obstructive lung diseases. Allergy Asthma Proc 2016; 37: 98-102.
13. https://efanet.online/ACCESS 2019
14. Pinnock H. Supported self-management for asthma. Breathe (Sheff) 2015; 11: 98-109.
15. Kang MG, Kim JY, Jung JW i wsp. Lost to follow-up in asthmatics does not mean treatment failure: causes and clinical outcomes of non-adherence to outpatient treatment in adult asthma. Allergy Asthma Immunol Res 2013; 5: 357-364.
16. Chazan R. Rozpoznawanie i postępowanie w astmie w 2012 roku. Pneumonol Alergol Pol 2012; 80: 375-382.
17. Haughney J, Fletcher M, Wolfe S i wsp. Features of asthma management: quantifying the patient perspective. BMC Pulm Med 2007; 7: 16-24.
