Baricytinib poprawia wyniki u pacjentów z atopowym zapaleniem skóry
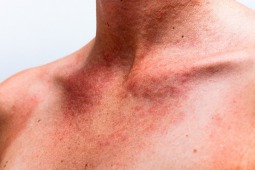
Pacjenci z umiarkowanym do ciężkiego atopowego zapalenia skóry po leczeniu baricytynibem i miejscowym kortykosteroidem mieli lepsze wyniki kliniczne, niż po leczeniu jedynie kortykosteroidami wynika z badań drugiej fazy przedstawionych podczas Europejskiej Akademii Dermatologii i Wenerologii w Genewie.
W analizie włączono 38 chorych leczonych 4-mg barticytynibem oraz miejscowymi kortykosteroidami (TCS), 37 chorych leczonych 2-mg baricytynibem plus TCS, a 49 pacjentów leczonych samym CS. Pacjenci otrzymywali 16 tygodni leczenia i oceniano ich za nasilenie choroby za pomocą wskaźnika Eskema Area (EASI-50).
50% lub więcej zmniejszenia ogólnego nasilenia choroby wystąpiło u 61% pacjentów w grupie przyjmującej baricitinib w dawce 4 mg i o 37% w grupie z TCS ( P<0,05). Inne wyniki wykazały, że 57% uczestników z powodu dawki 2-2 mg baricitinibu osiągnęło wskaźnik EASI-50, co było nieznaczną poprawą w porównaniu z TCS ( P = 0,065).
Po 4 tygodniach 68% pacjentów w grupie 4 mg i 62% pacjentów w grupie 2 mg osiągnęło znak EASI-50, w porównaniu z 16% pacjentów leczonych samym TCS ( P <.001).
Zdarzenia niepożądane związane z leczeniem wyniosły 71% wśród pacjentów leczonych 4 mg baricitinibem, u 46% wśród pacjentów leczonych 2 mg leku badanego i 49% u osób leczonych samym TCS. Najczęstszymi niekorzystnymi zdarzeniami niepożądanymi w leczeniu grupą 4-barową baricitinibu były zakażenia górnych dróg oddechowych, zapalenie nosogardzieli, bóle głowy i wzrost parametrów laboratoryjnych, takich jak fosfokinazy kreatyny.
Wyniki badania sugerują, że baricitinib może mieć możliwość leczenia doustnego u pacjentów cierpiących na atopowe zapalenie skóry, którzy nie są w stanie osiągnąć odpowiedniej poprawy po leczeniu TCS.
Baricytinib jest inhibitorem JAK i w lutym 2017 r. otrzymał zgodę na leczenie reumatoidalnego zapalenia stawów w Unii Europejskiej. W kwietniu 2017 r. lek został zatwierdzony przez FDA i zażądała dodatkowych danych w celu określenia odpowiednich dawek i kwestie bezpieczeństwa terapeutycznego. Obecnie lek ten jest badany w chorobach autoimmunologicznych i zapalnych.
50% lub więcej zmniejszenia ogólnego nasilenia choroby wystąpiło u 61% pacjentów w grupie przyjmującej baricitinib w dawce 4 mg i o 37% w grupie z TCS ( P<0,05). Inne wyniki wykazały, że 57% uczestników z powodu dawki 2-2 mg baricitinibu osiągnęło wskaźnik EASI-50, co było nieznaczną poprawą w porównaniu z TCS ( P = 0,065).
Po 4 tygodniach 68% pacjentów w grupie 4 mg i 62% pacjentów w grupie 2 mg osiągnęło znak EASI-50, w porównaniu z 16% pacjentów leczonych samym TCS ( P <.001).
Zdarzenia niepożądane związane z leczeniem wyniosły 71% wśród pacjentów leczonych 4 mg baricitinibem, u 46% wśród pacjentów leczonych 2 mg leku badanego i 49% u osób leczonych samym TCS. Najczęstszymi niekorzystnymi zdarzeniami niepożądanymi w leczeniu grupą 4-barową baricitinibu były zakażenia górnych dróg oddechowych, zapalenie nosogardzieli, bóle głowy i wzrost parametrów laboratoryjnych, takich jak fosfokinazy kreatyny.
Wyniki badania sugerują, że baricitinib może mieć możliwość leczenia doustnego u pacjentów cierpiących na atopowe zapalenie skóry, którzy nie są w stanie osiągnąć odpowiedniej poprawy po leczeniu TCS.
Baricytinib jest inhibitorem JAK i w lutym 2017 r. otrzymał zgodę na leczenie reumatoidalnego zapalenia stawów w Unii Europejskiej. W kwietniu 2017 r. lek został zatwierdzony przez FDA i zażądała dodatkowych danych w celu określenia odpowiednich dawek i kwestie bezpieczeństwa terapeutycznego. Obecnie lek ten jest badany w chorobach autoimmunologicznych i zapalnych.
Źródło:
healio/AK
healio/AK
Kategorie:
Atopowe zapalenie skóry




