Smoke and mirrors, czyli wyzwania i pułapki oceny leczenia immunomodulującego w SM

Stwardnienie rozsiane można leczyć objawowo. W ostatnich latach pojawiło się wiele leków powstrzymujących rozwój choroby, w tym doskonale znane interferony b (IFN-b). – Poziom bezpieczeństwa i profil działań niepożądanych tych leków zostały ocenione w długotrwałym zastosowaniu. Dzięki IFN-b pacjenci mogą przez lata dobrze funkcjonować w życiu zawodowym i rodzinnym – mówi prof. dr hab. n. med. Monika Adamczyk-Sowa. Leczenie SM nadal jednak stanowi wyzwanie, a chorzy oczekują coraz lepszych, bardziej skutecznych terapii.
Stwardnienie rozsiane (sclerosis multiplex – SM) jest nieuleczalną – dotychczas – chorobą autoimmunologiczną, którą jednak można leczyć objawowo, łagodząc dolegliwości oraz hamując jej postęp. W tym celu wykorzystuje się leki modyfikujące przebieg choroby (disease modifying therapy – DMT). W leczeniu przewlekłym stosowane są leki immunomodulujące, które zmniejszają częstość rzutów i opóźniają progresję SM, takie jak IFN-b, octan glatirameru, natalizumab, mitoksantron czy fingolimod.
– W SM istnieje przewaga procesów zapalnych nad procesami przeciwzapalnymi, które normalnie w homeostazie zachowują balans. W chorobach autoimmunologicznych, również w SM, mamy przewagę impulsacji Th1 nad Th2, natomiast immunomodulacja powoduje powrót równowagi pomiędzy systemem prozapalnym a systemem przeciwzapalnym – wyjaśnia prof. Monika Adamczyk-Sowa z Katedry i Kliniki Neurologii w Zabrzu Śląskiego Uniwersytetu Medycznego w Katowicach.
Mechanizmy działania DMT
Obecnie w leczeniu immunomodulującym najczęściej spotykanego rodzaju SM, a więc postaci rzutowo-remisyjnej, stosowane są przede wszystkim interferony oraz octan glatirameru.
– Przez wiele lat nie do końca było wiadomo, czy te leki działają na układ immunologiczny, w jaki sposób i czy mechanizm ich działania uderza wprost w element patofizjologiczny SM – mówi prof. Monika Adamczyk-Sowa.
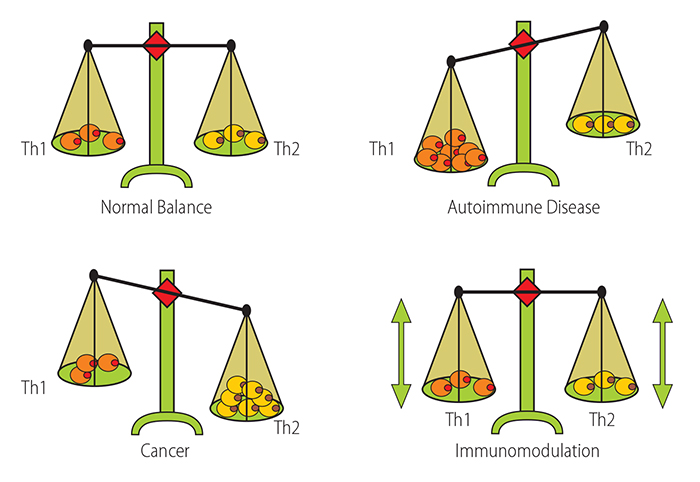
– Okazało się jednak, że np. IFN-b czy octan glatirameru biorą udział w aktywacji wielu genów, które modulują równowagę Th1 i Th2. Z punktu widzenia patogenezy i mechanizmu działania wpływają na przywrócenie równowagi, która jest potrzebna, by zahamować procesy toczące się w SM. Pozostałe leki immunomodulujące działają natomiast na komórki odpowiedzialne za układ immunologiczny, czyli limfocyty, zarówno T, jak i B, powodując albo wyłączenie ich działania, albo ich zniszczenie – dodaje.
– Interferon b powoduje wzrost produkcji cytokin przeciwzapalnych, a hamuje produkcję cytokin działających prozapalnie. I wreszcie – hamuje migrację komórek prozapalnych przez barierę krew–mózg. Działa w układzie obwodowym i ośrodkowym, wpływając zarówno na komórki T poprzez zmniejszenie ich aktywacji, jak i B już w ośrodkowym układzie nerwowym, hamując czy zmniejszając ich proliferację. Działa zatem również na komórki immunokompetentne, wpływając na limfocyty T i B – podsumowuje prof. Monika Adamczyk- Sowa.
Skuteczność leków immunomodulujących w SM
W czasopiśmie „Lancet” (Giancarlo Comi, Marta Radaelli, Per Soelberg Sorensen, Evolving conceptsin the treatment of relapsing multiple sclerosis. Lancet 2017; 389: 1347-1356: https://pubmed.ncbi.nlm. nih.gov/27889192/) opublikowano dane dotyczące skuteczności leków immunomodulujących w SM.
– Widać efekty działania leków od samego początku, kiedy rozpoczęła się era leczenia SM. Mamy do czynienia z wpływem na roczny wskaźnik rzutów, na progresję choroby oraz na aktywność rezonansową. Co widzimy, spoglądając na te dane? O ile roczny wskaźnik rzutu w przypadku leków, które były zarejestrowane jako pierwsze, wynosi nieco ponad 30 proc., to niezwykle istotny jest wpływ na aktywność rezonansową. Dla IFN-b-1b aktywność rezonansowa wynosi aż 83 proc., czyli jest to właściwie taka skuteczność, jaką ma natalizumab, uważany za jeden z najskuteczniejszych leków w terapii immunomodulującej w SM. Widzimy, że dane można interpretować w różny sposób i odkrywać te interpretacje zupełnie na nowo – mówi prof. Monika Adamczyk-Sowa.
Zmienia się populacja pacjentów z SM
Skuteczności poszczególnych leków na SM nie można jednak bezpośrednio porównywać. Dlaczego? Znaczenie ma zarówno roczny wskaźnik rzutów (annualized relapse rate – ARR), jak i kryteria rozpoznania SM.
– Pacjenci z SM, którzy w 1988 r. zostali włączeni do terapii pierwszym ze skutecznych leków, czyli IFN-b-1b, mieli ARR prawie 1,3, czyli aktywność rzutowa w ciągu roku była wysoka. W późniejszych latach ARR już nigdy nie był tak wysoki i w ostatnim zestawieniu, w badaniu z 2006 r., wynosił zaledwie 0,4. Wpływ leku na pacjenta, u którego roczna aktywność rzutowa jest większa, musi być zdecydowanie silniejszy niż na pacjenta z SM o niskiej aktywności rzutowej. Nie możemy zatem mówić o tej samej populacji pacjentów w przypadku leków badanych na samym początku i na przestrzeni lat – zastrzega prof. Monika Adamczyk-Sowa.
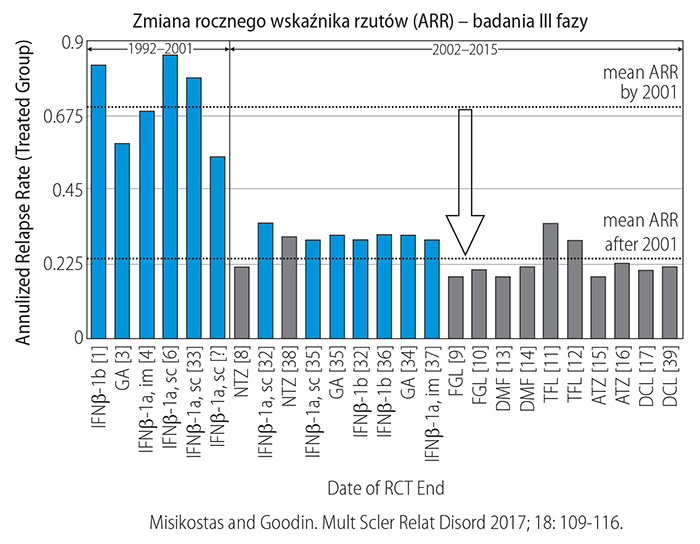
Zmiana rocznego wskaźnika rzutów – badania III fazy
– Na wykresie widzimy, że ARR w pierwszych badaniach dotyczących SM, w latach 1992–2001, był zdecydowanie wysoki. Później, w latach 2002–2015, ARR były już dużo niższe – zauważa prof. Monika Adamczyk-Sowa.
Populacja pacjentów z SM w poszczególnych latach różniła się nie tylko aktywnością rzutową, lecz także kryteriami rozpoznania.
– Pamiętajmy, że u pierwszych pacjentów SM rozpoznawano na podstawie kryteriów diagnostycznych Posera, później natomiast zaczęto stosować kryteria McDonalda, które z rewizji na rewizję są coraz bardziej liberalne. Chorzy, u których początkowo rozpoznawano zespół klinicznie izolowany (clinically isolated syndrome – CIS), na podstawie późniejszych kryteriów mogli zostać zakwalifikowani jako przypadki pełnoobjawowe i mieć zdefiniowane SM, co oczywiście też ma ogromne znaczenie dla porównywania skuteczności badanych leków – wyjaśnia prof. Monika Adamczyk-Sowa.
– Z metaanaliz jasno wynika, że każdy zastosowany lek immunomodulujący wykazuje zdecydowanie wyższą skuteczność w hamowaniu progresji niepełnosprawności niż placebo. Na dobrą sprawę nieważne, który lek zastosujemy. Podobnie jest, jeżeli chodzi o ARR – każdy z zastosowanych leków jest skuteczniejszy w porównaniu z placebo – stwierdza prof. Monika Adamczyk-Sowa.
Jaki lek dla jakiego pacjenta?
W SM stosowane są dwa główne modele leczenia – indukcyjny i eskalacyjny. Do tych terapii przyporządkowane są dwie rożne grupy preparatów.
– Musimy pamiętać, że w przypadku terapii rekonstytucyjnych typowo są to preparaty przeznaczone dla pacjentów z niekorzystną prognozą, czyli z bardzo dużą aktywnością choroby. Czy u każdego pacjenta powinniśmy stosować terapię rekonstytucyjną? Oczywiście nie. Zdecydowana większość naszych pacjentów – w polskim programie lekowym aż 90 proc. – to chorzy z umiarkowaną aktywnością SM i pacjenci, którzy stosują leki pierwszego wyboru. W krajach Europy Zachodniej ten odsetek wynosi nie 90 proc., lecz 70 proc. Jest to związane ze zbyt restrykcyjnymi warunkami terapii drugiej linii, niemniej na pewno główna populacja chorych z SM, których leczymy, to pacjenci z umiarkowaną aktywnością choroby. Dlatego nie powinniśmy im od razu przepisywać leków wysoce aktywnych, gdyż większość wymaga terapii eskalacyjnej. Dopiero później, jeśli jest taka potrzeba, możemy sięgać po leki bardziej aktywne. Między terapią eskalacyjną a terapią rekonstytucyjną są bowiem różnice, a skutki leczenia czy potencjalne działania niepożądane są nieodwracalne. W terapiach rekonstytucyjnych nie jesteśmy w stanie zmienić leczenia, bo jest ono prowadzone w odpowiednich interwałach czasowych – mówi prof. Monika Adamczyk-Sowa.
Proponowany aktualny algorytm leczenia SM
– Rekomendacje europejskie ECTRIMS/ EAN jasno mówią, że u pacjentów z aktywną rzutową postacią SM należy wybrać lek spośród wszystkich, które mamy na mapie leczenia tej choroby, od umiarkowanych – IFN-b poprzez wszystkie leki pierwszej linii aż do leków najbardziej aktywnych. W kontekście smoke and mirrors powinniśmy pamiętać, że mamy również preparaty, które są skuteczne w postaci wtórnie postępującej aktywnej, właśnie IFN-b-1a czy -1b – mówi prof. Monika Adamczyk-Sowa.
Planowanie rodziny przez pacjentki z SM
Do niedawna uważano, że największa aktywność rzutowa występuje w okresie dojrzewania i w okresie połogu. Wykres znany wszystkim lekarzom zajmującym się SM pokazuje, że w okresie połogu dochodzi do znacznego wzrostu aktywności rzutowej.
– Już w ubiegłym roku ten pogląd został nieco zmodyfikowany. Langer-Gould zaprezentowała nowy wykres, na którym widać, że aktywność rzutowa w okresie połogu nie jest tak duża. Wiąże się to z większą dostępnością leczenia, zdecydowanie mniejszym ARR przed włączeniem do terapii, wreszcie z aktywnym planowaniem rodziny – mówi prof. Monika Adamczyk-Sowa.
W 2019 r. nastąpiła zmiana zapisu w charakterystyce produktu leczniczego (ChPL) dla klasy interferonów dotycząca stosowania w okresie ciąży i karmienia piersią (update EMA, wrzesień 2019 r.).
– W ubiegłym roku IFN-b uzyskały nowy wpis w ChPL – można je stosować w ciąży i podczas karmienia piersią. Zmian dokonano na podstawie pozytywnych wyników publikacji bazujących na rejestrach ciąż. W ten sposób można aktywnie planować ciążę aż do momentu poczęcia. Również zgodnie z polskimi rekomendacjami pacjentka powinna najpierw ustabilizować chorobę i stosować leczenie IFN-b bądź octanem glatirameru do okresu zajścia w ciążę, bo wtedy należy ten lek odstawić – komentuje prof. Monika Adamczyk-Sowa.
W związku z nowymi zapisami w ChPL nieco zmieniły się zasady leczenia i myślenia o planowaniu rodziny w przypadku kobiet chorych na SM.
– Wiemy, że u kobiet w wieku rozrodczym możemy bezpiecznie stosować IFN-b i octan glatirameru, a jeżeli dochodzi do ekspozycji na te leki w pierwszym trymestrze ciąży, nie ma konieczności dodatkowego monitorowania płodu ani matki – wyjaśnia prof. Monika Adamczyk-Sowa.
Bezpieczeństwo DMT
Leki immunomodulujące są uznawane za bezpieczne.
– Wszyscy doskonale wiemy, że im bardziej bezpieczny jest lek, tym jego skuteczność jest mniejsza. Czy tak jest w przypadku wszystkich preparatów? Jeżeli chodzi o dane dotyczące bezpieczeństwa, to faktycznie IFN-b, które funkcjonują w codziennej praktyce klinicznej prawie 25 lat, nie zaskoczyły nas – mówi prof. Monika Adamczyk-Sowa.
– W stosunku do innych preparatów IFN-b charakteryzują się niewielkimi działaniami niepożądanymi, z którymi doskonale sobie radzimy i które jesteśmy w stanie przewidzieć, takimi jak gorączka, objawy grypopodobne, ból głowy, reakcje w miejscu wkłucia, wzrost aktywności transaminaz, złe samopoczucie, bóle mięśni. W tym roku opublikowano zbiorcze zestawienie działań niepożądanych wszystkich leków immunomodulujących. Te z nich, które zostały zarejestrowane jako pierwsze skuteczne leki, wypadają na tym tle naprawdę korzystnie, a ich bezpieczeństwo jest dobrze poznane – dodaje.
Stwardnienie rozsiane a COVID-19
Czy pacjenci z SM są bardziej narażeni na zakażenie koronawirusem SARS-CoV-2 i ciężki przebieg COVID-19? Okazuje się, że nie.
– Na początku epidemii pojawiło się dużo wątpliwości na temat bezpieczeństwa naszych pacjentów i przebiegu COVID-19, zarówno w aspekcie samej choroby, jak i leków, które wpływają przecież na odporność. Okazuje się, na podstawie już dość dużej liczby publikacji, że pacjenci z SM nie chorują ani częściej, ani ciężej niż pacjenci w populacji ogólnej. I dotyczy to zarówno osób, które stosują leczenie immunomodulujące, jak i bez takiego leczenia – mówi prof. Monika Adamczyk-Sowa.
Interferon b-1b – pierwszy skuteczny, najlepiej poznany lek dla chorych na SM
Zarówno chorzy na SM, jak i ich lekarze czekają na nowe terapie. Jednak te, które już są stosowane, bez wątpienia są skuteczne.
– Przez ponad 20 lat, odkąd w terapii SM stosowane są IFN-b, stan pacjentów znacząco się poprawił. Dzisiejszy pacjent z SM to osoba ze zdecydowanie mniejszą niesprawnością, która utrzymuje sprawność przez długie lata. Pod opieką mamy pacjentów z długoletnim dobrym, stabilnym stanem neurologicznym. Od kiedy pojawił się pierwszy skuteczny lek, terapie dla osób z SM, które okazały się skuteczne i rozpoczęły erę leczenia tej choroby, są stale stosowane, bo pomagają chorym. Są też bardzo bezpieczne i nie zaskoczyły nas w codziennej praktyce działaniami niepożądanymi, więc na pewno będziemy po nie sięgać w leczeniu naszych pacjentów – podsumowuje prof. Monika Adamczyk-Sowa.
Tekst opublikowano w „Kurierze Medycznym” 1/2021. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.

– W SM istnieje przewaga procesów zapalnych nad procesami przeciwzapalnymi, które normalnie w homeostazie zachowują balans. W chorobach autoimmunologicznych, również w SM, mamy przewagę impulsacji Th1 nad Th2, natomiast immunomodulacja powoduje powrót równowagi pomiędzy systemem prozapalnym a systemem przeciwzapalnym – wyjaśnia prof. Monika Adamczyk-Sowa z Katedry i Kliniki Neurologii w Zabrzu Śląskiego Uniwersytetu Medycznego w Katowicach.
Mechanizmy działania DMT
Obecnie w leczeniu immunomodulującym najczęściej spotykanego rodzaju SM, a więc postaci rzutowo-remisyjnej, stosowane są przede wszystkim interferony oraz octan glatirameru.
– Przez wiele lat nie do końca było wiadomo, czy te leki działają na układ immunologiczny, w jaki sposób i czy mechanizm ich działania uderza wprost w element patofizjologiczny SM – mówi prof. Monika Adamczyk-Sowa.

– Okazało się jednak, że np. IFN-b czy octan glatirameru biorą udział w aktywacji wielu genów, które modulują równowagę Th1 i Th2. Z punktu widzenia patogenezy i mechanizmu działania wpływają na przywrócenie równowagi, która jest potrzebna, by zahamować procesy toczące się w SM. Pozostałe leki immunomodulujące działają natomiast na komórki odpowiedzialne za układ immunologiczny, czyli limfocyty, zarówno T, jak i B, powodując albo wyłączenie ich działania, albo ich zniszczenie – dodaje.
– Interferon b powoduje wzrost produkcji cytokin przeciwzapalnych, a hamuje produkcję cytokin działających prozapalnie. I wreszcie – hamuje migrację komórek prozapalnych przez barierę krew–mózg. Działa w układzie obwodowym i ośrodkowym, wpływając zarówno na komórki T poprzez zmniejszenie ich aktywacji, jak i B już w ośrodkowym układzie nerwowym, hamując czy zmniejszając ich proliferację. Działa zatem również na komórki immunokompetentne, wpływając na limfocyty T i B – podsumowuje prof. Monika Adamczyk- Sowa.
Skuteczność leków immunomodulujących w SM
W czasopiśmie „Lancet” (Giancarlo Comi, Marta Radaelli, Per Soelberg Sorensen, Evolving conceptsin the treatment of relapsing multiple sclerosis. Lancet 2017; 389: 1347-1356: https://pubmed.ncbi.nlm. nih.gov/27889192/) opublikowano dane dotyczące skuteczności leków immunomodulujących w SM.
– Widać efekty działania leków od samego początku, kiedy rozpoczęła się era leczenia SM. Mamy do czynienia z wpływem na roczny wskaźnik rzutów, na progresję choroby oraz na aktywność rezonansową. Co widzimy, spoglądając na te dane? O ile roczny wskaźnik rzutu w przypadku leków, które były zarejestrowane jako pierwsze, wynosi nieco ponad 30 proc., to niezwykle istotny jest wpływ na aktywność rezonansową. Dla IFN-b-1b aktywność rezonansowa wynosi aż 83 proc., czyli jest to właściwie taka skuteczność, jaką ma natalizumab, uważany za jeden z najskuteczniejszych leków w terapii immunomodulującej w SM. Widzimy, że dane można interpretować w różny sposób i odkrywać te interpretacje zupełnie na nowo – mówi prof. Monika Adamczyk-Sowa.
Zmienia się populacja pacjentów z SM
Skuteczności poszczególnych leków na SM nie można jednak bezpośrednio porównywać. Dlaczego? Znaczenie ma zarówno roczny wskaźnik rzutów (annualized relapse rate – ARR), jak i kryteria rozpoznania SM.
– Pacjenci z SM, którzy w 1988 r. zostali włączeni do terapii pierwszym ze skutecznych leków, czyli IFN-b-1b, mieli ARR prawie 1,3, czyli aktywność rzutowa w ciągu roku była wysoka. W późniejszych latach ARR już nigdy nie był tak wysoki i w ostatnim zestawieniu, w badaniu z 2006 r., wynosił zaledwie 0,4. Wpływ leku na pacjenta, u którego roczna aktywność rzutowa jest większa, musi być zdecydowanie silniejszy niż na pacjenta z SM o niskiej aktywności rzutowej. Nie możemy zatem mówić o tej samej populacji pacjentów w przypadku leków badanych na samym początku i na przestrzeni lat – zastrzega prof. Monika Adamczyk-Sowa.
Zmiana rocznego wskaźnika rzutów – badania III fazy
– Na wykresie widzimy, że ARR w pierwszych badaniach dotyczących SM, w latach 1992–2001, był zdecydowanie wysoki. Później, w latach 2002–2015, ARR były już dużo niższe – zauważa prof. Monika Adamczyk-Sowa.
Populacja pacjentów z SM w poszczególnych latach różniła się nie tylko aktywnością rzutową, lecz także kryteriami rozpoznania.
– Pamiętajmy, że u pierwszych pacjentów SM rozpoznawano na podstawie kryteriów diagnostycznych Posera, później natomiast zaczęto stosować kryteria McDonalda, które z rewizji na rewizję są coraz bardziej liberalne. Chorzy, u których początkowo rozpoznawano zespół klinicznie izolowany (clinically isolated syndrome – CIS), na podstawie późniejszych kryteriów mogli zostać zakwalifikowani jako przypadki pełnoobjawowe i mieć zdefiniowane SM, co oczywiście też ma ogromne znaczenie dla porównywania skuteczności badanych leków – wyjaśnia prof. Monika Adamczyk-Sowa.
– Z metaanaliz jasno wynika, że każdy zastosowany lek immunomodulujący wykazuje zdecydowanie wyższą skuteczność w hamowaniu progresji niepełnosprawności niż placebo. Na dobrą sprawę nieważne, który lek zastosujemy. Podobnie jest, jeżeli chodzi o ARR – każdy z zastosowanych leków jest skuteczniejszy w porównaniu z placebo – stwierdza prof. Monika Adamczyk-Sowa.

Jaki lek dla jakiego pacjenta?
W SM stosowane są dwa główne modele leczenia – indukcyjny i eskalacyjny. Do tych terapii przyporządkowane są dwie rożne grupy preparatów.
– Musimy pamiętać, że w przypadku terapii rekonstytucyjnych typowo są to preparaty przeznaczone dla pacjentów z niekorzystną prognozą, czyli z bardzo dużą aktywnością choroby. Czy u każdego pacjenta powinniśmy stosować terapię rekonstytucyjną? Oczywiście nie. Zdecydowana większość naszych pacjentów – w polskim programie lekowym aż 90 proc. – to chorzy z umiarkowaną aktywnością SM i pacjenci, którzy stosują leki pierwszego wyboru. W krajach Europy Zachodniej ten odsetek wynosi nie 90 proc., lecz 70 proc. Jest to związane ze zbyt restrykcyjnymi warunkami terapii drugiej linii, niemniej na pewno główna populacja chorych z SM, których leczymy, to pacjenci z umiarkowaną aktywnością choroby. Dlatego nie powinniśmy im od razu przepisywać leków wysoce aktywnych, gdyż większość wymaga terapii eskalacyjnej. Dopiero później, jeśli jest taka potrzeba, możemy sięgać po leki bardziej aktywne. Między terapią eskalacyjną a terapią rekonstytucyjną są bowiem różnice, a skutki leczenia czy potencjalne działania niepożądane są nieodwracalne. W terapiach rekonstytucyjnych nie jesteśmy w stanie zmienić leczenia, bo jest ono prowadzone w odpowiednich interwałach czasowych – mówi prof. Monika Adamczyk-Sowa.
Proponowany aktualny algorytm leczenia SM
– Rekomendacje europejskie ECTRIMS/ EAN jasno mówią, że u pacjentów z aktywną rzutową postacią SM należy wybrać lek spośród wszystkich, które mamy na mapie leczenia tej choroby, od umiarkowanych – IFN-b poprzez wszystkie leki pierwszej linii aż do leków najbardziej aktywnych. W kontekście smoke and mirrors powinniśmy pamiętać, że mamy również preparaty, które są skuteczne w postaci wtórnie postępującej aktywnej, właśnie IFN-b-1a czy -1b – mówi prof. Monika Adamczyk-Sowa.
Planowanie rodziny przez pacjentki z SM
Do niedawna uważano, że największa aktywność rzutowa występuje w okresie dojrzewania i w okresie połogu. Wykres znany wszystkim lekarzom zajmującym się SM pokazuje, że w okresie połogu dochodzi do znacznego wzrostu aktywności rzutowej.
– Już w ubiegłym roku ten pogląd został nieco zmodyfikowany. Langer-Gould zaprezentowała nowy wykres, na którym widać, że aktywność rzutowa w okresie połogu nie jest tak duża. Wiąże się to z większą dostępnością leczenia, zdecydowanie mniejszym ARR przed włączeniem do terapii, wreszcie z aktywnym planowaniem rodziny – mówi prof. Monika Adamczyk-Sowa.
W 2019 r. nastąpiła zmiana zapisu w charakterystyce produktu leczniczego (ChPL) dla klasy interferonów dotycząca stosowania w okresie ciąży i karmienia piersią (update EMA, wrzesień 2019 r.).
– W ubiegłym roku IFN-b uzyskały nowy wpis w ChPL – można je stosować w ciąży i podczas karmienia piersią. Zmian dokonano na podstawie pozytywnych wyników publikacji bazujących na rejestrach ciąż. W ten sposób można aktywnie planować ciążę aż do momentu poczęcia. Również zgodnie z polskimi rekomendacjami pacjentka powinna najpierw ustabilizować chorobę i stosować leczenie IFN-b bądź octanem glatirameru do okresu zajścia w ciążę, bo wtedy należy ten lek odstawić – komentuje prof. Monika Adamczyk-Sowa.
W związku z nowymi zapisami w ChPL nieco zmieniły się zasady leczenia i myślenia o planowaniu rodziny w przypadku kobiet chorych na SM.
– Wiemy, że u kobiet w wieku rozrodczym możemy bezpiecznie stosować IFN-b i octan glatirameru, a jeżeli dochodzi do ekspozycji na te leki w pierwszym trymestrze ciąży, nie ma konieczności dodatkowego monitorowania płodu ani matki – wyjaśnia prof. Monika Adamczyk-Sowa.
Bezpieczeństwo DMT
Leki immunomodulujące są uznawane za bezpieczne.
– Wszyscy doskonale wiemy, że im bardziej bezpieczny jest lek, tym jego skuteczność jest mniejsza. Czy tak jest w przypadku wszystkich preparatów? Jeżeli chodzi o dane dotyczące bezpieczeństwa, to faktycznie IFN-b, które funkcjonują w codziennej praktyce klinicznej prawie 25 lat, nie zaskoczyły nas – mówi prof. Monika Adamczyk-Sowa.
– W stosunku do innych preparatów IFN-b charakteryzują się niewielkimi działaniami niepożądanymi, z którymi doskonale sobie radzimy i które jesteśmy w stanie przewidzieć, takimi jak gorączka, objawy grypopodobne, ból głowy, reakcje w miejscu wkłucia, wzrost aktywności transaminaz, złe samopoczucie, bóle mięśni. W tym roku opublikowano zbiorcze zestawienie działań niepożądanych wszystkich leków immunomodulujących. Te z nich, które zostały zarejestrowane jako pierwsze skuteczne leki, wypadają na tym tle naprawdę korzystnie, a ich bezpieczeństwo jest dobrze poznane – dodaje.
Stwardnienie rozsiane a COVID-19
Czy pacjenci z SM są bardziej narażeni na zakażenie koronawirusem SARS-CoV-2 i ciężki przebieg COVID-19? Okazuje się, że nie.
– Na początku epidemii pojawiło się dużo wątpliwości na temat bezpieczeństwa naszych pacjentów i przebiegu COVID-19, zarówno w aspekcie samej choroby, jak i leków, które wpływają przecież na odporność. Okazuje się, na podstawie już dość dużej liczby publikacji, że pacjenci z SM nie chorują ani częściej, ani ciężej niż pacjenci w populacji ogólnej. I dotyczy to zarówno osób, które stosują leczenie immunomodulujące, jak i bez takiego leczenia – mówi prof. Monika Adamczyk-Sowa.
Interferon b-1b – pierwszy skuteczny, najlepiej poznany lek dla chorych na SM
Zarówno chorzy na SM, jak i ich lekarze czekają na nowe terapie. Jednak te, które już są stosowane, bez wątpienia są skuteczne.
– Przez ponad 20 lat, odkąd w terapii SM stosowane są IFN-b, stan pacjentów znacząco się poprawił. Dzisiejszy pacjent z SM to osoba ze zdecydowanie mniejszą niesprawnością, która utrzymuje sprawność przez długie lata. Pod opieką mamy pacjentów z długoletnim dobrym, stabilnym stanem neurologicznym. Od kiedy pojawił się pierwszy skuteczny lek, terapie dla osób z SM, które okazały się skuteczne i rozpoczęły erę leczenia tej choroby, są stale stosowane, bo pomagają chorym. Są też bardzo bezpieczne i nie zaskoczyły nas w codziennej praktyce działaniami niepożądanymi, więc na pewno będziemy po nie sięgać w leczeniu naszych pacjentów – podsumowuje prof. Monika Adamczyk-Sowa.
Tekst opublikowano w „Kurierze Medycznym” 1/2021. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.