Algorytm różnicowania przyczyn niedokrwistości
Niedokrwistość to stan kliniczny objawiający się zmniejszeniem stężenia hemoglobiny i hematokrytu poniżej wartości przyjętych za normę dla danej płci i wieku. Warunkiem skutecznego leczenia niedokrwistości jest poznanie jej przyczyny. W diagnostyce należy brać pod uwagę całość obrazu klinicznego, a nie tylko wynik pojedynczego testu.
Autorki: Iwona Hus, Agnieszka Mastalerz-Migas
Definicja niedokrwistości
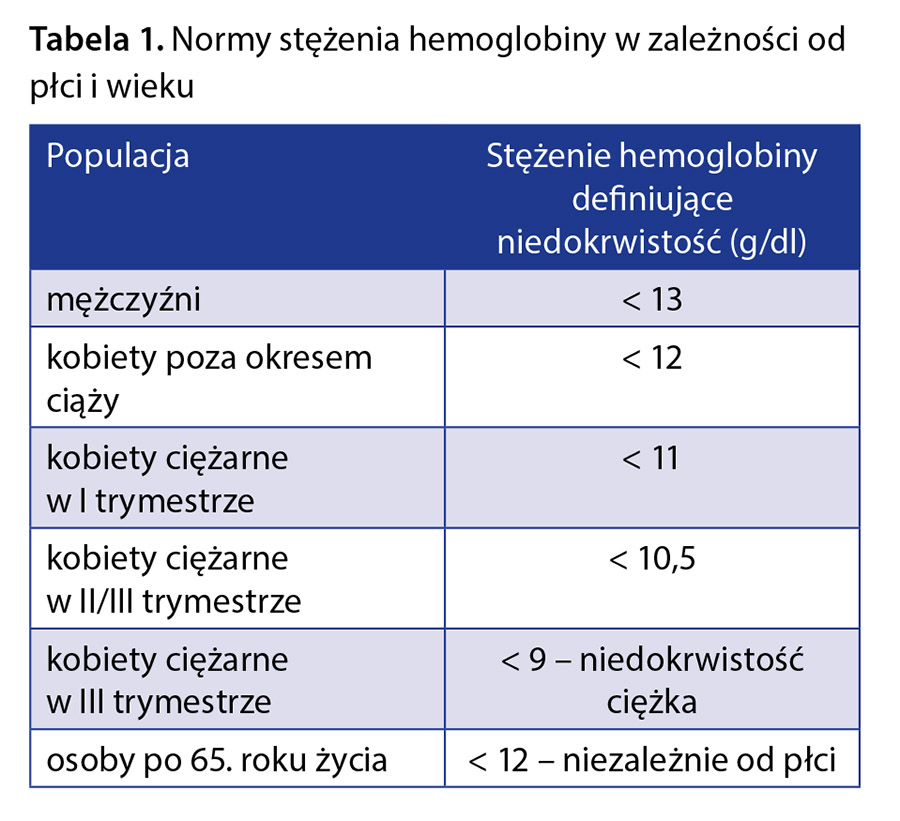
Niedokrwistość to stan kliniczny objawiający się zmniejszeniem stężenia hemoglobiny (Hgb) i hematokrytu (Ht) poniżej wartości przyjętych za normę dla danej płci i wieku. Liczba krwinek czerwonych może być zmniejszona, zwiększona lub prawidłowa w zależności od przyczyny i stopnia nasilenia niedokrwistości. Wartości stężenia Hgb definiujące niedokrwistość w zależności od płci i wieku przedstawiono w tabeli 1, a stopnie niedokrwistości według Światowej Organizacji Zdrowia (World Health Organization – WHO) w tabeli 2.

Przyczyny niedokrwistości
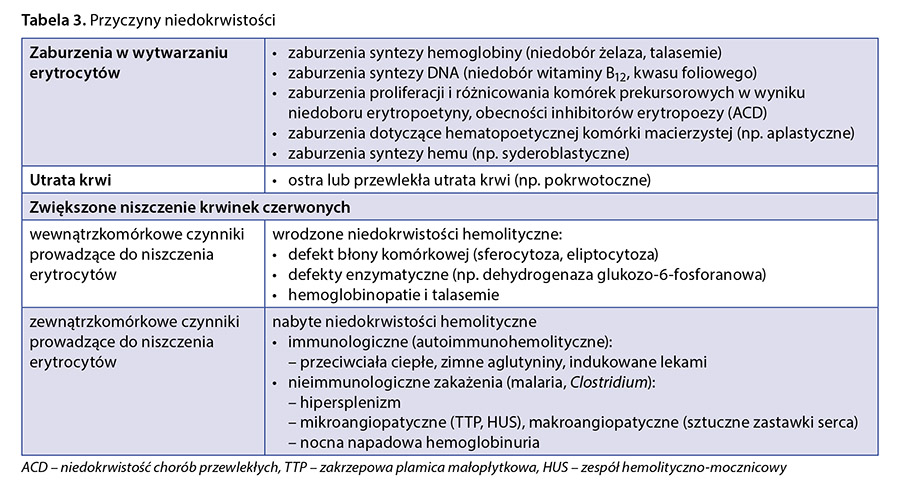
Niedokrwistość nie jest samodzielną jednostką chorobową, ale należy ją traktować jako następstwo stanu chorobowego toczącego się w organizmie. Warunkiem skutecznego leczenia niedokrwistości jest poznanie jej przyczyny. Przyczyny niedokrwistości obejmują cztery główne grupy przedstawione w tabeli 3.
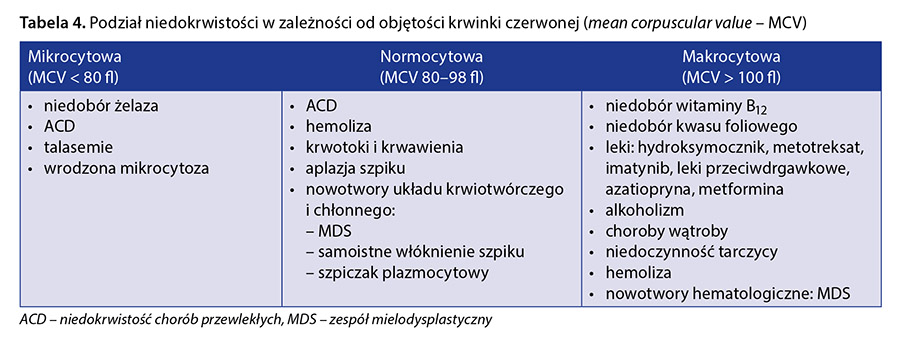
Inny podział, często wykorzystywany w diagnostyce niedokrwistości, jest oparty na objętości krwinki czerwonej (mean corpuscular value – MCV) (tab. 4).
Najczęstsze rodzaje niedokrwistości to niedokrwistość z niedoboru żelaza (iron deficiency anemia – IDA) oraz niedokrwistość chorób przewlekłych (anemia of chronic diseases – ACD).
Diagnostyka niedokrwistości
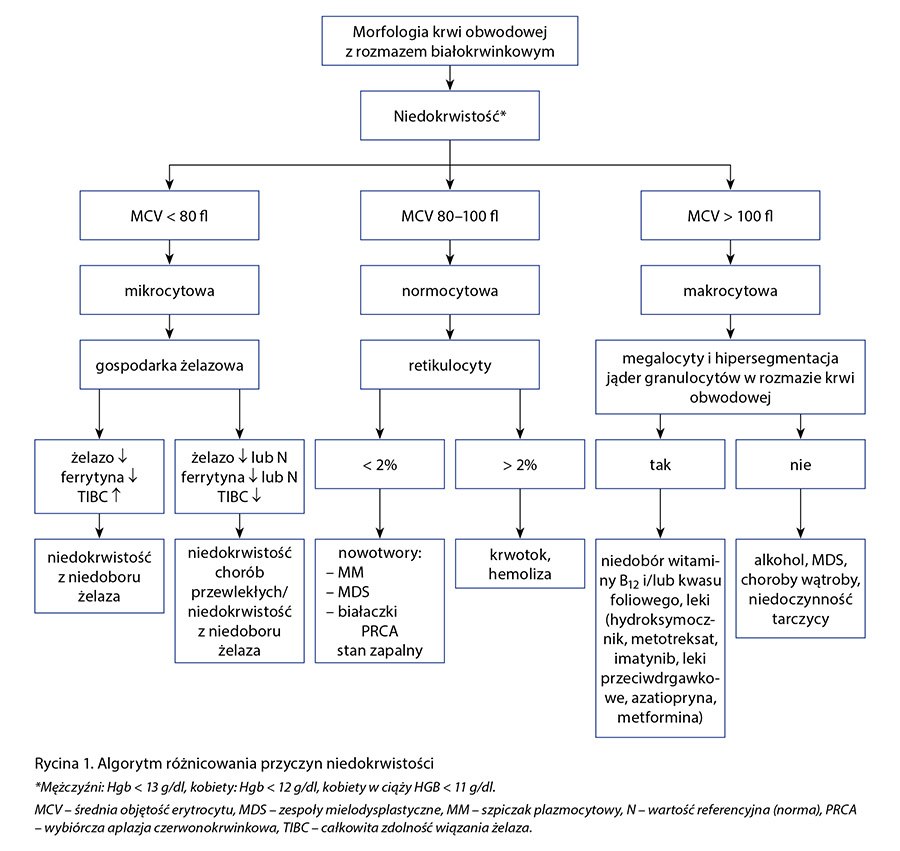
W praktyce często wykorzystywany jest algorytm diagnostyki niedokrwistości zależny od wartości MCV, przedstawiony na rycinie 1.
Niedokrwistości niedoborowe
Niedokrwistość z niedoboru żelaza
Obraz kliniczny niedokrwistości z niedoboru żelaza oprócz objawów typowych dla każdej niedokrwistości obejmuje również symptomy tkankowego niedoboru żelaza, takie jak: zaburzenia troficzne skóry, suchość skóry i włosów, łamliwość włosów i paznokci, deformacje płytki paznokciowej, zajady w kącikach ust, atroficzne bolesne zapalenie błony śluzowej jamy ustnej, bóle głowy, zaburzenia koncentracji, rozdrażnienie lub senność, „niespokojne nogi”, spaczone łaknienie (pica) – „zachcianki” na rzeczy niejadalne, np. ziemię, błoto, lód.
Wyróżnia się trzy główne przyczyny niedokrwistości z niedoboru żelaza, które należy uwzględnić w diagnostyce różnicowej:
• przewlekła utrata krwi:
» obfite krwawienia miesięczne, krwawienia z dróg rodnych,
» krwawienia z przewodu pokarmowego – choroba wrzodowa żołądka, zakażenie Helicobacter pylori, angiodysplazja, choroby zapalne jelit (choroba Leśniowskiego-Crohna), zmiany łagodne lub nowotworowe (rak żołądka, jelita grubego), leki (NLPZ),
» krwawienia z dróg moczowych,
» wewnątrznaczyniowa hemoliza (utrata żelaza z moczem);
• brak wystarczającej ilości żelaza w diecie:
» zwiększone zapotrzebowanie (kobiety w ciąży, dzieci i młodzież),
» niedobór w diecie (dieta wegetariańska, osoby starsze);
• zaburzenia wchłaniania żelaza w przewodzie pokarmowym:
» celiakia (5–6% chorych z IDA, najczęstsza pozajelitowa manifestacja celiakii),
» autoimmunologiczne zapalenie żołądka,
» choroby zapalne jelit (np. choroba Leśniowskiego-Crohna),
» zakażenie Helicobacter pylori (konkurencja o żelazo, nadżerki), Giardia lamblia,
» stan po gastrektomii, po operacji bariatrycznej (IDA u 45% chorych),
» dieta bogata w substancje upośledzające wchłanianie żelaza (fosforany, szczawiany, fityniany, garbniki, polifenole, suplementy cynku i manganu),
» leki (np. inhibitory pomby protonowej, leki zobojętniające, blokery H2).
Niedokrwistość z niedoboru żelaza najczęściej występuje u kobiet w wieku menoplauzalnym, jej przyczyną są nieprawidłowe krwawienia miesięczne. Często obserwowana jest również u kobiet w ciąży. Zazwyczaj przyczyną IDA u kobiet w wieku pomenopauzalnym i mężczyzn są choroby przewodu pokarmowego (50–70%), dlatego badanie przewodu pokarmowego stanowi niezbędny element postępowania diagnostycznego.
Diagnostyka przewodu pokarmowego powinna obejmować: gastroskopię, kolonoskopię, diagnostykę jelita cienkiego (endoskopia kapsułkowa, enteroskopia balonowa), badania w kierunku celiakii (przeciwciała przeciw transglutaminazie tkankowej lub endomysium), badania w kierunku zakażenia Helicobacter pylori lub Giardia lamblia, przeciwciała przeciw komórkom okładzinowym żołądka.
Należy również pamiętać o przyczynach urologicznych i wykonaniu badania ogólnego moczu w celu wykluczenia krwinkomoczu.
Diagnostyka laboratoryjna powinna obejmować ocenę morfologii krwi i gospodarki żelazowej. W morfologii krwi typowe dla niedoboru żelaza jest obniżone MCV (czułość 96,7%), ale w 40% przypadków IDA wartość MCV jest prawidłowa. Obserwuje się również podwyższenie wskaźnika RDW (rozpiętość rozkładu erytrocytów). Wartość RDW jest prawidłowa w talasemii, w której podobnie jak w przypadku niedoboru żelaza występuje obniżenie MCV.
Spośród parametrów gospodarki żelazowej najważniejszym wskaźnikiem jest ferrytyna, której stężenie w surowicy odzwierciedla całkowite zapasy żelaza w organizmie. Ferrytyna cechuje się dużą swoistością, ale jest również białkiem ostrej fazy, w związku z czym jej stężenie wzrasta w przebiegu stanów zapalnych, w zakażeniach, chorobach autoimmunologicznych oraz przy uszkodzeniu wątroby. Zwykle w IDA stężenie ferrytyny wynosi < 15 – 10 µg/l. O niedoborze żelaza przy współistniejącym stanie zapalnym świadczy stężenie ferrytyny < 100 µg/l.
Zwiększenie stężenia transferyny lub całkowitej zdolności wiązania żelaza (TIBC) jest parametrem swoistym dla IDA, ale cechuje się małą czułością (zmniejszenie w stanie zapalnym, w starszym wieku, przy niedożywieniu). Wartościowym parametrem niezależnym od stanu zapalnego jest saturacja transferyny (TSAT, %) obliczana według wzoru: (stężenie żelaza/stężenie transferyny) × 1,41. Zwykle u pacjentów z IDA wartość TSAT jest < 16%. U chorych z niewydolnością krążenia lub niewydolnością nerek IDA rozpoznaje się przy saturacji transferyny < 30% i stężeniu ferrytyny < 300 µg/l. Należy unikać rozpoznawania niedoboru żelaza na podstawie oznaczenia stężenia żelaza, uważanego za suboptymalny test diagnostyczny z powodu obniżonego stężenia w stanach zapalnych, fałszywie podwyższonego przy doustnej suplementacji oraz dużej zmienności oznaczeń z dnia na dzień. Stężenie żelaza należy ocenić, jeśli jest potrzeba obliczenia saturacji transferyny.
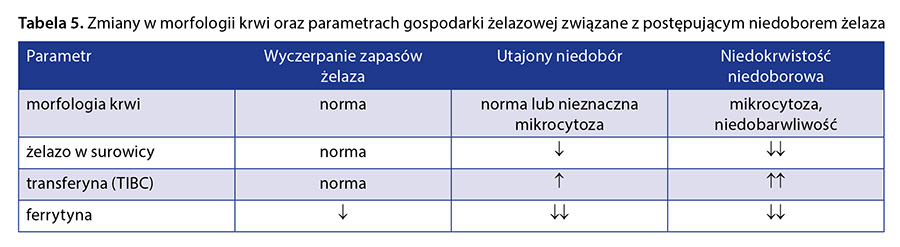
W tabeli 5 przedstawiono zmiany w morfologii krwi oraz parametrach gospodarki żelazowej związane z postępującym niedoborem żelaza, a w tabeli 6 różnicowanie między IDA i ACD.
Niedokrwistość megaloblastyczna
Niedokrwistość megaloblastyczna jest wywołana niedoborem witaminy B12 i/lub kwasu foliowego. Dzienne zapotrzebowanie na witaminę B12 wynosi 1–2 µg, dieta zachodnia zawierająca produkty pochodzenia zwierzęcego jest wystarczająca do pokrycia zapotrzebowania dobowego. Zapasy w organizmie wynoszące 2–3 mg wystarczają na okres 3–5 lat. Dzienne zapotrzebowanie na kwas foliowy wynosi 0,1–0,2 mg. Dieta zachodnia zawiera 0,5–0,7 mg (świeże warzywa). Zapasy kwasu foliowego w organizmie wynoszą 10–15 mg i wystarczają na 2 miesiące.
Do przyczyn niedoboru witaminy B12 należą:
• niedobór w diecie (bardzo rzadko – ścisła dieta wegańska),
• zaburzenia wchłaniania:
» niedokrwistość Addisona-Biermera (przeciwciała przeciw komórkom okładzinowym żołądka – najczęstsza przyczyna ciężkiego niedoboru),
» przewlekłe zanikowe zapalenie żołądka – 20% osób w starszym wieku;
• inne przyczyny: niewydolność trzustki, zespół ślepej pętli, gastrektomia, chirurgiczna resekcja końcowego odcinka ileum.
Niedobór kwasu foliowego może być wynikiem jego niewystarczającej podaży w diecie, alkoholizmu, zaburzeń wchłaniania, zwiększonego zapotrzebowania (niedokrwistość hemolityczna, leczenie metoreksatem).
W przypadku niedoboru zarówno witaminy B12, jak i kwasu foliowego występują objawy ze strony przewodu pokarmowego, takie jak brak apetytu (osłabienie wrażeń smakowych), cechy zapalenia błony śluzowej jamy ustnej, cechy zapalenia języka w postaci pieczenia, wygładzenia języka (język Huntera), skłonność do biegunek lub zaparć i nudności. Objawy neurologiczne (zaburzenia ze strony ośrodkowego układu nerwowego) związane są wyłącznie z niedoborem witaminy B12 i wynikają z demielinizacji neuronów rdzenia kręgowego oraz kory mózgowej. Zmiany utrzymujące się ponad 1/2 roku nie cofają się, dlatego tak istotne jest różnicowanie i właściwe leczenie niedokrwistości megaloblastycznej.
Obraz kliniczny obejmuje: zmiany psychiczne (spowolnienie psychiczne i apatia, trudności w przeprowadzeniu prostych rachunków arytmetycznych, zaburzenia pamięci, drażliwość, depresja, stupor, urojenia, halucynacje, paranoja, tzw. obłęd megaloblastyczny) oraz objawy związane ze zwyrodnieniem powrózkowym rdzenia kręgowego (zaburzenia czucia głębokiego, ataksja, parestezje, uczucie drętwienia, niestabilność chodu).
W rozmazie krwi obwodowej widoczne są wyraźne zmiany morfologii krwinek: zwiększenie MCV, megaloowalocytoza i hiperchromia erytrocytów, anizocytoza i poikilocytoza, hipersegmentacja jąder granulocytów (ponad 5% granulocytów z liczbą segmentów 6 i więcej) oraz obecność patologicznych płytek krwi (megatrombocytów).
Nieprawidłowości w badaniach biochemicznych obejmują hiperbilirubinemię (pośrednia – w wyniku hemolizy) i podwyższone stężenie LDH. Stężenie żelaza w surowicy jest w normie lub podwyższone.
Diagnostyka niedokrwistości megaloblastycznej powinna uwzględniać badania laboratoryjne: oznaczanie stężenia kwasu foliowego i witaminy B12. W razie wątpliwości należy oznaczyć stężenie kwasu metylomalonowego i homocysteiny. Należy również przeprowadzić badanie czynności wydzielniczej żołądka i stanu jego błony śluzowej (gastroskopia z oceną histopatologiczną wycinka błony śluzowej, badanie obecności przeciwciał przeciw komórkom okładzinowym żołądka i czynnikowi wewnętrznemu Castle’a).
Niedokrwistość hemolityczna
W obrazie klinicznym niedokrwistości hemolitycznej oprócz ogólnych objawów niedokrwistości obserwuje się:
• objawy ogólne, takie jak: gorączka, ból mięśni i stawów, objawy żółtaczki,
• splenomegalię i/lub hepatomegalię.
Niedokrwistość hemolityczna ma charakter normocytowy lub makrocytowy, a badania biochemiczne wykonane w ramach diagnostyki laboratoryjnej wykazują następujące nieprawidłowości: ↑ stężenia bilirubiny, ↑ stężenia urobilinogenu w moczu, ↑ stężenia sterkobilinogenu w kale, ↑ retikulocytozy, ↑ aktywności LDH, ↑ stężenia żelaza, ↑ haptoglobiny.
U chorych z niedokrwistością hemolityczną należy wykonać bezpośredni test antyglobulinowy (odczyn Coombsa, BTA) oraz przeprowadzić diagnostykę w kierunku chorób autoimmunologicznych i limfoproliferacyjnych.
Niedokrwistość chorób przewlekłych
Niedokrwistość chorób przewlekłych jest drugim najczęstszym po niedokrwistości z niedoboru rodzajem niedokrwistości. Do jej przyczyn należą przewlekły stan zapalny (zakażenie, choroby autoimmunologiczne, nowotwory) oraz inne stany z komponentem zapalnym (np. cukrzyca, niewydolność serca).
Patofizjologia ACD jest złożona i obejmuje zaburzenia metabolizmu żelaza spowodowane indukowanym przez zapalne cytokiny zwiększonym wydzielaniem hepcydyny, zmniejszenie wytwarzania EPO i upośledzenie odpowiedzi na EPO.
Niedokrwistości złożone
W wielu przypadkach patomechanizm niedokrwistości bywa złożony. Niedokrwistość może równocześnie wynikać z niedoboru żelaza, witaminy B12 i/lub kwasu foliowego. Niedokrwistości niedoborowe mogą współistnieć z ACD.
W diagnostyce niedokrwistości należy zatem uwzględnić przyczyny złożone, np. obfite krwawienia miesięczne i niedobór żelaza w pożywieniu. Niedokrwistość o charakterze złożonym często obserwuje się u osób starszych w wyniku współwystępowania niedożywienia, zaburzeń opróżniania żołądka, utajonego krwawienia z przewodu pokarmowego oraz chorób współistniejących, w tym chorób zapalnych czy nowotworów. Liczne przyczyny może mieć również niedokrwistość wywołana utratą krwi w trakcie dializy, przewlekłym stanem zapalnym i zmniejszonym klirensem hepcydyny, jak również przyjmowanymi lekami (inhibitory pompy protonowej, antykoagulanty).
Z powyższych względów należy pamiętać, aby poszukując przyczyny niedokrwistości, brać pod uwagę całość obrazu klinicznego, a nie tylko wynik pojedynczego testu.
Piśmiennictwo
1. Hempel EV, Bollard ER. The evidence-based evaluation of iron deficiency anemia. Med Clin N Am 2016; 100: 1065-1075.
2. DeLoughery TG. Iron deficiency anemia. Med Clin N Am 2017; 101: 319-332.
3. Camaschella C. Iron-deficiency anemia. N Engl J Med 2015; 372: 1832-1843.
4. Pavord S, Myers B, Robinson S i wsp.; British Committee for Standards in Haematology. UK guidelines on the management of iron deficiency in pregnancy. Br J Haematol 2012; 156: 588-600.
Pełna treść artykułu: Iwona Hus, Agnieszka Mastalerz-Migas. Algorytm różnicowania przyczyn niedokrwistości. Lekarz POZ 2022; 8 (1): 12-17.
Definicja niedokrwistości
Niedokrwistość to stan kliniczny objawiający się zmniejszeniem stężenia hemoglobiny (Hgb) i hematokrytu (Ht) poniżej wartości przyjętych za normę dla danej płci i wieku. Liczba krwinek czerwonych może być zmniejszona, zwiększona lub prawidłowa w zależności od przyczyny i stopnia nasilenia niedokrwistości. Wartości stężenia Hgb definiujące niedokrwistość w zależności od płci i wieku przedstawiono w tabeli 1, a stopnie niedokrwistości według Światowej Organizacji Zdrowia (World Health Organization – WHO) w tabeli 2.


Przyczyny niedokrwistości
Niedokrwistość nie jest samodzielną jednostką chorobową, ale należy ją traktować jako następstwo stanu chorobowego toczącego się w organizmie. Warunkiem skutecznego leczenia niedokrwistości jest poznanie jej przyczyny. Przyczyny niedokrwistości obejmują cztery główne grupy przedstawione w tabeli 3.

Inny podział, często wykorzystywany w diagnostyce niedokrwistości, jest oparty na objętości krwinki czerwonej (mean corpuscular value – MCV) (tab. 4).

Najczęstsze rodzaje niedokrwistości to niedokrwistość z niedoboru żelaza (iron deficiency anemia – IDA) oraz niedokrwistość chorób przewlekłych (anemia of chronic diseases – ACD).
Diagnostyka niedokrwistości
W praktyce często wykorzystywany jest algorytm diagnostyki niedokrwistości zależny od wartości MCV, przedstawiony na rycinie 1.

Niedokrwistości niedoborowe
Niedokrwistość z niedoboru żelaza
Obraz kliniczny niedokrwistości z niedoboru żelaza oprócz objawów typowych dla każdej niedokrwistości obejmuje również symptomy tkankowego niedoboru żelaza, takie jak: zaburzenia troficzne skóry, suchość skóry i włosów, łamliwość włosów i paznokci, deformacje płytki paznokciowej, zajady w kącikach ust, atroficzne bolesne zapalenie błony śluzowej jamy ustnej, bóle głowy, zaburzenia koncentracji, rozdrażnienie lub senność, „niespokojne nogi”, spaczone łaknienie (pica) – „zachcianki” na rzeczy niejadalne, np. ziemię, błoto, lód.
Wyróżnia się trzy główne przyczyny niedokrwistości z niedoboru żelaza, które należy uwzględnić w diagnostyce różnicowej:
• przewlekła utrata krwi:
» obfite krwawienia miesięczne, krwawienia z dróg rodnych,
» krwawienia z przewodu pokarmowego – choroba wrzodowa żołądka, zakażenie Helicobacter pylori, angiodysplazja, choroby zapalne jelit (choroba Leśniowskiego-Crohna), zmiany łagodne lub nowotworowe (rak żołądka, jelita grubego), leki (NLPZ),
» krwawienia z dróg moczowych,
» wewnątrznaczyniowa hemoliza (utrata żelaza z moczem);
• brak wystarczającej ilości żelaza w diecie:
» zwiększone zapotrzebowanie (kobiety w ciąży, dzieci i młodzież),
» niedobór w diecie (dieta wegetariańska, osoby starsze);
• zaburzenia wchłaniania żelaza w przewodzie pokarmowym:
» celiakia (5–6% chorych z IDA, najczęstsza pozajelitowa manifestacja celiakii),
» autoimmunologiczne zapalenie żołądka,
» choroby zapalne jelit (np. choroba Leśniowskiego-Crohna),
» zakażenie Helicobacter pylori (konkurencja o żelazo, nadżerki), Giardia lamblia,
» stan po gastrektomii, po operacji bariatrycznej (IDA u 45% chorych),
» dieta bogata w substancje upośledzające wchłanianie żelaza (fosforany, szczawiany, fityniany, garbniki, polifenole, suplementy cynku i manganu),
» leki (np. inhibitory pomby protonowej, leki zobojętniające, blokery H2).
Niedokrwistość z niedoboru żelaza najczęściej występuje u kobiet w wieku menoplauzalnym, jej przyczyną są nieprawidłowe krwawienia miesięczne. Często obserwowana jest również u kobiet w ciąży. Zazwyczaj przyczyną IDA u kobiet w wieku pomenopauzalnym i mężczyzn są choroby przewodu pokarmowego (50–70%), dlatego badanie przewodu pokarmowego stanowi niezbędny element postępowania diagnostycznego.
Diagnostyka przewodu pokarmowego powinna obejmować: gastroskopię, kolonoskopię, diagnostykę jelita cienkiego (endoskopia kapsułkowa, enteroskopia balonowa), badania w kierunku celiakii (przeciwciała przeciw transglutaminazie tkankowej lub endomysium), badania w kierunku zakażenia Helicobacter pylori lub Giardia lamblia, przeciwciała przeciw komórkom okładzinowym żołądka.
Należy również pamiętać o przyczynach urologicznych i wykonaniu badania ogólnego moczu w celu wykluczenia krwinkomoczu.
Diagnostyka laboratoryjna powinna obejmować ocenę morfologii krwi i gospodarki żelazowej. W morfologii krwi typowe dla niedoboru żelaza jest obniżone MCV (czułość 96,7%), ale w 40% przypadków IDA wartość MCV jest prawidłowa. Obserwuje się również podwyższenie wskaźnika RDW (rozpiętość rozkładu erytrocytów). Wartość RDW jest prawidłowa w talasemii, w której podobnie jak w przypadku niedoboru żelaza występuje obniżenie MCV.
Spośród parametrów gospodarki żelazowej najważniejszym wskaźnikiem jest ferrytyna, której stężenie w surowicy odzwierciedla całkowite zapasy żelaza w organizmie. Ferrytyna cechuje się dużą swoistością, ale jest również białkiem ostrej fazy, w związku z czym jej stężenie wzrasta w przebiegu stanów zapalnych, w zakażeniach, chorobach autoimmunologicznych oraz przy uszkodzeniu wątroby. Zwykle w IDA stężenie ferrytyny wynosi < 15 – 10 µg/l. O niedoborze żelaza przy współistniejącym stanie zapalnym świadczy stężenie ferrytyny < 100 µg/l.
Zwiększenie stężenia transferyny lub całkowitej zdolności wiązania żelaza (TIBC) jest parametrem swoistym dla IDA, ale cechuje się małą czułością (zmniejszenie w stanie zapalnym, w starszym wieku, przy niedożywieniu). Wartościowym parametrem niezależnym od stanu zapalnego jest saturacja transferyny (TSAT, %) obliczana według wzoru: (stężenie żelaza/stężenie transferyny) × 1,41. Zwykle u pacjentów z IDA wartość TSAT jest < 16%. U chorych z niewydolnością krążenia lub niewydolnością nerek IDA rozpoznaje się przy saturacji transferyny < 30% i stężeniu ferrytyny < 300 µg/l. Należy unikać rozpoznawania niedoboru żelaza na podstawie oznaczenia stężenia żelaza, uważanego za suboptymalny test diagnostyczny z powodu obniżonego stężenia w stanach zapalnych, fałszywie podwyższonego przy doustnej suplementacji oraz dużej zmienności oznaczeń z dnia na dzień. Stężenie żelaza należy ocenić, jeśli jest potrzeba obliczenia saturacji transferyny.
W tabeli 5 przedstawiono zmiany w morfologii krwi oraz parametrach gospodarki żelazowej związane z postępującym niedoborem żelaza, a w tabeli 6 różnicowanie między IDA i ACD.

Niedokrwistość megaloblastyczna
Niedokrwistość megaloblastyczna jest wywołana niedoborem witaminy B12 i/lub kwasu foliowego. Dzienne zapotrzebowanie na witaminę B12 wynosi 1–2 µg, dieta zachodnia zawierająca produkty pochodzenia zwierzęcego jest wystarczająca do pokrycia zapotrzebowania dobowego. Zapasy w organizmie wynoszące 2–3 mg wystarczają na okres 3–5 lat. Dzienne zapotrzebowanie na kwas foliowy wynosi 0,1–0,2 mg. Dieta zachodnia zawiera 0,5–0,7 mg (świeże warzywa). Zapasy kwasu foliowego w organizmie wynoszą 10–15 mg i wystarczają na 2 miesiące.
Do przyczyn niedoboru witaminy B12 należą:
• niedobór w diecie (bardzo rzadko – ścisła dieta wegańska),
• zaburzenia wchłaniania:
» niedokrwistość Addisona-Biermera (przeciwciała przeciw komórkom okładzinowym żołądka – najczęstsza przyczyna ciężkiego niedoboru),
» przewlekłe zanikowe zapalenie żołądka – 20% osób w starszym wieku;
• inne przyczyny: niewydolność trzustki, zespół ślepej pętli, gastrektomia, chirurgiczna resekcja końcowego odcinka ileum.
Niedobór kwasu foliowego może być wynikiem jego niewystarczającej podaży w diecie, alkoholizmu, zaburzeń wchłaniania, zwiększonego zapotrzebowania (niedokrwistość hemolityczna, leczenie metoreksatem).
W przypadku niedoboru zarówno witaminy B12, jak i kwasu foliowego występują objawy ze strony przewodu pokarmowego, takie jak brak apetytu (osłabienie wrażeń smakowych), cechy zapalenia błony śluzowej jamy ustnej, cechy zapalenia języka w postaci pieczenia, wygładzenia języka (język Huntera), skłonność do biegunek lub zaparć i nudności. Objawy neurologiczne (zaburzenia ze strony ośrodkowego układu nerwowego) związane są wyłącznie z niedoborem witaminy B12 i wynikają z demielinizacji neuronów rdzenia kręgowego oraz kory mózgowej. Zmiany utrzymujące się ponad 1/2 roku nie cofają się, dlatego tak istotne jest różnicowanie i właściwe leczenie niedokrwistości megaloblastycznej.
Obraz kliniczny obejmuje: zmiany psychiczne (spowolnienie psychiczne i apatia, trudności w przeprowadzeniu prostych rachunków arytmetycznych, zaburzenia pamięci, drażliwość, depresja, stupor, urojenia, halucynacje, paranoja, tzw. obłęd megaloblastyczny) oraz objawy związane ze zwyrodnieniem powrózkowym rdzenia kręgowego (zaburzenia czucia głębokiego, ataksja, parestezje, uczucie drętwienia, niestabilność chodu).
W rozmazie krwi obwodowej widoczne są wyraźne zmiany morfologii krwinek: zwiększenie MCV, megaloowalocytoza i hiperchromia erytrocytów, anizocytoza i poikilocytoza, hipersegmentacja jąder granulocytów (ponad 5% granulocytów z liczbą segmentów 6 i więcej) oraz obecność patologicznych płytek krwi (megatrombocytów).
Nieprawidłowości w badaniach biochemicznych obejmują hiperbilirubinemię (pośrednia – w wyniku hemolizy) i podwyższone stężenie LDH. Stężenie żelaza w surowicy jest w normie lub podwyższone.
Diagnostyka niedokrwistości megaloblastycznej powinna uwzględniać badania laboratoryjne: oznaczanie stężenia kwasu foliowego i witaminy B12. W razie wątpliwości należy oznaczyć stężenie kwasu metylomalonowego i homocysteiny. Należy również przeprowadzić badanie czynności wydzielniczej żołądka i stanu jego błony śluzowej (gastroskopia z oceną histopatologiczną wycinka błony śluzowej, badanie obecności przeciwciał przeciw komórkom okładzinowym żołądka i czynnikowi wewnętrznemu Castle’a).
Niedokrwistość hemolityczna
W obrazie klinicznym niedokrwistości hemolitycznej oprócz ogólnych objawów niedokrwistości obserwuje się:
• objawy ogólne, takie jak: gorączka, ból mięśni i stawów, objawy żółtaczki,
• splenomegalię i/lub hepatomegalię.
Niedokrwistość hemolityczna ma charakter normocytowy lub makrocytowy, a badania biochemiczne wykonane w ramach diagnostyki laboratoryjnej wykazują następujące nieprawidłowości: ↑ stężenia bilirubiny, ↑ stężenia urobilinogenu w moczu, ↑ stężenia sterkobilinogenu w kale, ↑ retikulocytozy, ↑ aktywności LDH, ↑ stężenia żelaza, ↑ haptoglobiny.
U chorych z niedokrwistością hemolityczną należy wykonać bezpośredni test antyglobulinowy (odczyn Coombsa, BTA) oraz przeprowadzić diagnostykę w kierunku chorób autoimmunologicznych i limfoproliferacyjnych.
Niedokrwistość chorób przewlekłych
Niedokrwistość chorób przewlekłych jest drugim najczęstszym po niedokrwistości z niedoboru rodzajem niedokrwistości. Do jej przyczyn należą przewlekły stan zapalny (zakażenie, choroby autoimmunologiczne, nowotwory) oraz inne stany z komponentem zapalnym (np. cukrzyca, niewydolność serca).
Patofizjologia ACD jest złożona i obejmuje zaburzenia metabolizmu żelaza spowodowane indukowanym przez zapalne cytokiny zwiększonym wydzielaniem hepcydyny, zmniejszenie wytwarzania EPO i upośledzenie odpowiedzi na EPO.
Niedokrwistości złożone
W wielu przypadkach patomechanizm niedokrwistości bywa złożony. Niedokrwistość może równocześnie wynikać z niedoboru żelaza, witaminy B12 i/lub kwasu foliowego. Niedokrwistości niedoborowe mogą współistnieć z ACD.
W diagnostyce niedokrwistości należy zatem uwzględnić przyczyny złożone, np. obfite krwawienia miesięczne i niedobór żelaza w pożywieniu. Niedokrwistość o charakterze złożonym często obserwuje się u osób starszych w wyniku współwystępowania niedożywienia, zaburzeń opróżniania żołądka, utajonego krwawienia z przewodu pokarmowego oraz chorób współistniejących, w tym chorób zapalnych czy nowotworów. Liczne przyczyny może mieć również niedokrwistość wywołana utratą krwi w trakcie dializy, przewlekłym stanem zapalnym i zmniejszonym klirensem hepcydyny, jak również przyjmowanymi lekami (inhibitory pompy protonowej, antykoagulanty).
Z powyższych względów należy pamiętać, aby poszukując przyczyny niedokrwistości, brać pod uwagę całość obrazu klinicznego, a nie tylko wynik pojedynczego testu.
Piśmiennictwo
1. Hempel EV, Bollard ER. The evidence-based evaluation of iron deficiency anemia. Med Clin N Am 2016; 100: 1065-1075.
2. DeLoughery TG. Iron deficiency anemia. Med Clin N Am 2017; 101: 319-332.
3. Camaschella C. Iron-deficiency anemia. N Engl J Med 2015; 372: 1832-1843.
4. Pavord S, Myers B, Robinson S i wsp.; British Committee for Standards in Haematology. UK guidelines on the management of iron deficiency in pregnancy. Br J Haematol 2012; 156: 588-600.
Pełna treść artykułu: Iwona Hus, Agnieszka Mastalerz-Migas. Algorytm różnicowania przyczyn niedokrwistości. Lekarz POZ 2022; 8 (1): 12-17.








