29.09.2021
Redaktor:
Agnieszka Starewicz-Jaworska
Źródło: Kurier Medyczny/dr hab. n. med. Marcin Barylski
Telmisartan z hydrochlorotiazydem – o czym należy pamiętać
W zaleceniach PTNT z 2019 r. sartany należą do pięciu głównych grup leków stosowanych w leczeniu hipotensyjnym, wykorzystywanych zarówno w monoterapii, jak i w leczeniu skojarzonym. Przyjęta w aktualnych i poprzednich wytycznych strategia leczenia farmakologicznego nadciśnienia tętniczego kładzie nacisk na jego indywidualizację.
Tekst dr. hab. n. med. Marcina Barylskiego z FESC Kliniki Chorób Wewnętrznych i Rehabilitacji Kardiologicznej Uniwersytetu Medycznego w Łodzi i Uniwersytetu Szpital Kliniczny im. Wojskowej Akademii Medycznej – Centralny Szpital Weteranów
– Miejsce sartanów w zaleceniach PTNT
Antagoniści receptora angiotensyny II (sartany) to nowoczesna grupa leków hipotensyjnych o dużej skuteczności w prewencji sercowo-naczyniowej, potwierdzonej w dużych badaniach klinicznych. W zaleceniach Polskiego Towarzystwa Nadciśnienia Tętniczego (PTNT) z 2019 r. sartany należą do pięciu głównych grup leków stosowanych w leczeniu hipotensyjnym, wykorzystywanych zarówno w monoterapii, jak i w leczeniu skojarzonym. Przyjęta w aktualnych i poprzednich wytycznych strategia leczenia farmakologicznego nadciśnienia tętniczego kładzie nacisk na jego indywidualizację. Ze względu na potencjalne korzyści pozahipotensyjne udokumentowane w dużych badaniach klinicznych duże znaczenie ma wybór terapii pierwszego rzutu. Biorąc pod uwagę indywidualne wskazania, sartany należą do leków pierwszego wyboru w następujących sytuacjach klinicznych: przerost lewej komory serca, przebyty udar mózgu, zespół metaboliczny, cukrzyca, powikłania sercowo-naczyniowe i metaboliczne (w tym wskazaniu tylko telmisartan), hiperurykemia lub dna moczanowa, albuminuria lub białkomocz, przewlekła choroba nerek (cukrzycowa lub niecukrzycowa), niewydolność nerek, zaburzenia potencji, astma oskrzelowa, przewlekła obturacyjna choroba płuc.
Zgodnie z wytycznymi PTNT 2019 sartany należą do leków drugiego wyboru w następujących sytuacjach klinicznych: choroba niedokrwienna serca (przy nietolerancji inhibitorów konwertazy angiotensyny (ACE-I) – preferowane telmisartan i walsartan), niewydolność serca (przy nietolerancji ACE-I – preferowane kandesartan i walsartan), nadciśnienie tętnicze u osób w podeszłym wieku, izolowane nadciśnienie skurczowe, powikłania sercowo-naczyniowe i metaboliczne (przy nietolerancji ACE-I, poza telmisartanem, który ma status leku pierwszego wyboru na równi z ACE-I).
Telmisartan
Telmisartan wyróżnia się szczególnie korzystnym profilem farmakokinetycznym. Jego efekt hipotensyjny jest wynikiem długotrwałej i selektywnej blokady receptorów AT1 dla angiotensyny II. Na podstawie badań in vitro ustalono, że ma on największe powinowactwo do wiązania z ludzkim receptorem angiotensyny II typu 1 i zarazem najwolniej spośród wszystkich sartanów od niego dysocjuje. Należy również podkreślić, że telmisartan jest najbardziej lipofilnym sartanem, co ułatwia mu dyfuzję przez błony komórkowe i dotarcie do trudno dostępnych kompartmentów tkankowych.
Po podaniu doustnym telmisartan szybko wchłania się z przewodu pokarmowego, osiągając maksymalne stężenie we krwi w czasie 0,5–1,5 godziny. Jego całkowita biodostępność wynosi ok. 50 proc. i tylko w niewielkim stopniu zmniejsza ją przyjmowanie leku łącznie z pokarmem. Pozorna objętość dystrybucji, która określa zdolność leku do przekraczania bariery układu naczyniowego i penetracji do narządów dobrze ukrwionych, wynosi dla telmisartanu 500 litrów i jest największa nie tylko spośród sartanów, ale również pozostałych leków hamujących układ renina–angiotensyna–aldosteron (RAA). Dzięki temu telmisartan może w znacznie większym stopniu niż inne leki z tej grupy penetrować do tkanek obwodowych, gwarantując blokadę układu RAA zarówno miejscową, jak i ogólnoustrojową.
Telmisartan jest metabolizowany w wątrobie i podlega powolnej eliminacji. Większa część podanej dawki (> 97 proc.) zostaje usunięta drogą wydalania żółciowego z kałem. Z moczem są wydalane jedynie niewielkie ilości leku (< 1 proc.), co w dużym stopniu uniezależnia jego farmakokinetykę od zaburzeń czynności nerek.
Telmisartan charakteryzuje się korzystnym profilem działania hipotensyjnego utrzymującym się ponad 24 godziny od przyjęcia leku i ma najdłuższy okres półtrwania w osoczu, który wynosi 24 godziny. Jego unikatową cechą jest podobieństwo strukturalne cząsteczki do agonistów receptorów jądrowych PPAR-g, co nadaje mu właściwości tiazolidinedionów w postaci: zwiększania insulinowrażliwości, zwiększania obwodowego zużycia glukozy, hamowania uwalniania wolnych kwasów tłuszczowych z adipocytów, zmniejszania zawartości tłuszczów w tkance mięśniowej i wątrobie, zwiększania stężenia cholesterolu frakcji HDL, hamowania uwalniania niektórych mediatorów i cytokin zapalnych, zwiększania stężenia przeciwmiażdżycowej adiponektyny, korzystnego wpływu na morfologię i czynność komórek b trzustki. Ponadto telmisartan nie wchodzi w interakcje z większością leków powszechnie stosowanych w kardiologii. Poza niewielkim wpływem na izoenzym cytochromu CYP2C19 nie wykazuje interakcji z układem enzymatycznym CYP.
W wytycznych PTNT 2019 u pacjentów z wysokim ryzykiem sercowo-naczyniowym (powikłania sercowo-naczyniowe i metaboliczne) telmisartanowi przyznano pozycję leku pierwszego wyboru na równi z ACE-I (perindoprilem i ramiprilem). Argumentem uzasadniającym powyższą decyzję były wyniki badania ONTARGET, które miały również wpływ na wskazania rejestracyjne dla telmisartanu w dawce 80 mg, będącego obecnie jedynym sartanem zarejestrowanym do stosowania w profilaktyce incydentów sercowo-naczyniowych. Telmisartan ma również potwierdzoną skuteczność w zakresie działania nefroprotekcyjnego, ochronnego wpływu na ośrodkowy układ nerwowy, korzystnego wpływu na funkcje poznawcze, poprawy
funkcji śródbłonka naczyniowego, zmniejszania ryzyka migotania przedsionków.
Hydrochlorotiazyd
Hydrochlorotiazyd (HCTZ) działa w końcowym, korowym odcinku pętli nefronu oraz w początkowej części kanalika dalszego. Powoduje zwiększone wydalanie jonów sodu, potasu i magnezu oraz hamowanie wydalania jonów wapnia. Wchłania się z przewodu pokarmowego w 50–60 proc. i wiąże się z białkami surowicy w 67,9 proc. Nie jest metabolizowany, ale szybko eliminowany przez nerki w postaci niezmienionej. W przypadku stosowania HCTZ diureza rozpoczyna się po 2 godzinach, a maksymalny efekt zostaje osiągnięty po ok. 4 godzinach.
Panująca opinia o metabolicznych działaniach niepożądanych HCTZ wiąże się z faktem, że w przeszłości był on stosowany w wysokich dawkach. Jego stosowanie w małej dawce w lekach złożonych przynosi następujące korzyści: zmniejszenie chorobowości i śmiertelności, zmniejszenie ciśnienia tętniczego (szczególnie u osób spożywających duże ilości soli), zwiększenie efektywności hipotensyjnej, zmniejszenie utraty wapnia (efekt przeciwosteoporotyczny).
Lek złożony: telmisartan i HCTZ – dla kogo szczególnie wskazany?
Telmisartan można bezpiecznie wykorzystywać w połączeniach z większością stosowanych obecnie preparatów hipotensyjnych, oprócz ACE-I. Zgodnie z obowiązującymi wytycznymi PTNT 2019 diuretyki tiazydowe stanowią jedną z pięciu podstawowych grup leków hipotensyjnych, a połączenie z sartanem należy do preferowanych skojarzeń pierwszego rzutu. W zakrojonych na szeroką skalę badaniach klinicznych potwierdzono skuteczność i bezpieczeństwo leczenia skojarzonego telmisartanem i HCTZ pacjentów dorosłych, w tym osób starszych. W badaniach klinicznych zgodnie wykazano, że dołączenie HCTZ, nawet w małej dawce, wyraźnie zwiększa przeciwnadciśnieniowy efekt leczenia.
Zastosowanie tego skojarzenia wiąże się więc nie tylko z istotniejszym zmniejszeniem ciśnienia tętniczego, lecz także z większym odsetkiem pacjentów, u których udaje się osiągnąć docelowe jego wartości, co potwierdzono w badaniach wykorzystujących ABPM w celu oceny efektu hipotensyjnego. Preparat ten podany raz na dobę powoduje efektywne i regularne zmniejszenie ciśnienia tętniczego we wszystkich dawkach terapeutycznych.
Wykazano, że połączenie telmisartanu z HCTZ wiąże się z podobną częstością występowania działań niepożądanych jak w przypadku stosowania telmisartanu w monoterapii. Bardzo dobrą tolerancję zaobserwowano zarówno w grupie pacjentów młodych, jak i wśród chorych w wieku podeszłym.
Połączenie telmisartanu z HCTZ porównywano głównie z preparatami złożonymi, w których skład wchodził inny antagonista receptora angiotensyny II i HCTZ. Godny uwagi jest fakt, że w ramach przeprowadzonych badań oprócz klinicznych pomiarów ciśnienia tętniczego przeprowadzonych w czasie, gdy lek wykazywał najsłabsze działanie, wykonano ABPM, by ocenić, w jakim stopniu kontrolowane jest średnie ciśnienie tętnicze w okresie między kolejnymi dawkami leku. Wyniki wskazują, że preparat złożony telmisartan i HCTZ ma dużą skuteczność w obniżaniu ciśnienia tętniczego w okresie poprzedzającym przyjęcie kolejnej dawki (okres zwiększonego ryzyka sercowo-naczyniowego).
Połączenie telmisartanu z HCTZ jest jednym z najskuteczniejszych połączeń leku blokującego układ RAA z lekiem moczopędnym i najsilniejszym spośród skojarzeń sartanu z HCTZ. Należy więc oczekiwać, że uzyskany lepszy efekt hipotensyjny w odległej obserwacji przełoży się na zmniejszenie częstości incydentów sercowo-naczyniowych i poprawę rokowania.
Połączenie telmisartanu z HCTZ uznaje się za optymalne pod względem synergistycznego działania hipotensyjnego i przeciwstawnego działania metabolicznego obu składowych. Preparat ten wyróżnia bardzo dobra tolerancja wynikająca z ograniczania przez sartan działań niepożądanych diuretyku tiazydowego (szczególnie hipokaliemii) oraz szczególnej cechy sartanów, jaką jest liczba objawów niepożądanych równa notowanej dla placebo.
Ponadto przy zastosowaniu preparatu złożonego wykorzystuje się znane zjawisko lepszego przestrzegania zaleceń przez pacjentów i dłuższą wytrwałość terapeutyczną w porównaniu ze stosowaniem tych samych leków w dwóch osobnych preparatach.
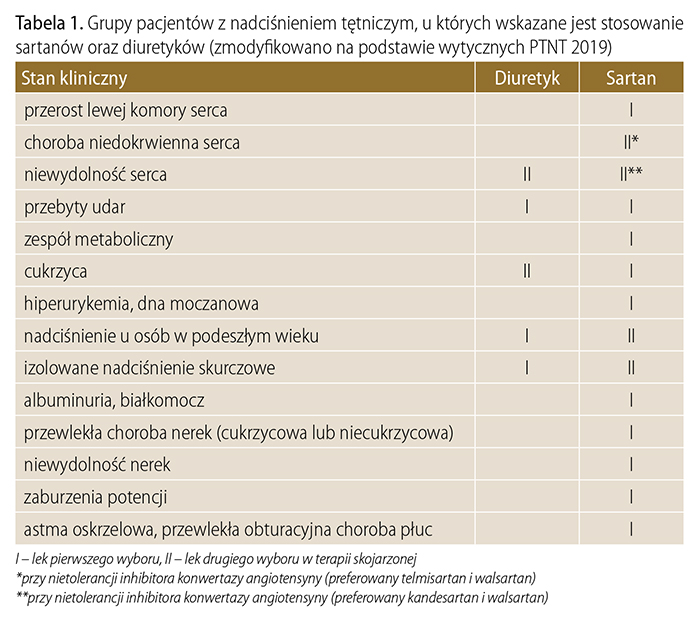
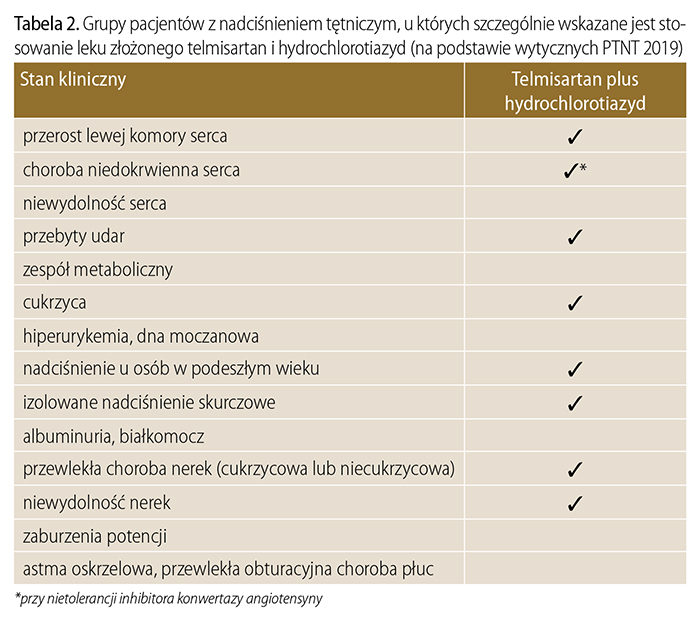
Preparat złożony telmisartan i HCTZ, który charakteryzuje się dużą skutecznością hipotensyjną, z pewnością spełni oczekiwania dotyczące grup pacjentów obciążonych wysokim ryzykiem sercowo-naczyniowym, z cukrzycą oraz z powikłaniami naczyniowymi i nerkowymi. W tabeli 1 przedstawiono grupy pacjentów z nadciśnieniem tętniczym, u których wskazane jest stosowanie sartanów (telmisartanu) i diuretyków (HCTZ), a w tabeli 2 szczególne grupy pacjentów, u których warto to połączenie rozważyć.
Piśmiennictwo:
Bakris G, Burgess E, Weir M i wsp.; AMADEO Study Investigators. Telmisartan is more effective than losartan in reducing proteinuria in patients with diabetic nephropathy. Kidney Int 2008; 74: 364-369.
Barnett AH, Bain SC, Bouter P i wsp. Diabetics Exposed to Telmisartan and Enalapril Study Group. Angiotensin-receptor blockade versus converting-enzyme inhibition in type 2 diabetes and nephropathy. N Engl J Med 2004; 351: 1952-1961.
Barylski M, Banach M, Ciećwierz J, Kowalski J. Telmisartan równie skuteczny jak ramipril w populacji chorych z wysokim ryzykiem zdarzeń sercowo-naczyniowych – wyniki badania ONTARGET. Geriatria 2008; 2: 157-168.
Beermann B, Groschinsky-Grind M. Pharmacokinetics of hydrochlorothiazide in man. Eur J Clin Pharmacol 1977; 12: 297-303.
Benson SC, Pershadsingh HA, Ho CI i wsp. Identification of telmisartan as a unique angiotensin II receptor antagonist with selective PPAR-gamma modulating activity. Hypertension 2004; 43: 993-1002.
Birkett DJ. Pharmacokinetics made easy. McGraw Hill, New York 2010.
Burnier M, Brunner HR. Angiotensin II receptor antagonists. Lancet 2000; 355: 637-645.
Charakterystyka produktu leczniczego Zanacodar, 80 mg, tabletki; 17.04.2015.
Dzau VJ. Tissue angiotensin and pathobiology of vascular disease a unifying hypothesis. Hypertension 2001; 37: 1047-1052.
Fabris B, Chen BZ, Pupic V i wsp. Inhibition of angiotensin-converting enzyme (ACE) in plasma and tissue.
J Cardiovasc Pharmacol 1990; 15 (Suppl. 2): S6-S13.
Galle J, Schwedhelm E, Pinnetti S. Antiproteinuric effects of angiotensin receptor blockers: telmisartan versus valsartan in hypertensive patients with type 2 diabetes mellitus and overt nephropathy. Nephrol Dial Transplant 2008; 23: 3174-3183.
Hermann TW. Farmakokinetyka. Teoria i praktyka. Wydawnictwo Lekarskie PZWL, Warszawa 2002.
Januszewicz A, Januszewicz W, Rużyłło W. Inhibitory konwertazy angiotensyny w leczeniu chorób układu sercowo-naczyniowego. Medycyna Praktyczna, Kraków 2005.
Kjeldsen SE, Schumacher H, Neldam S, Guthrie RM. Telmisartan/hydrochlorothiazide combination therapy for the treatment of hypertension: a pooled analysis in older and younger patients. J Clin Hypertens (Greenwich) 2013; 15: 380-388.
Lacourcière Y, Martin K. Comparison of a fixed-dose combination of telmisartan 40 mg plus hydrochlorothiazide 12.5 mg with telmisartan 40 mg in the control of mild-to-moderate hypertension. Am J Ther 2002; 9: 111-117.
Lacourcière Y, Tytus R, O’Keefe D i wsp. Efficacy and tolerability of a fixed-dose combination of telmisartan plus hydrochlorothiazide in patients uncontrolled with telmisartan monotherapy. J Hum Hypertens 2001; 15: 763-770.
Makino H, Haneda M, Babazono T, Moriva T. Microalbuminuria reduction with telmisartan in normotensive and hypertensive Japanese patients with type 2 diabetes: a posthoc analysis of The Incipient to Overt: Angiotensin II Blocker, Telmisartan, Investigation on Type 2 Diabetic Nephropathy (INNOVATION) study. Hypertens Res 2008; 31: 657-664.
McClellan KJ, Markham A. Telmisartan. Drugs 1998; 56: 1039-1044.
McGill JB, Reilly PA. Telmisartan plus hydrochlorothiazide versus telmisartan or hydrochlorothiazide monotherapy in patients with mild to moderate hypertension: a multicenter, randomized, double-blind, placebo-controlled, parallel-group trial. Clin Ther 2001; 23: 833-850.
Neldam S, Edwards C; ATHOS Study Group. Telmisartan plus hydrochlorothiazide compared with amlodipine plus hydrochlorothiazide in older patients with systolic hypertension: Results from a large ABPM study. Am J Geriat Cardiol 2006; 15: 151-160.
Neutel JM, Littlejohan TW, Chrysant SG, Singh SA. Telmisartan/hydrochlorothiazide in comparison with losartan/ hydrochlorothiazide in managing patients with mild-to-moderate hypertension. Hypertens Res 2005; 28: 555-563.
Pan G, Zhou X, Zhao J. Effect of telmisartan on atrial fibrillation recurrences in patients with hypertension: a systematic review and meta-analysis. Cardiovasc Ther 2014; 32: 184-188.
Parati G, Bilo G, Redon J; SURGE Steering Committee. The effects of telmisartan alone or with hydrochlorothiazide on morning and 24-h ambulatory BP control: results from a practice-based study (SURGE 2). Hypertens Res 2013; 36: 322-327.
Prejbisz A, Januszewicz A. Antagoniści receptora angiotensyny II w terapii nadciśnienia tętniczego i chorób współistniejących. Medycyna Praktyczna, Kraków 2014.
Re RN. Mechanisms of disease: local renin-angiotensin-aldosterone systems and the pathogenesis and treatment of cardiovascular disease. Nat Clin Pract Cardiovasc Med 2004; 1: 42-47.
Schmieder RE, Delles C, Mimran A i wsp. Impact of telmisartan versus ramipril on renal endothelial function in patients with hypertension and type 2 diabetes. Diabetes Care 2007; 30: 1351-1356.
Sharma AM, Davidson J, Koval S, Lacourciere Y. Telmisartan/hydrochlorothiazide versus valsartan/hydrochlorothiazide in obese hypertensive patients with type 2 diabetes: the SMOOTH study. Cardiovasc Diabetol 2007; 6: 28.
Shiga Y, Miura S, Mitsutake R i wsp. Efficacy and safety of a single-pill fixed-dose combination of high-dose telmisartan/ hydrochlorothiazide in patients with uncontrolled hypertension. J Renin Angiotensin Aldosterone Syst 2012; 13: 394-400.
Takagi H, Umemoto T. A meta-analysis of randomized controlled trials of telmisartan for flow-mediated dilatation. Hypertens Res 2014; 37: 845-851.
Yusuf S, Teo KK, Pogue J i wsp.; The ONTARGET Investigators. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547-1559.
Tykarski A, Filipiak KJ, Januszewicz A i wsp. Zasady postępowania w nadciśnieniu tętniczym – 2019 rok. Wytyczne Polskiego Towarzystwa Nadciśnienia Tętniczego. Nadciśnienie Tętnicze w Praktyce 2019; 5: 1-84.
Unger T, Schölkens BA. Angiotensin. Vol. II. Springer-Verlag, Berlin Heidelberg 2004.
Wienen W, Enthzerod M, van Meel JCA i wsp. A review on telmisartan: a novel, long acting aniotensin II-receptor antagonist. Cardiovasc Drug Rev 2000; 18; 127-156.
Zhu DL, Bays H, Gao P i wsp. Efficacy and tolerability of initial therapy with single-pill combination telmisartan/hydrochlorothiazide 80/25 mg in patients with grade 2 or 3 hypertension: a multinational, randomized, double-blind, active-controlled trial. Clin Ther 2012; 34: 1613-1624.
Tekst opublikowano w „Kurierze Medycznym” 5/2021. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.

– Miejsce sartanów w zaleceniach PTNT
Antagoniści receptora angiotensyny II (sartany) to nowoczesna grupa leków hipotensyjnych o dużej skuteczności w prewencji sercowo-naczyniowej, potwierdzonej w dużych badaniach klinicznych. W zaleceniach Polskiego Towarzystwa Nadciśnienia Tętniczego (PTNT) z 2019 r. sartany należą do pięciu głównych grup leków stosowanych w leczeniu hipotensyjnym, wykorzystywanych zarówno w monoterapii, jak i w leczeniu skojarzonym. Przyjęta w aktualnych i poprzednich wytycznych strategia leczenia farmakologicznego nadciśnienia tętniczego kładzie nacisk na jego indywidualizację. Ze względu na potencjalne korzyści pozahipotensyjne udokumentowane w dużych badaniach klinicznych duże znaczenie ma wybór terapii pierwszego rzutu. Biorąc pod uwagę indywidualne wskazania, sartany należą do leków pierwszego wyboru w następujących sytuacjach klinicznych: przerost lewej komory serca, przebyty udar mózgu, zespół metaboliczny, cukrzyca, powikłania sercowo-naczyniowe i metaboliczne (w tym wskazaniu tylko telmisartan), hiperurykemia lub dna moczanowa, albuminuria lub białkomocz, przewlekła choroba nerek (cukrzycowa lub niecukrzycowa), niewydolność nerek, zaburzenia potencji, astma oskrzelowa, przewlekła obturacyjna choroba płuc.
Zgodnie z wytycznymi PTNT 2019 sartany należą do leków drugiego wyboru w następujących sytuacjach klinicznych: choroba niedokrwienna serca (przy nietolerancji inhibitorów konwertazy angiotensyny (ACE-I) – preferowane telmisartan i walsartan), niewydolność serca (przy nietolerancji ACE-I – preferowane kandesartan i walsartan), nadciśnienie tętnicze u osób w podeszłym wieku, izolowane nadciśnienie skurczowe, powikłania sercowo-naczyniowe i metaboliczne (przy nietolerancji ACE-I, poza telmisartanem, który ma status leku pierwszego wyboru na równi z ACE-I).
Telmisartan
Telmisartan wyróżnia się szczególnie korzystnym profilem farmakokinetycznym. Jego efekt hipotensyjny jest wynikiem długotrwałej i selektywnej blokady receptorów AT1 dla angiotensyny II. Na podstawie badań in vitro ustalono, że ma on największe powinowactwo do wiązania z ludzkim receptorem angiotensyny II typu 1 i zarazem najwolniej spośród wszystkich sartanów od niego dysocjuje. Należy również podkreślić, że telmisartan jest najbardziej lipofilnym sartanem, co ułatwia mu dyfuzję przez błony komórkowe i dotarcie do trudno dostępnych kompartmentów tkankowych.
Po podaniu doustnym telmisartan szybko wchłania się z przewodu pokarmowego, osiągając maksymalne stężenie we krwi w czasie 0,5–1,5 godziny. Jego całkowita biodostępność wynosi ok. 50 proc. i tylko w niewielkim stopniu zmniejsza ją przyjmowanie leku łącznie z pokarmem. Pozorna objętość dystrybucji, która określa zdolność leku do przekraczania bariery układu naczyniowego i penetracji do narządów dobrze ukrwionych, wynosi dla telmisartanu 500 litrów i jest największa nie tylko spośród sartanów, ale również pozostałych leków hamujących układ renina–angiotensyna–aldosteron (RAA). Dzięki temu telmisartan może w znacznie większym stopniu niż inne leki z tej grupy penetrować do tkanek obwodowych, gwarantując blokadę układu RAA zarówno miejscową, jak i ogólnoustrojową.
Telmisartan jest metabolizowany w wątrobie i podlega powolnej eliminacji. Większa część podanej dawki (> 97 proc.) zostaje usunięta drogą wydalania żółciowego z kałem. Z moczem są wydalane jedynie niewielkie ilości leku (< 1 proc.), co w dużym stopniu uniezależnia jego farmakokinetykę od zaburzeń czynności nerek.
Telmisartan charakteryzuje się korzystnym profilem działania hipotensyjnego utrzymującym się ponad 24 godziny od przyjęcia leku i ma najdłuższy okres półtrwania w osoczu, który wynosi 24 godziny. Jego unikatową cechą jest podobieństwo strukturalne cząsteczki do agonistów receptorów jądrowych PPAR-g, co nadaje mu właściwości tiazolidinedionów w postaci: zwiększania insulinowrażliwości, zwiększania obwodowego zużycia glukozy, hamowania uwalniania wolnych kwasów tłuszczowych z adipocytów, zmniejszania zawartości tłuszczów w tkance mięśniowej i wątrobie, zwiększania stężenia cholesterolu frakcji HDL, hamowania uwalniania niektórych mediatorów i cytokin zapalnych, zwiększania stężenia przeciwmiażdżycowej adiponektyny, korzystnego wpływu na morfologię i czynność komórek b trzustki. Ponadto telmisartan nie wchodzi w interakcje z większością leków powszechnie stosowanych w kardiologii. Poza niewielkim wpływem na izoenzym cytochromu CYP2C19 nie wykazuje interakcji z układem enzymatycznym CYP.
W wytycznych PTNT 2019 u pacjentów z wysokim ryzykiem sercowo-naczyniowym (powikłania sercowo-naczyniowe i metaboliczne) telmisartanowi przyznano pozycję leku pierwszego wyboru na równi z ACE-I (perindoprilem i ramiprilem). Argumentem uzasadniającym powyższą decyzję były wyniki badania ONTARGET, które miały również wpływ na wskazania rejestracyjne dla telmisartanu w dawce 80 mg, będącego obecnie jedynym sartanem zarejestrowanym do stosowania w profilaktyce incydentów sercowo-naczyniowych. Telmisartan ma również potwierdzoną skuteczność w zakresie działania nefroprotekcyjnego, ochronnego wpływu na ośrodkowy układ nerwowy, korzystnego wpływu na funkcje poznawcze, poprawy
funkcji śródbłonka naczyniowego, zmniejszania ryzyka migotania przedsionków.
Telmisartan to:
• największe powinowactwo do wiązania z receptorem AT1,
• największa lipofilność,
• niewielki wpływ pokarmu na biodostępność leku,
• największa pozorna objętość dystrybucji,
• bezpieczeństwo stosowania u osób z przewlekłą chorobą nerek,
• najdłuższy okres półtrwania,
• wysoki wskaźnik trough-to-peak,
• wiązanie z receptorem PPAR-g,
• niewielkie ryzyko interakcji z innymi lekami,
• jedyny sartan mający rejestrację w profilaktyce incydentów sercowo-naczyniowych,
• w wytycznych PTNT 2019 u pacjentów z wysokim ryzykiem sercowo-naczyniowym (powikłania sercowo-naczyniowe i metaboliczne) jako jedyny sartan ma pozycję leku pierwszego wyboru na równi z ACE-I.
• największe powinowactwo do wiązania z receptorem AT1,
• największa lipofilność,
• niewielki wpływ pokarmu na biodostępność leku,
• największa pozorna objętość dystrybucji,
• bezpieczeństwo stosowania u osób z przewlekłą chorobą nerek,
• najdłuższy okres półtrwania,
• wysoki wskaźnik trough-to-peak,
• wiązanie z receptorem PPAR-g,
• niewielkie ryzyko interakcji z innymi lekami,
• jedyny sartan mający rejestrację w profilaktyce incydentów sercowo-naczyniowych,
• w wytycznych PTNT 2019 u pacjentów z wysokim ryzykiem sercowo-naczyniowym (powikłania sercowo-naczyniowe i metaboliczne) jako jedyny sartan ma pozycję leku pierwszego wyboru na równi z ACE-I.
Hydrochlorotiazyd
Hydrochlorotiazyd (HCTZ) działa w końcowym, korowym odcinku pętli nefronu oraz w początkowej części kanalika dalszego. Powoduje zwiększone wydalanie jonów sodu, potasu i magnezu oraz hamowanie wydalania jonów wapnia. Wchłania się z przewodu pokarmowego w 50–60 proc. i wiąże się z białkami surowicy w 67,9 proc. Nie jest metabolizowany, ale szybko eliminowany przez nerki w postaci niezmienionej. W przypadku stosowania HCTZ diureza rozpoczyna się po 2 godzinach, a maksymalny efekt zostaje osiągnięty po ok. 4 godzinach.
Panująca opinia o metabolicznych działaniach niepożądanych HCTZ wiąże się z faktem, że w przeszłości był on stosowany w wysokich dawkach. Jego stosowanie w małej dawce w lekach złożonych przynosi następujące korzyści: zmniejszenie chorobowości i śmiertelności, zmniejszenie ciśnienia tętniczego (szczególnie u osób spożywających duże ilości soli), zwiększenie efektywności hipotensyjnej, zmniejszenie utraty wapnia (efekt przeciwosteoporotyczny).
Lek złożony: telmisartan i HCTZ – dla kogo szczególnie wskazany?
Telmisartan można bezpiecznie wykorzystywać w połączeniach z większością stosowanych obecnie preparatów hipotensyjnych, oprócz ACE-I. Zgodnie z obowiązującymi wytycznymi PTNT 2019 diuretyki tiazydowe stanowią jedną z pięciu podstawowych grup leków hipotensyjnych, a połączenie z sartanem należy do preferowanych skojarzeń pierwszego rzutu. W zakrojonych na szeroką skalę badaniach klinicznych potwierdzono skuteczność i bezpieczeństwo leczenia skojarzonego telmisartanem i HCTZ pacjentów dorosłych, w tym osób starszych. W badaniach klinicznych zgodnie wykazano, że dołączenie HCTZ, nawet w małej dawce, wyraźnie zwiększa przeciwnadciśnieniowy efekt leczenia.
Zastosowanie tego skojarzenia wiąże się więc nie tylko z istotniejszym zmniejszeniem ciśnienia tętniczego, lecz także z większym odsetkiem pacjentów, u których udaje się osiągnąć docelowe jego wartości, co potwierdzono w badaniach wykorzystujących ABPM w celu oceny efektu hipotensyjnego. Preparat ten podany raz na dobę powoduje efektywne i regularne zmniejszenie ciśnienia tętniczego we wszystkich dawkach terapeutycznych.
Wykazano, że połączenie telmisartanu z HCTZ wiąże się z podobną częstością występowania działań niepożądanych jak w przypadku stosowania telmisartanu w monoterapii. Bardzo dobrą tolerancję zaobserwowano zarówno w grupie pacjentów młodych, jak i wśród chorych w wieku podeszłym.
Lek złożony telmisartan plus HCTZ:
• jest jednym z zalecanych połączeń pierwszego rzutu,
• powoduje efektywne i regularne zmniejszenie ciśnienia tętniczego we wszystkich dawkach terapeutycznych,
• wykazuje dużą skuteczność w obniżaniu ciśnienia tętniczego w okresie poprzedzającym przyjęcie kolejnej dawki,
• jest najsilniejszym ze skojarzeń sartan plus HCTZ,
• wykazuje synergistyczne działanie hipotensyjne i przeciwstawne działanie metaboliczne obu składowych,
• jest dobrze tolerowany.
• jest jednym z zalecanych połączeń pierwszego rzutu,
• powoduje efektywne i regularne zmniejszenie ciśnienia tętniczego we wszystkich dawkach terapeutycznych,
• wykazuje dużą skuteczność w obniżaniu ciśnienia tętniczego w okresie poprzedzającym przyjęcie kolejnej dawki,
• jest najsilniejszym ze skojarzeń sartan plus HCTZ,
• wykazuje synergistyczne działanie hipotensyjne i przeciwstawne działanie metaboliczne obu składowych,
• jest dobrze tolerowany.
Połączenie telmisartanu z HCTZ porównywano głównie z preparatami złożonymi, w których skład wchodził inny antagonista receptora angiotensyny II i HCTZ. Godny uwagi jest fakt, że w ramach przeprowadzonych badań oprócz klinicznych pomiarów ciśnienia tętniczego przeprowadzonych w czasie, gdy lek wykazywał najsłabsze działanie, wykonano ABPM, by ocenić, w jakim stopniu kontrolowane jest średnie ciśnienie tętnicze w okresie między kolejnymi dawkami leku. Wyniki wskazują, że preparat złożony telmisartan i HCTZ ma dużą skuteczność w obniżaniu ciśnienia tętniczego w okresie poprzedzającym przyjęcie kolejnej dawki (okres zwiększonego ryzyka sercowo-naczyniowego).
Połączenie telmisartanu z HCTZ jest jednym z najskuteczniejszych połączeń leku blokującego układ RAA z lekiem moczopędnym i najsilniejszym spośród skojarzeń sartanu z HCTZ. Należy więc oczekiwać, że uzyskany lepszy efekt hipotensyjny w odległej obserwacji przełoży się na zmniejszenie częstości incydentów sercowo-naczyniowych i poprawę rokowania.
Połączenie telmisartanu z HCTZ uznaje się za optymalne pod względem synergistycznego działania hipotensyjnego i przeciwstawnego działania metabolicznego obu składowych. Preparat ten wyróżnia bardzo dobra tolerancja wynikająca z ograniczania przez sartan działań niepożądanych diuretyku tiazydowego (szczególnie hipokaliemii) oraz szczególnej cechy sartanów, jaką jest liczba objawów niepożądanych równa notowanej dla placebo.
Ponadto przy zastosowaniu preparatu złożonego wykorzystuje się znane zjawisko lepszego przestrzegania zaleceń przez pacjentów i dłuższą wytrwałość terapeutyczną w porównaniu ze stosowaniem tych samych leków w dwóch osobnych preparatach.
Preparat złożony telmisartan i HCTZ, który charakteryzuje się dużą skutecznością hipotensyjną, z pewnością spełni oczekiwania dotyczące grup pacjentów obciążonych wysokim ryzykiem sercowo-naczyniowym, z cukrzycą oraz z powikłaniami naczyniowymi i nerkowymi. W tabeli 1 przedstawiono grupy pacjentów z nadciśnieniem tętniczym, u których wskazane jest stosowanie sartanów (telmisartanu) i diuretyków (HCTZ), a w tabeli 2 szczególne grupy pacjentów, u których warto to połączenie rozważyć.


Piśmiennictwo:
Bakris G, Burgess E, Weir M i wsp.; AMADEO Study Investigators. Telmisartan is more effective than losartan in reducing proteinuria in patients with diabetic nephropathy. Kidney Int 2008; 74: 364-369.
Barnett AH, Bain SC, Bouter P i wsp. Diabetics Exposed to Telmisartan and Enalapril Study Group. Angiotensin-receptor blockade versus converting-enzyme inhibition in type 2 diabetes and nephropathy. N Engl J Med 2004; 351: 1952-1961.
Barylski M, Banach M, Ciećwierz J, Kowalski J. Telmisartan równie skuteczny jak ramipril w populacji chorych z wysokim ryzykiem zdarzeń sercowo-naczyniowych – wyniki badania ONTARGET. Geriatria 2008; 2: 157-168.
Beermann B, Groschinsky-Grind M. Pharmacokinetics of hydrochlorothiazide in man. Eur J Clin Pharmacol 1977; 12: 297-303.
Benson SC, Pershadsingh HA, Ho CI i wsp. Identification of telmisartan as a unique angiotensin II receptor antagonist with selective PPAR-gamma modulating activity. Hypertension 2004; 43: 993-1002.
Birkett DJ. Pharmacokinetics made easy. McGraw Hill, New York 2010.
Burnier M, Brunner HR. Angiotensin II receptor antagonists. Lancet 2000; 355: 637-645.
Charakterystyka produktu leczniczego Zanacodar, 80 mg, tabletki; 17.04.2015.
Dzau VJ. Tissue angiotensin and pathobiology of vascular disease a unifying hypothesis. Hypertension 2001; 37: 1047-1052.
Fabris B, Chen BZ, Pupic V i wsp. Inhibition of angiotensin-converting enzyme (ACE) in plasma and tissue.
J Cardiovasc Pharmacol 1990; 15 (Suppl. 2): S6-S13.
Galle J, Schwedhelm E, Pinnetti S. Antiproteinuric effects of angiotensin receptor blockers: telmisartan versus valsartan in hypertensive patients with type 2 diabetes mellitus and overt nephropathy. Nephrol Dial Transplant 2008; 23: 3174-3183.
Hermann TW. Farmakokinetyka. Teoria i praktyka. Wydawnictwo Lekarskie PZWL, Warszawa 2002.
Januszewicz A, Januszewicz W, Rużyłło W. Inhibitory konwertazy angiotensyny w leczeniu chorób układu sercowo-naczyniowego. Medycyna Praktyczna, Kraków 2005.
Kjeldsen SE, Schumacher H, Neldam S, Guthrie RM. Telmisartan/hydrochlorothiazide combination therapy for the treatment of hypertension: a pooled analysis in older and younger patients. J Clin Hypertens (Greenwich) 2013; 15: 380-388.
Lacourcière Y, Martin K. Comparison of a fixed-dose combination of telmisartan 40 mg plus hydrochlorothiazide 12.5 mg with telmisartan 40 mg in the control of mild-to-moderate hypertension. Am J Ther 2002; 9: 111-117.
Lacourcière Y, Tytus R, O’Keefe D i wsp. Efficacy and tolerability of a fixed-dose combination of telmisartan plus hydrochlorothiazide in patients uncontrolled with telmisartan monotherapy. J Hum Hypertens 2001; 15: 763-770.
Makino H, Haneda M, Babazono T, Moriva T. Microalbuminuria reduction with telmisartan in normotensive and hypertensive Japanese patients with type 2 diabetes: a posthoc analysis of The Incipient to Overt: Angiotensin II Blocker, Telmisartan, Investigation on Type 2 Diabetic Nephropathy (INNOVATION) study. Hypertens Res 2008; 31: 657-664.
McClellan KJ, Markham A. Telmisartan. Drugs 1998; 56: 1039-1044.
McGill JB, Reilly PA. Telmisartan plus hydrochlorothiazide versus telmisartan or hydrochlorothiazide monotherapy in patients with mild to moderate hypertension: a multicenter, randomized, double-blind, placebo-controlled, parallel-group trial. Clin Ther 2001; 23: 833-850.
Neldam S, Edwards C; ATHOS Study Group. Telmisartan plus hydrochlorothiazide compared with amlodipine plus hydrochlorothiazide in older patients with systolic hypertension: Results from a large ABPM study. Am J Geriat Cardiol 2006; 15: 151-160.
Neutel JM, Littlejohan TW, Chrysant SG, Singh SA. Telmisartan/hydrochlorothiazide in comparison with losartan/ hydrochlorothiazide in managing patients with mild-to-moderate hypertension. Hypertens Res 2005; 28: 555-563.
Pan G, Zhou X, Zhao J. Effect of telmisartan on atrial fibrillation recurrences in patients with hypertension: a systematic review and meta-analysis. Cardiovasc Ther 2014; 32: 184-188.
Parati G, Bilo G, Redon J; SURGE Steering Committee. The effects of telmisartan alone or with hydrochlorothiazide on morning and 24-h ambulatory BP control: results from a practice-based study (SURGE 2). Hypertens Res 2013; 36: 322-327.
Prejbisz A, Januszewicz A. Antagoniści receptora angiotensyny II w terapii nadciśnienia tętniczego i chorób współistniejących. Medycyna Praktyczna, Kraków 2014.
Re RN. Mechanisms of disease: local renin-angiotensin-aldosterone systems and the pathogenesis and treatment of cardiovascular disease. Nat Clin Pract Cardiovasc Med 2004; 1: 42-47.
Schmieder RE, Delles C, Mimran A i wsp. Impact of telmisartan versus ramipril on renal endothelial function in patients with hypertension and type 2 diabetes. Diabetes Care 2007; 30: 1351-1356.
Sharma AM, Davidson J, Koval S, Lacourciere Y. Telmisartan/hydrochlorothiazide versus valsartan/hydrochlorothiazide in obese hypertensive patients with type 2 diabetes: the SMOOTH study. Cardiovasc Diabetol 2007; 6: 28.
Shiga Y, Miura S, Mitsutake R i wsp. Efficacy and safety of a single-pill fixed-dose combination of high-dose telmisartan/ hydrochlorothiazide in patients with uncontrolled hypertension. J Renin Angiotensin Aldosterone Syst 2012; 13: 394-400.
Takagi H, Umemoto T. A meta-analysis of randomized controlled trials of telmisartan for flow-mediated dilatation. Hypertens Res 2014; 37: 845-851.
Yusuf S, Teo KK, Pogue J i wsp.; The ONTARGET Investigators. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547-1559.
Tykarski A, Filipiak KJ, Januszewicz A i wsp. Zasady postępowania w nadciśnieniu tętniczym – 2019 rok. Wytyczne Polskiego Towarzystwa Nadciśnienia Tętniczego. Nadciśnienie Tętnicze w Praktyce 2019; 5: 1-84.
Unger T, Schölkens BA. Angiotensin. Vol. II. Springer-Verlag, Berlin Heidelberg 2004.
Wienen W, Enthzerod M, van Meel JCA i wsp. A review on telmisartan: a novel, long acting aniotensin II-receptor antagonist. Cardiovasc Drug Rev 2000; 18; 127-156.
Zhu DL, Bays H, Gao P i wsp. Efficacy and tolerability of initial therapy with single-pill combination telmisartan/hydrochlorothiazide 80/25 mg in patients with grade 2 or 3 hypertension: a multinational, randomized, double-blind, active-controlled trial. Clin Ther 2012; 34: 1613-1624.
Tekst opublikowano w „Kurierze Medycznym” 5/2021. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.