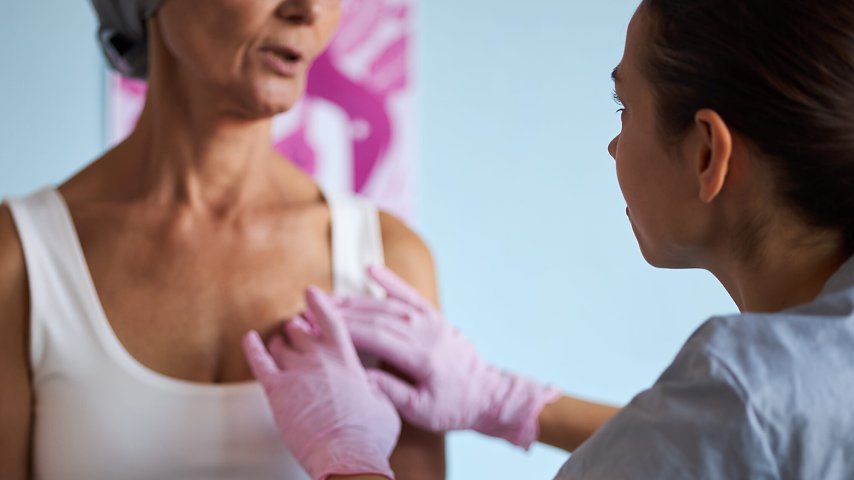
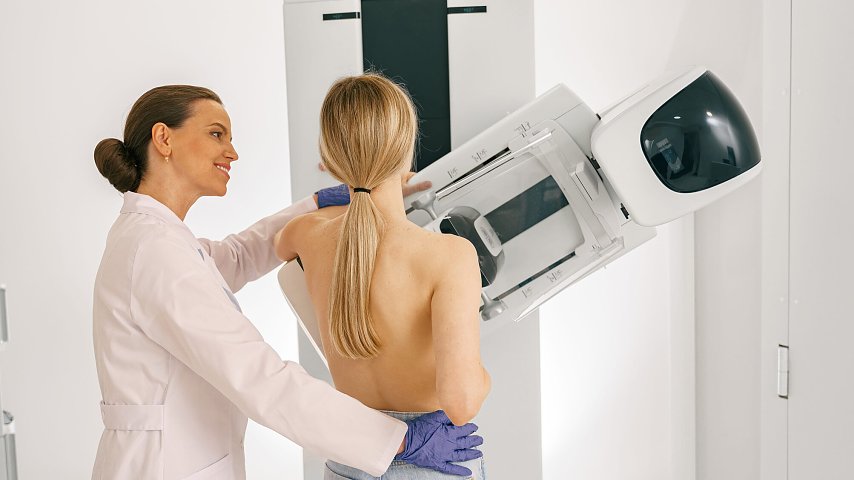
FDA zarejestrowałą lek skuteczny w biegunce w przebiegu rakowiaka
Amerykańska Agencja Żywności i Leków (ang. American Food and Drug Administration, FDA) zarejestrowała telotristat (Xermelo) w skojarzeniu z obecnym standardem terapii, jakim są analogi somatostatyny do leczenia chorych z biegunką w przebiegu zespołu rakowiaka nieodpowiadającą na leczenie samymi analogami somatostatyny.
Rakowiaki są rodzajem guzów neuroendokrynnych i rozwijają się często w przewodzie pokarmowym lub w płucach. U mniej niż 10% chorych z tymi nowotworami dochodzi do rozwoju zespołu rakowiaka, zwykle po rozsiewie do wątroby i zwiększeniu ilości wydzielanej serotoniny. Inne objawy zespołu rakowiaka obejmują uderzenia gorąca, zaczerwienienie twarzy, kołatania serca, astmę, rozszerzenie naczyń skórnych, zawroty głowy i zmęczenie. Lek zarejestrowano na podstawie kontrolowanego placebo badania klinicznego 3. fazy TELESTAR, do którego włączono 135 chorych z zespołem rakowiaka, u których stwierdzano co najmniej 4 wypróżnienia na dobę pomimo leczenia analogami somatostatyny. Chorych przydzielano losowo w stosunku 1:1:1 do grupy otrzymującej analogi somatostatyny w skojarzeniu z telotristatem w dawce 250 mg, sam telotristat w dawce 500 mg lub placebo 3 razy na dobę. Pierwszorzędowym punktem końcowym badania była zmiana ilości wypróżnień od rozpoczęcia badania. W Journal of Clinical Oncology opublikowano wyniki 12-tygodniowej podwójnie zaślepionej fazy badania oraz 36-tygodniowej otwartej fazy wydłużonej. W badaniu wykazano, że w porównaniu z placebo u chorych zakwalifikowanych do obu ramion z telotristatem doszło do statystycznie istotnego zmniejszenia średniej ilości wypróżnień na dobę. Obliczona różnica częstości wypróżnień w pierwszej, 12-tygodniowej fazie badania wyniosła -0,81 u chorych otrzymujących telotristat w dawce 250 mg (p < 0,001) oraz -0,69 u chorych otrzymujących telotristat w dawce 500 mg (p < 0,001). Odpowiedzi na leczenie zdefiniowane jako zmniejszenie częstości wypróżnień o co najmniej 30% w porównaniu z wartością początkową przez co najmniej połowę 12-tygodniowego okresu uzyskano u 20%, 44% i 42% odpowiednio w grupach otrzymujących placebo, telotristat w dawce 250 mg i telotristat w dawce 250 mg. Leczenie telotristatem było ogólnie dobrze tolerowane, a najczęstsze działania niepożądane obejmowały gorączkę, nudności, bóle głowy, depresję, obrzęki obwodowe, zwiększoną aktywność GGTP, zwiększoną ilość gazów w jelitach oraz zmniejszenie apetytu.