20.09.2022
Autor:
Aleksandra Lang
Pozytywna opinia w sprawie rozszerzenia wskazań tralokinumabu
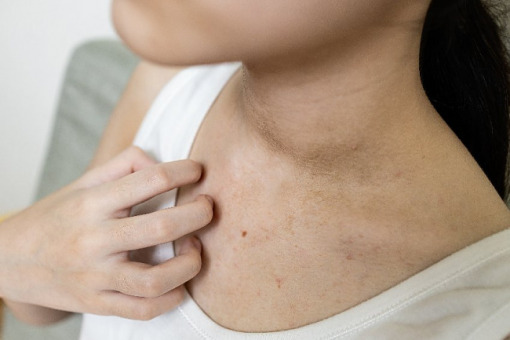
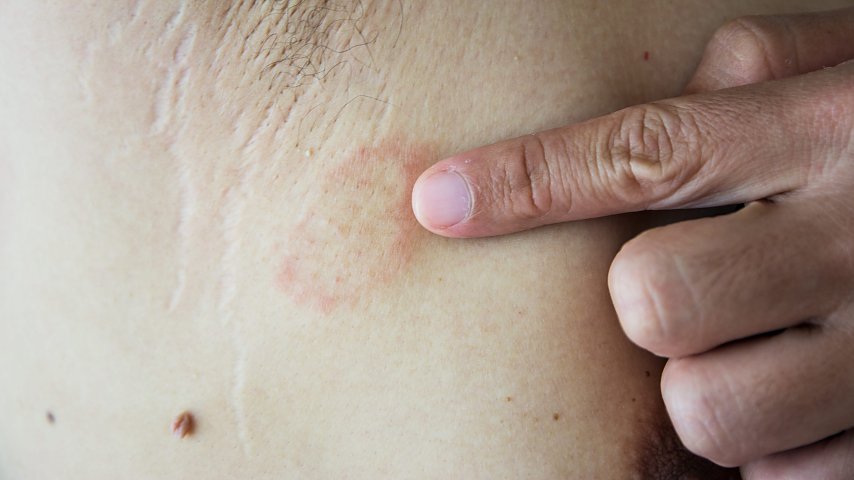
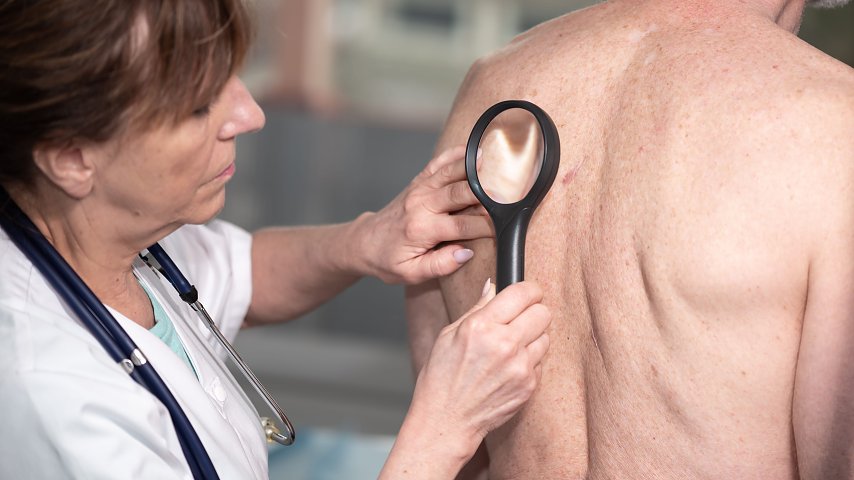
Tralokinumab został dopuszczony do stosowania u dorosłych z umiarkowanym lub ciężkim atopowym zapaleniem skóry w USA, w UE, Wielkiej Brytanii, Kanadzie, Zjednoczonych Emiratach Arabskich i Szwajcarii. W żadnym kraju nie jest jednak zatwierdzony do leczenia młodzieży.
Tralokinumab otrzymał pozytywną opinię Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) Europejskiej Agencji Leków dotyczącą rozszerzenia stosowania tego leku u nastolatków w wieku co najmniej 12 lat z atopowym zapaleniem skóry (AZS) umiarkowanym do ciężkiego.
Opinia CHMP została poparta danymi z badania fazy 3 (ECZTRA 6), w którym oceniano bezpieczeństwo i skuteczność tralokinumabu w dawkach 150 mg lub 300 mg w porównaniu z placebo u młodzieży z umiarkowaną do ciężkiej postaci AZS. Pierwszorzędowymi wynikami były Investigator Global Assessment dla czystej lub prawie czystej skóry (IGA 0/1) oraz poprawa o co najmniej 75 proc. w wyniku Eczema Area and Severity Index (EASI-75). W badaniu, przedstawionym jako plakat na spotkaniu w październiku zeszłego roku, 195 nastolatków w wieku 12-17 lat z AZS o nasileniu umiarkowanym do ciężkiego, kwalifikujących się do leczenia systemowego, zostało losowo przydzielonych do tralokinumabu, a 94 do placebo.
Zdarzenia niepożądane były podobne między grupami, a większość z nich była łagodna lub umiarkowana; ogólne profile bezpieczeństwa były podobne do tych obserwowanych u dorosłych pacjentów.
Komisja Europejska (KE) dokona przeglądu pozytywnej opinii i podejmie ostateczną decyzję.
Opinia CHMP została poparta danymi z badania fazy 3 (ECZTRA 6), w którym oceniano bezpieczeństwo i skuteczność tralokinumabu w dawkach 150 mg lub 300 mg w porównaniu z placebo u młodzieży z umiarkowaną do ciężkiej postaci AZS. Pierwszorzędowymi wynikami były Investigator Global Assessment dla czystej lub prawie czystej skóry (IGA 0/1) oraz poprawa o co najmniej 75 proc. w wyniku Eczema Area and Severity Index (EASI-75). W badaniu, przedstawionym jako plakat na spotkaniu w październiku zeszłego roku, 195 nastolatków w wieku 12-17 lat z AZS o nasileniu umiarkowanym do ciężkiego, kwalifikujących się do leczenia systemowego, zostało losowo przydzielonych do tralokinumabu, a 94 do placebo.
Zdarzenia niepożądane były podobne między grupami, a większość z nich była łagodna lub umiarkowana; ogólne profile bezpieczeństwa były podobne do tych obserwowanych u dorosłych pacjentów.
Komisja Europejska (KE) dokona przeglądu pozytywnej opinii i podejmie ostateczną decyzję.