Leki miorelaksujące w praktyce klinicznej – dlaczego niezbędna jest indywidualizacja wyboru
Leki miorelaksujące należą do podstawowych grup leków stosowanych w bólu krzyża, rwie kulszowej, kręczu karku i w spastyczności poudarowej. Skuteczna terapia musi się opierać na spersonalizowanym doborze leku z uwzględnieniem cech pacjenta i cech procesu patologicznego, który doprowadza do wzmożonego napięcia mięśni.
Autor: Jarosław Woroń
Wstęp
Leki miorelaksujące należą do podstawowych grup leków stosowanych w bólu krzyża, rwie kulszowej kręczu karku, a także spastyczności poudarowej. Skuteczna terapia musi się opierać na spersonalizowanym doborze leku z uwzględnieniem zarówno cech pacjenta, jak i cech procesu patologicznego, który doprowadza do wzmożonego napięcia mięśni. Jak wynika z praktyki klinicznej, leki miorelaksujące są stosowane głównie w zespołach bólowych dolnego odcinka kręgosłupa. Właśnie w tym wskazaniu najczęściej występują błędy w wyborze leków miorelaksujących, co sprawia, że ten aspekt ich zastosowania wymaga szczególnej uwagi.
Ból krzyża to ból odcinka lędźwiowo-krzyżowego kręgosłupa zlokalizowany pomiędzy 12. żebrem a dolnymi fałdami pośladkowymi, któremu może towarzyszyć ból kończyn dolnych. Ból krzyża nie jest odrębną jednostką chorobową, lecz zespołem objawów [1–7].
Objawy ostrego bólu krzyża
Ostry ból krzyża charakteryzuje się następującymi cechami:
• pojawia się nagle, po wysiłku związanym z dźwignięciem, gwałtownym ruchem czy zwykłą czynnością codzienną,
• ma różny charakter i nasilenie, najczęściej jest tępy, zaczyna się w okolicy lędźwiowej i promieniuje wzdłuż kończyny do okolic kolana,
• może promieniować (zwykle jednostronnie) wzdłuż korzenia nerwu rdzeniowego,
• zmniejsza się w nocy – pozostawanie w łóżku zwyczaj łagodzi dolegliwości,
• nasila się podczas chodzenia.
W przypadku ostrego zespołu bólowego obserwuje się:
• boczne skrzywienie kręgosłupa w odcinku lędźwiowym, skierowane wypukłością w zdrową stronę,
• znaczne spłaszczenie lordozy lędźwiowej,
• skurcz mięśni przykręgosłupowych,
• ograniczenie ruchomości kręgosłupa.
Przyczyną bocznego skrzywienia kręgosłupa i wygładzenia lordozy jest pozycja odruchowa, którą chory przybiera w ucieczce przed bólem, odbarczając uciśnięty korzeń [1, 8, 9].
Podstawowym celem leczenia na etapie początkowym jest zabezpieczenie pacjenta przed chronifikacją dolegliwości. Jednym z elementów leczenia farmakologicznego jest prawidłowy wybór leków miorelaksujących i odpowiednie ich dawkowanie.
Wzmożone napięcie mięśniowe u pacjentów z zespołami bólowymi dolnego odcinka kręgosłupa często uruchamia błędne koło: ból – wzmożone napięcie mięśniowe – ból. Co więcej, może w konsekwencji doprowadzać do przykurczów utrudniających przebieg ruchu dowolnego, co w praktyce stanowi poważny problem u chorych z uszkodzeniem układu piramidowego na poziomie mózgu i rdzenia kręgowego. W leczeniu tych chorych istotną rolę odgrywają leki miorelaksujące. Są to produkty lecznicze o różnej budowie chemicznej i różnych mechanizmach działania farmakologicznego. Warto przypomnieć, że wykazują one synergizm działania w bólu krzyża z niesteroidowymi lekami przeciwzapalnymi (NLPZ), metamizolem oraz analgetykami opioidowymi [1, 2, 4, 10, 11, 12]. Najmniej efektywnie działają w skojarzeniu z paracetamolem, który nie jest aktualnie zalecany w bólu krzyża z uwagi na patomechanizm jego powstawania. Warto przypomnieć, że wybór leku miorelaksującego musi być zindywidualizowany w zależności od:
• cech pacjenta,
• charakterystyki zespołu bólowego z towarzyszącym wzmożonym napięciem mięśniowym,
• chorób współwystępujących,
• innych jednocześnie stosowanych leków,
• ewentualnych przeciwwskazań do stosowania leków miorelaksujących [1, 2, 12].
Należy uwzględnić mechanizm działania poszczególnych leków, aby uzyskać wysoką skuteczność i zmniejszyć ryzyko wystąpienia powikłań. Aktualnie na polskim rynku farmaceutycznym jest dostępnych pięć leków o działaniu miorelaksującym, które nie są wzajemnie wprost zastępowalne z uwagi na ich mechanizmy działania [1, 2, 4, 8, 10, 12, 13].
Baklofen
Baklofen jest strukturalnym analogiem kwasu gamma-aminomasłowego (GABA). Wykazuje działanie agonistyczne w stosunku do pre- i postsynaptycznych, metabotropowych receptorów GABAB oraz postsynaptycznych receptorów jonotropowych GABAA. Wpływa hamująco na przewodnictwo w strukturach ośrodkowego układu nerwowego (OUN), hamując uwalnianie neurotransmiterów do szczeliny synaptycznej poprzez działanie na receptor GABAB, a także zmniejszając pobudliwość postsynapsy poprzez działanie na receptory GABAA i GABAB. Baklofen jest stosowany w zespołach bólowych dolnego odcinka kręgosłupa, stwardnieniu rozsianym, stwardnieniu zanikowym bocznym, późnej dystonii, spastyczności po urazach mózgu i rdzenia kręgowego, w tężcu, zespole sztywności uogólnionej. Niepożądane działanie baklofenu wynika z jego wpływu na struktury OUN, gdzie znajdują się także receptory GABA. W wyniku tej interakcji mogą się pojawić objawy niepożądane w postaci sedacji, senności lub bezsenności, zawrotów głowy, osłabienia, męczliwości, nudności oraz obniżenia progu drgawkowego. To ostatnie działanie jest szczególnie istotne w sytuacji, gdy pacjent jednocześnie stosuje inne leki obniżające próg drgawkowy [1, 2, 12]. W tabeli 1 wymieniono leki, które mogą powodować obniżenie progu drgawkowego i działać prodrgawkowo.

Metokarbamol
Metokarbamol jest estrem kwasu karbaminowego, a także pochodną znanego leku o działaniu wykrztuśnym i miorelaksacyjnym – gwajfenazyny. Wykazuje ośrodkowy efekt miorelaksujący. Lek jest dostępny na rynku od wielu lat, ale nadal nie znamy jego molekularnego mechanizmu działania. Mechanizm działania metokarbamolu jest związany z hamowaniem transmisji synaptycznej w różnych strukturach OUN. Uważa się, że lek ten wybiórczo hamuje wielosynaptyczne odruchy rdzeniowe. Dotyczy to szczególnie aktywności alfa-motoneuronów rdzenia kręgowego, w wyniku czego pojawia się działanie zmniejszające napięcie mięśni szkieletowych. Jest skuteczny głównie w terapii bolesnych skurczów mięśni szkieletowych i w związku z tym stosuje się go w licznych schorzeniach narządu ruchu. Metokarbamol jest wykorzystywany głównie w terapii zespołów bólowych kręgosłupa, zwłaszcza odcinka lędźwiowo-krzyżowego. Wykazuje także skuteczność w leczeniu spastyczności w przebiegu mózgowego porażenia dziecięcego. Zmniejsza dolegliwości bólowe związane ze skurczami mięśni szkieletowych oraz umożliwia skrócenie okresu rehabilitacji chorych po zabiegach chirurgicznych. Skuteczność metokarbamolu potwierdzono także w przypadku chirurgicznego zabiegu wymiany stawu kolanowego. Metokarbamol rzadziej niż baklofen powoduje senność, sedację, dezorientację i zawroty głowy. Do najczęściej występujących działań niepożądanych metokarbamolu należą: osłabienie siły mięśniowej, zaburzenia orientacji oraz czarne, brązowe lub zielone zabarwienie moczu [1, 2, 12].
Tizanidyna
Tizanidyna jest strukturalnie podobna do klonidyny. Zarówno klonidyna, jak i tizanidyna są pochodnymi imidazolinowymi i agonistami receptorów 2-adrenergicznych. Tizanidyna podobnie jak baklofen wykazuje działanie ośrodkowe, natomiast nie ma bezpośredniego wpływu na włókna mięśni szkieletowych. Efekt terapeutyczny tizanidyny jest skorelowany z działaniem agonistycznym na receptory imidazolinowe w strukturach ponadrdzeniowych. Z uwagi na fakt, że tizanidyna działa agonistycznie w stosunku do presynaptycznych receptorów alfa2, wywoluje także efekt analgetyczny. Agonizm w stosunku do receptora 2 powoduje zahamowanie uwalniania do szczeliny synaptycznej czynników probólowych. W praktyce lek wykorzystuje się w objawowym leczeniu wzmożonego napięcia mięśni m.in. w stwardnieniu rozsianym, porażeniu mózgowym i w zespole sztywności uogólnionej, a także w zespołach bólowych dolnego odcinka kręgosłupa. Z uwagi na obecność receptorów alfa2-adrenergicznych, które występują nie tylko w rdzeniu kręgowym, tizanidyna może powodować spadki ciśnienia tętniczego, senność, sedację, suchość w jamie ustnej, zawroty głowy, nudności oraz halucynacje, aczkolwiek zdarza się to rzadko. Może także wydłużać odstęp QTc w zapisie EKG, co jest szczególnie istotne u pacjentów stosujących politerapię z użyciem innych leków potencjalnie torsadogennych. Warto przypomnieć, że skojarzenie tizanidyny z NLPZ zmniejsza ryzyko wystąpienia gastropatii, co nie jest bez znaczenia w farmakoterapii bólu [1, 2, 4, 8, 12, 13].
Korzyści ze stosowania tizanidyny obejmują duży zakres wskazań klinicznych. Szerokie spektrum efektów farmakologicznych zapewnia mechanizm działania, który nie wynika jedynie z wpływu miorelaksującego, ale obejmuje równocześnie efekt przeciwbólowy realizowany w sposób pozwalający na osiągnięcie synergizmu z innymi analgetykami w skojarzonej terapii bólu.
Tiokolchikozyd
Tiokolchikozyd jest półsyntetyczną siarkową pochodną kolchicyny, glikozydu uzyskiwanego z roślin z rodziny zimowitowatych. Tiokolchikozyd ma przede wszystkim właściwości miorelaksujące. Mechanizm działania leku jest związany z pobudzaniem hamujących receptorów Gly (glicynowych) i GABAA w OUN. Wykazuje także działanie przeciwbólowe oraz właściwości przeciwzapalne, co jest szczególnie istotne w przypadku leczenia zespołów bólowych kręgosłupa. Być może przeciwzapalny wpływ tiokolchikozydu jest związany z właściwościami macierzystego związku, jakim jest kolchicyna. Po podaniu doustnym lek jest metabolizowany w jelitach. Stwierdzane są jego dwa metabolity: farmakologicznie czynny SL (M1) i nieaktywny SL (M2). W przypadku obu związków maksymalne stężenie w osoczu krwi występuje po 1 godzinie od podania leku. Po podaniu doustnym wydalanie tiokolchikozydu odbywa się w 79% z kałem i w 20% z moczem, a okres półtrwania aktywnego metabolitu M1 wynosi 3,2–7,0 godzin. Tiokolchikozyd jest stosowany jest w leczeniu wspomagającym bolesnych przykurczów mięśni w ostrych chorobach kręgosłupa u dorosłych i młodzieży od 16. roku życia. Zalecana i jednocześnie maksymalna dawka to 8 mg co 12 godzin. Czas leczenia jest ograniczony do 7 kolejnych dni. Leku nie należy stosować u pacjentów z nadwrażliwością na substancję czynną, w okresie ciąży i karmienia piersią oraz u kobiet w wieku rozrodczym, które nie stosują skutecznej antykoncepcji [1, 2, 12].
Tolperyzon
Tolperyzon może być stosowany wyłącznie w spastyczności poudarowej, co wprost wynika z mechanizmu działania farmakologicznego. W żadnym wypadku nie może być przyjmowany z powodu zespołów bólowych kręgosłupa. Warto także przypomnieć o możliwych działaniach niepożądanych, w tym o ciężkich powikłaniach dermatologicznych, które stały się podstawą wygenerowania dla leku komunikatu bezpieczeństwa [1, 2]. Jednym z istotnych błędów w zakresie stosowania tolperyzonu jest lekceważenie ryzyka interakcji z innymi jednocześnie stosowanymi lekami. Tolperyzon jest inhibitorem izoenzymu 2D6 cytochormu P450, a zatem indukuje interakcje farmakokinetyczne z wieloma lekami. W tabeli 2 zebrano najczęściej stosowane leki, z którymi tolperyzon wchodzi w istotne klinicznie interakcje.

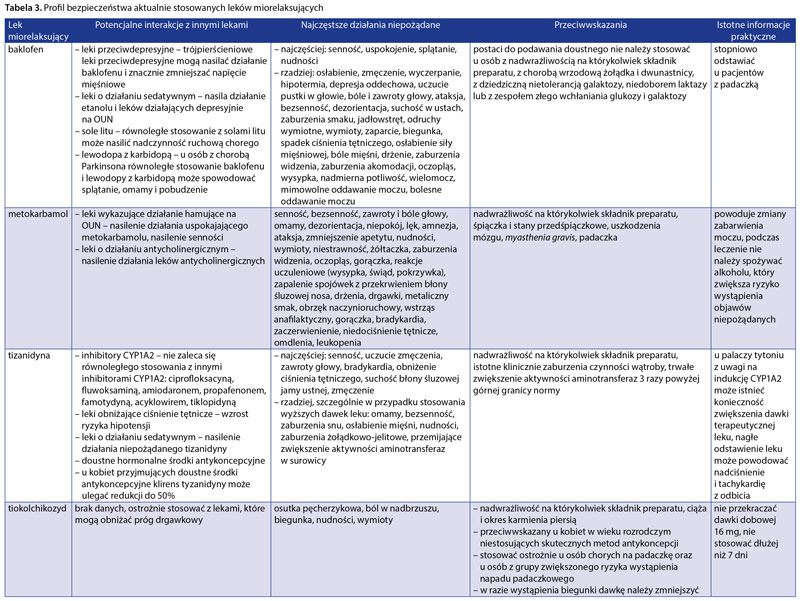
Ważnymi czynnikami decydującymi o wyborze leku miorelaksującego oprócz wskazań są również profil bezpieczeństwa oraz interakcje z innymi lekami. W tabeli 3 zebrano najistotniejsze dane dotyczące profilu bezpieczeństwa aktualnie stosowanych leków miorelaksujących [12].
Prydynol
Mechanizm działania prydynolu wynika z jego wpływu antycholinergicznego zarówno obwodowego, jak i ośrodkowego. Lek usuwa nadmierne napięcie i drżenie mięśni szkieletowych, hamuje występowanie ruchów mimowolnych, wykazuje również działanie zwiotczające mięśnie. Oddziałuje depresyjnie na układ pozapiramidowy, hamuje ruchy mimowolne. Wpływa także na mięśniówkę gładką. Z uwagi na mechanizm działania prydynol nie powinien być stosowany u pacjentów z nadmierną spastycznością, u których współwystępują dolegliwości bólowe. W tej grupie pacjentów oprócz leków miorelaksujących stosowane są jednocześnie analgetyki, w tym NLPZ. Z uwagi na fakt, że jednym z mechanizmów przeciwbólowego działania NLPZ jest aktywacja nadrdzeniowych szklaków cholinergicznych, jednoczesne stosowanie prydynolu, który wykazuje ośrodkowe działanie antycholinergiczne, prowadzi do osłabienia wpływu analgetycznego NLPZ [14]. Co więcej, aktualnie uznaje się, że u pacjentów z dolegliwościami bólowymi nie należy stosować jakichkolwiek leków działających antycholinergicznie ośrodkowo z uwagi na możliwość braku optymalnej kontroli bólu [14]. Do leków, których stosowania należy unikać, zaliczamy neuroleptyki fenotiazynowe, hydroksyzynę, difenhydraminę, doksylaminę. Mechanizm farmakologicznego działania prydynolu nie jest kompatybilny z mechanizmem powstawania spastyczności w zespołach bólowych zlokalizowanych w narządzie ruchu. Wskazania do stosowania prydynolu obejmują: chorobę Parkinsona (jako leczenie wspomagające we wszystkich postaciach parkinsonizmu), zespoły spastyczne pochodzenia ośrodkowego i obwodowego (w tym zespoły indukowane przez leki), leczenie i zapobieganie nocnym skurczom mięśni (wspomagająco) oraz objawowe leczenie ślinotoku w przebiegu różnych schorzeń (z uwagi na efekt cholinolityczny). Nie należy kojarzyć prydynolu z innymi lekami o działaniu antycholinergicznym. Takie skojarzenie zwiększa ryzyko wystąpienia powikłań. Nie powinno się go stosować jednocześnie z amantadyną. Metoklopramid zmniejsza niepożądany wpływ prydynolu na perystaltykę przewodu pokarmowego, jednak metoklopramidu nie można stosować dłużej niż 5 dni.
Podsumowanie
Warto pamiętać, że stosowanie leków miorelaksujących wiąże się z ryzykiem ograniczenia sprawności psychofizycznej, jednak ryzyko to musi być oceniane indywidualnie.
Dawkowanie w praktyce powinno być indywidualizowane w zależności od wskazań i specyfiki leczonego pacjenta. Czynniki, które należy uwzględnić podczas wyboru leku miorelaksującego, zebrano w tabeli 4.

Skuteczność i bezpieczeństwo stosowania leków miorelaksujących muszą być rozpatrywane indywidualnie. Indywidualizacja wyboru leku miorelaksującego jest jednym z najistotniejszych czynników wpływających na uzyskanie skuteczności terapeutycznej i zmniejszenie ryzyka wystąpienia objawów niepożądanych.
Piśmiennictwo
1. Malec-Milewska M, Woroń J (red.). Kompendium leczenia bólu. Medical Education, Warszawa 2017.
2. Woroń J. Chory na nowotwór. Interakcje analgetyków i leków stosowanych w terapii objawów współtowarzyszących. Medical Education, Warszawa 2019.
3. Airaksinen O, Brox JI, Cedraschi C i wsp. Chapter 4 European guidelines for the management of chronic nonspecific low back pain. Eur Spine J 2006; 15 (Suppl. 2): S192-S300.
4. Brzeziński K. Niespecyficzny ból krzyża (medycyna oparta na faktach). Ból 2011; 12: 19-26.
5. Chou R, Qaseem A, Snow V i wsp. Rozpoznawanie i leczenie bólu krzyża. Wytyczne American College of Physicians i American Pain Society. Med Prakt 2008; 2: 92-119.
6. Sękowska A, Malec-Milewska M, Kolęda I. Bóle krzyża w praktyce lekarza rodzinnego. Klinika Nowa 2011;
5 (numer zjazdowy).
7. van Tulder M, Koes B. Chronic low back pain. W: Evidence-Based Chronic Pain Management. Stannard C,
Kalso E, Ballantyne J. Wiley-Blackwell 2010.
8. Koes BW, van Tulder M, Lin CW i wsp. An updated overview of clinical guidelines for the management of non-specific low back pain in primary care. Eur Spine J 2010; 19: 2075-2094.
9. Stannard C, Kalso E, Ballantyne J. Evidence-Based Chronic Pain Management. Blackwell Publishing 2010.
10. Macfarlane GJ, Jones GT, Hannaford PC. Managing low back pain presenting to primary care: where do we go from here? Pain 2006; 122: 219-222.
11. Kolęda I, Malec-Milewska M. Pacjent z przewlekłym bólem – diagnozowanie, leczenie, wytyczne. Praktyka Lekarska 2010; 11: 15-16.
12. Martindale. The Complete Drug Reference. Pharmaceutical Press, London 2020.
13. Istrati J, Kocot-Krępska M, Gadek A. Zespoły bólowe narządu ruchu – leczenie. Terapia 2010; 11-12: 27-34.
14. Woroń J, Siwek M, Wordliczek J, Kutaj-Wąsikowska H. Farmakoterapia bólu u pacjenta leczonego lekami psychotropowymi – dlaczego należy zachować ostrożność? Ból 2017; 18: 22-28.
Pełna treść artykułu: Jarosław Woroń. Leki miorelaksujące w praktyce klinicznej – dlaczego niezbędna jest indywidualizacja wyboru. Lekarz POZ 2021; 4: 301-306.
Wstęp
Leki miorelaksujące należą do podstawowych grup leków stosowanych w bólu krzyża, rwie kulszowej kręczu karku, a także spastyczności poudarowej. Skuteczna terapia musi się opierać na spersonalizowanym doborze leku z uwzględnieniem zarówno cech pacjenta, jak i cech procesu patologicznego, który doprowadza do wzmożonego napięcia mięśni. Jak wynika z praktyki klinicznej, leki miorelaksujące są stosowane głównie w zespołach bólowych dolnego odcinka kręgosłupa. Właśnie w tym wskazaniu najczęściej występują błędy w wyborze leków miorelaksujących, co sprawia, że ten aspekt ich zastosowania wymaga szczególnej uwagi.
Ból krzyża to ból odcinka lędźwiowo-krzyżowego kręgosłupa zlokalizowany pomiędzy 12. żebrem a dolnymi fałdami pośladkowymi, któremu może towarzyszyć ból kończyn dolnych. Ból krzyża nie jest odrębną jednostką chorobową, lecz zespołem objawów [1–7].
Objawy ostrego bólu krzyża
Ostry ból krzyża charakteryzuje się następującymi cechami:
• pojawia się nagle, po wysiłku związanym z dźwignięciem, gwałtownym ruchem czy zwykłą czynnością codzienną,
• ma różny charakter i nasilenie, najczęściej jest tępy, zaczyna się w okolicy lędźwiowej i promieniuje wzdłuż kończyny do okolic kolana,
• może promieniować (zwykle jednostronnie) wzdłuż korzenia nerwu rdzeniowego,
• zmniejsza się w nocy – pozostawanie w łóżku zwyczaj łagodzi dolegliwości,
• nasila się podczas chodzenia.
W przypadku ostrego zespołu bólowego obserwuje się:
• boczne skrzywienie kręgosłupa w odcinku lędźwiowym, skierowane wypukłością w zdrową stronę,
• znaczne spłaszczenie lordozy lędźwiowej,
• skurcz mięśni przykręgosłupowych,
• ograniczenie ruchomości kręgosłupa.
Przyczyną bocznego skrzywienia kręgosłupa i wygładzenia lordozy jest pozycja odruchowa, którą chory przybiera w ucieczce przed bólem, odbarczając uciśnięty korzeń [1, 8, 9].
Podstawowym celem leczenia na etapie początkowym jest zabezpieczenie pacjenta przed chronifikacją dolegliwości. Jednym z elementów leczenia farmakologicznego jest prawidłowy wybór leków miorelaksujących i odpowiednie ich dawkowanie.
Wzmożone napięcie mięśniowe u pacjentów z zespołami bólowymi dolnego odcinka kręgosłupa często uruchamia błędne koło: ból – wzmożone napięcie mięśniowe – ból. Co więcej, może w konsekwencji doprowadzać do przykurczów utrudniających przebieg ruchu dowolnego, co w praktyce stanowi poważny problem u chorych z uszkodzeniem układu piramidowego na poziomie mózgu i rdzenia kręgowego. W leczeniu tych chorych istotną rolę odgrywają leki miorelaksujące. Są to produkty lecznicze o różnej budowie chemicznej i różnych mechanizmach działania farmakologicznego. Warto przypomnieć, że wykazują one synergizm działania w bólu krzyża z niesteroidowymi lekami przeciwzapalnymi (NLPZ), metamizolem oraz analgetykami opioidowymi [1, 2, 4, 10, 11, 12]. Najmniej efektywnie działają w skojarzeniu z paracetamolem, który nie jest aktualnie zalecany w bólu krzyża z uwagi na patomechanizm jego powstawania. Warto przypomnieć, że wybór leku miorelaksującego musi być zindywidualizowany w zależności od:
• cech pacjenta,
• charakterystyki zespołu bólowego z towarzyszącym wzmożonym napięciem mięśniowym,
• chorób współwystępujących,
• innych jednocześnie stosowanych leków,
• ewentualnych przeciwwskazań do stosowania leków miorelaksujących [1, 2, 12].
Należy uwzględnić mechanizm działania poszczególnych leków, aby uzyskać wysoką skuteczność i zmniejszyć ryzyko wystąpienia powikłań. Aktualnie na polskim rynku farmaceutycznym jest dostępnych pięć leków o działaniu miorelaksującym, które nie są wzajemnie wprost zastępowalne z uwagi na ich mechanizmy działania [1, 2, 4, 8, 10, 12, 13].
Baklofen
Baklofen jest strukturalnym analogiem kwasu gamma-aminomasłowego (GABA). Wykazuje działanie agonistyczne w stosunku do pre- i postsynaptycznych, metabotropowych receptorów GABAB oraz postsynaptycznych receptorów jonotropowych GABAA. Wpływa hamująco na przewodnictwo w strukturach ośrodkowego układu nerwowego (OUN), hamując uwalnianie neurotransmiterów do szczeliny synaptycznej poprzez działanie na receptor GABAB, a także zmniejszając pobudliwość postsynapsy poprzez działanie na receptory GABAA i GABAB. Baklofen jest stosowany w zespołach bólowych dolnego odcinka kręgosłupa, stwardnieniu rozsianym, stwardnieniu zanikowym bocznym, późnej dystonii, spastyczności po urazach mózgu i rdzenia kręgowego, w tężcu, zespole sztywności uogólnionej. Niepożądane działanie baklofenu wynika z jego wpływu na struktury OUN, gdzie znajdują się także receptory GABA. W wyniku tej interakcji mogą się pojawić objawy niepożądane w postaci sedacji, senności lub bezsenności, zawrotów głowy, osłabienia, męczliwości, nudności oraz obniżenia progu drgawkowego. To ostatnie działanie jest szczególnie istotne w sytuacji, gdy pacjent jednocześnie stosuje inne leki obniżające próg drgawkowy [1, 2, 12]. W tabeli 1 wymieniono leki, które mogą powodować obniżenie progu drgawkowego i działać prodrgawkowo.

Metokarbamol
Metokarbamol jest estrem kwasu karbaminowego, a także pochodną znanego leku o działaniu wykrztuśnym i miorelaksacyjnym – gwajfenazyny. Wykazuje ośrodkowy efekt miorelaksujący. Lek jest dostępny na rynku od wielu lat, ale nadal nie znamy jego molekularnego mechanizmu działania. Mechanizm działania metokarbamolu jest związany z hamowaniem transmisji synaptycznej w różnych strukturach OUN. Uważa się, że lek ten wybiórczo hamuje wielosynaptyczne odruchy rdzeniowe. Dotyczy to szczególnie aktywności alfa-motoneuronów rdzenia kręgowego, w wyniku czego pojawia się działanie zmniejszające napięcie mięśni szkieletowych. Jest skuteczny głównie w terapii bolesnych skurczów mięśni szkieletowych i w związku z tym stosuje się go w licznych schorzeniach narządu ruchu. Metokarbamol jest wykorzystywany głównie w terapii zespołów bólowych kręgosłupa, zwłaszcza odcinka lędźwiowo-krzyżowego. Wykazuje także skuteczność w leczeniu spastyczności w przebiegu mózgowego porażenia dziecięcego. Zmniejsza dolegliwości bólowe związane ze skurczami mięśni szkieletowych oraz umożliwia skrócenie okresu rehabilitacji chorych po zabiegach chirurgicznych. Skuteczność metokarbamolu potwierdzono także w przypadku chirurgicznego zabiegu wymiany stawu kolanowego. Metokarbamol rzadziej niż baklofen powoduje senność, sedację, dezorientację i zawroty głowy. Do najczęściej występujących działań niepożądanych metokarbamolu należą: osłabienie siły mięśniowej, zaburzenia orientacji oraz czarne, brązowe lub zielone zabarwienie moczu [1, 2, 12].
Tizanidyna
Tizanidyna jest strukturalnie podobna do klonidyny. Zarówno klonidyna, jak i tizanidyna są pochodnymi imidazolinowymi i agonistami receptorów 2-adrenergicznych. Tizanidyna podobnie jak baklofen wykazuje działanie ośrodkowe, natomiast nie ma bezpośredniego wpływu na włókna mięśni szkieletowych. Efekt terapeutyczny tizanidyny jest skorelowany z działaniem agonistycznym na receptory imidazolinowe w strukturach ponadrdzeniowych. Z uwagi na fakt, że tizanidyna działa agonistycznie w stosunku do presynaptycznych receptorów alfa2, wywoluje także efekt analgetyczny. Agonizm w stosunku do receptora 2 powoduje zahamowanie uwalniania do szczeliny synaptycznej czynników probólowych. W praktyce lek wykorzystuje się w objawowym leczeniu wzmożonego napięcia mięśni m.in. w stwardnieniu rozsianym, porażeniu mózgowym i w zespole sztywności uogólnionej, a także w zespołach bólowych dolnego odcinka kręgosłupa. Z uwagi na obecność receptorów alfa2-adrenergicznych, które występują nie tylko w rdzeniu kręgowym, tizanidyna może powodować spadki ciśnienia tętniczego, senność, sedację, suchość w jamie ustnej, zawroty głowy, nudności oraz halucynacje, aczkolwiek zdarza się to rzadko. Może także wydłużać odstęp QTc w zapisie EKG, co jest szczególnie istotne u pacjentów stosujących politerapię z użyciem innych leków potencjalnie torsadogennych. Warto przypomnieć, że skojarzenie tizanidyny z NLPZ zmniejsza ryzyko wystąpienia gastropatii, co nie jest bez znaczenia w farmakoterapii bólu [1, 2, 4, 8, 12, 13].
Korzyści ze stosowania tizanidyny obejmują duży zakres wskazań klinicznych. Szerokie spektrum efektów farmakologicznych zapewnia mechanizm działania, który nie wynika jedynie z wpływu miorelaksującego, ale obejmuje równocześnie efekt przeciwbólowy realizowany w sposób pozwalający na osiągnięcie synergizmu z innymi analgetykami w skojarzonej terapii bólu.
Tiokolchikozyd
Tiokolchikozyd jest półsyntetyczną siarkową pochodną kolchicyny, glikozydu uzyskiwanego z roślin z rodziny zimowitowatych. Tiokolchikozyd ma przede wszystkim właściwości miorelaksujące. Mechanizm działania leku jest związany z pobudzaniem hamujących receptorów Gly (glicynowych) i GABAA w OUN. Wykazuje także działanie przeciwbólowe oraz właściwości przeciwzapalne, co jest szczególnie istotne w przypadku leczenia zespołów bólowych kręgosłupa. Być może przeciwzapalny wpływ tiokolchikozydu jest związany z właściwościami macierzystego związku, jakim jest kolchicyna. Po podaniu doustnym lek jest metabolizowany w jelitach. Stwierdzane są jego dwa metabolity: farmakologicznie czynny SL (M1) i nieaktywny SL (M2). W przypadku obu związków maksymalne stężenie w osoczu krwi występuje po 1 godzinie od podania leku. Po podaniu doustnym wydalanie tiokolchikozydu odbywa się w 79% z kałem i w 20% z moczem, a okres półtrwania aktywnego metabolitu M1 wynosi 3,2–7,0 godzin. Tiokolchikozyd jest stosowany jest w leczeniu wspomagającym bolesnych przykurczów mięśni w ostrych chorobach kręgosłupa u dorosłych i młodzieży od 16. roku życia. Zalecana i jednocześnie maksymalna dawka to 8 mg co 12 godzin. Czas leczenia jest ograniczony do 7 kolejnych dni. Leku nie należy stosować u pacjentów z nadwrażliwością na substancję czynną, w okresie ciąży i karmienia piersią oraz u kobiet w wieku rozrodczym, które nie stosują skutecznej antykoncepcji [1, 2, 12].
Tolperyzon
Tolperyzon może być stosowany wyłącznie w spastyczności poudarowej, co wprost wynika z mechanizmu działania farmakologicznego. W żadnym wypadku nie może być przyjmowany z powodu zespołów bólowych kręgosłupa. Warto także przypomnieć o możliwych działaniach niepożądanych, w tym o ciężkich powikłaniach dermatologicznych, które stały się podstawą wygenerowania dla leku komunikatu bezpieczeństwa [1, 2]. Jednym z istotnych błędów w zakresie stosowania tolperyzonu jest lekceważenie ryzyka interakcji z innymi jednocześnie stosowanymi lekami. Tolperyzon jest inhibitorem izoenzymu 2D6 cytochormu P450, a zatem indukuje interakcje farmakokinetyczne z wieloma lekami. W tabeli 2 zebrano najczęściej stosowane leki, z którymi tolperyzon wchodzi w istotne klinicznie interakcje.

Ważnymi czynnikami decydującymi o wyborze leku miorelaksującego oprócz wskazań są również profil bezpieczeństwa oraz interakcje z innymi lekami. W tabeli 3 zebrano najistotniejsze dane dotyczące profilu bezpieczeństwa aktualnie stosowanych leków miorelaksujących [12].

Prydynol
Mechanizm działania prydynolu wynika z jego wpływu antycholinergicznego zarówno obwodowego, jak i ośrodkowego. Lek usuwa nadmierne napięcie i drżenie mięśni szkieletowych, hamuje występowanie ruchów mimowolnych, wykazuje również działanie zwiotczające mięśnie. Oddziałuje depresyjnie na układ pozapiramidowy, hamuje ruchy mimowolne. Wpływa także na mięśniówkę gładką. Z uwagi na mechanizm działania prydynol nie powinien być stosowany u pacjentów z nadmierną spastycznością, u których współwystępują dolegliwości bólowe. W tej grupie pacjentów oprócz leków miorelaksujących stosowane są jednocześnie analgetyki, w tym NLPZ. Z uwagi na fakt, że jednym z mechanizmów przeciwbólowego działania NLPZ jest aktywacja nadrdzeniowych szklaków cholinergicznych, jednoczesne stosowanie prydynolu, który wykazuje ośrodkowe działanie antycholinergiczne, prowadzi do osłabienia wpływu analgetycznego NLPZ [14]. Co więcej, aktualnie uznaje się, że u pacjentów z dolegliwościami bólowymi nie należy stosować jakichkolwiek leków działających antycholinergicznie ośrodkowo z uwagi na możliwość braku optymalnej kontroli bólu [14]. Do leków, których stosowania należy unikać, zaliczamy neuroleptyki fenotiazynowe, hydroksyzynę, difenhydraminę, doksylaminę. Mechanizm farmakologicznego działania prydynolu nie jest kompatybilny z mechanizmem powstawania spastyczności w zespołach bólowych zlokalizowanych w narządzie ruchu. Wskazania do stosowania prydynolu obejmują: chorobę Parkinsona (jako leczenie wspomagające we wszystkich postaciach parkinsonizmu), zespoły spastyczne pochodzenia ośrodkowego i obwodowego (w tym zespoły indukowane przez leki), leczenie i zapobieganie nocnym skurczom mięśni (wspomagająco) oraz objawowe leczenie ślinotoku w przebiegu różnych schorzeń (z uwagi na efekt cholinolityczny). Nie należy kojarzyć prydynolu z innymi lekami o działaniu antycholinergicznym. Takie skojarzenie zwiększa ryzyko wystąpienia powikłań. Nie powinno się go stosować jednocześnie z amantadyną. Metoklopramid zmniejsza niepożądany wpływ prydynolu na perystaltykę przewodu pokarmowego, jednak metoklopramidu nie można stosować dłużej niż 5 dni.
Podsumowanie
Warto pamiętać, że stosowanie leków miorelaksujących wiąże się z ryzykiem ograniczenia sprawności psychofizycznej, jednak ryzyko to musi być oceniane indywidualnie.
Dawkowanie w praktyce powinno być indywidualizowane w zależności od wskazań i specyfiki leczonego pacjenta. Czynniki, które należy uwzględnić podczas wyboru leku miorelaksującego, zebrano w tabeli 4.

Skuteczność i bezpieczeństwo stosowania leków miorelaksujących muszą być rozpatrywane indywidualnie. Indywidualizacja wyboru leku miorelaksującego jest jednym z najistotniejszych czynników wpływających na uzyskanie skuteczności terapeutycznej i zmniejszenie ryzyka wystąpienia objawów niepożądanych.
Piśmiennictwo
1. Malec-Milewska M, Woroń J (red.). Kompendium leczenia bólu. Medical Education, Warszawa 2017.
2. Woroń J. Chory na nowotwór. Interakcje analgetyków i leków stosowanych w terapii objawów współtowarzyszących. Medical Education, Warszawa 2019.
3. Airaksinen O, Brox JI, Cedraschi C i wsp. Chapter 4 European guidelines for the management of chronic nonspecific low back pain. Eur Spine J 2006; 15 (Suppl. 2): S192-S300.
4. Brzeziński K. Niespecyficzny ból krzyża (medycyna oparta na faktach). Ból 2011; 12: 19-26.
5. Chou R, Qaseem A, Snow V i wsp. Rozpoznawanie i leczenie bólu krzyża. Wytyczne American College of Physicians i American Pain Society. Med Prakt 2008; 2: 92-119.
6. Sękowska A, Malec-Milewska M, Kolęda I. Bóle krzyża w praktyce lekarza rodzinnego. Klinika Nowa 2011;
5 (numer zjazdowy).
7. van Tulder M, Koes B. Chronic low back pain. W: Evidence-Based Chronic Pain Management. Stannard C,
Kalso E, Ballantyne J. Wiley-Blackwell 2010.
8. Koes BW, van Tulder M, Lin CW i wsp. An updated overview of clinical guidelines for the management of non-specific low back pain in primary care. Eur Spine J 2010; 19: 2075-2094.
9. Stannard C, Kalso E, Ballantyne J. Evidence-Based Chronic Pain Management. Blackwell Publishing 2010.
10. Macfarlane GJ, Jones GT, Hannaford PC. Managing low back pain presenting to primary care: where do we go from here? Pain 2006; 122: 219-222.
11. Kolęda I, Malec-Milewska M. Pacjent z przewlekłym bólem – diagnozowanie, leczenie, wytyczne. Praktyka Lekarska 2010; 11: 15-16.
12. Martindale. The Complete Drug Reference. Pharmaceutical Press, London 2020.
13. Istrati J, Kocot-Krępska M, Gadek A. Zespoły bólowe narządu ruchu – leczenie. Terapia 2010; 11-12: 27-34.
14. Woroń J, Siwek M, Wordliczek J, Kutaj-Wąsikowska H. Farmakoterapia bólu u pacjenta leczonego lekami psychotropowymi – dlaczego należy zachować ostrożność? Ból 2017; 18: 22-28.
Pełna treść artykułu: Jarosław Woroń. Leki miorelaksujące w praktyce klinicznej – dlaczego niezbędna jest indywidualizacja wyboru. Lekarz POZ 2021; 4: 301-306.