Najnowsze dowody skuteczności leków stosowanych w SMA
W terapii rdzeniowego zaniku mięśni (spinal muscular atrophy – SMA) można osiągnąć ogromny sukces, stosując najnowsze metody leczenia, prowadzące w różny sposób do zwiększenia ekspresji białka SMN. W ostatnim czasie ukazało się kilka ważnych publikacji podsumowujących osiągnięcia w leczeniu SMA z użyciem nusinersenu i rysdyplamu.
Mogą one w przyszłości doprowadzić do rozszerzenia wskazań terapeutycznych na nowe grupy pacjentów oraz do personalizacji leczenia SMA.
Nusinersen jest oligonukleotydem antysensownym wpływającym na splicing genu SMN2, a przez to na produkcję białka SMN. Początkowe badania nad skutecznością tego leku były ukierunkowane na pacjentów z SMA typu 1, o najcięższym fenotypie i początku w wieku niemowlęcym. Obecnie część badań jest rozszerzana na starsze grupy pacjentów, z wolniej postępującą postacią SMA. W ostatnim czasie w „Orphanet Journal of Rare Disease” ukazała się ważna metaanaliza Coratti i wsp. dotycząca stosowania nusinersenu u pacjentów z SMA typu 2 i 31. Jest to największa dotychczas metaanaliza badań przeprowadzonych w tej grupie chorych, obejmująca ponad 2600 pacjentów do 78. roku życia z ośrodków z 10 krajów. Metaanalizy podsumowujące wyniki wielu badań z randomizacją z różnych ośrodków są bardzo ważnym narzędziem w ocenie skuteczności leczenia. Stanowią one najwyższej jakości dowody naukowe na skuteczność określonej terapii lub jej brak.
Nusinersen w terapii SMA w różnych grupach wiekowych – wyniki metaanalizy
Coratti i wsp. wśród ponad 15 tys. publikacji zidentyfikowali 30 prac oryginalnych oceniających funkcje ruchowe pacjentów z SMA, 15 z nich dotyczyło osób dorosłych leczonych nusinersenem, a 10 nieleczonych (dane dotyczące naturalnego przebiegu choroby). Pośród badań na populacji pediatrycznej 7 dotyczyło dzieci leczonych nusinersenem, a 6 zawierało dane dotyczące naturalnego przebiegu choroby. Porównywano między innymi zmianę w rozszerzonej skali sprawności motorycznej Hammersmith (Hammersmith Functional Motor Scale Expanded – HFMSE), oceniającej funkcje ruchowe chorych na SMA. W badaniu uwzględniono najważniejsze prace oryginalne na temat skuteczności leczenia SMA w warunkach codziennej praktyki klinicznej: Hagenacker i wsp. 2020, Maggi i wsp. 2020, Duong i wsp. 2021, Osmanovic i wsp. 2021. We wszystkich zidentyfikowanych pracach autorzy raportowali poprawę w grupie leczonej nusinersenem w stosunku do nieleczonej. Łączna średnia zmiana w grupie leczonej wynosiła 2,27 pkt w skali HFMSE (95 proc. CI: 1,41–3,13). U pacjentów nieleczonych łączna średnia zmiana wynosiła –1,00 (95 proc. CI: −1,33 – −0,67), co wskazuje na znamienną redukcję wyniku. Różnica w łącznej średniej zmianie punktacji między grupą leczoną a nieleczoną wynosiła więc 3,27 pkt i była istotna statystycznie (p < 0,0001). Również dodatkowe analizy porównujące efekt leczenia w grupie dorosłych i dzieci, chorych chodzących i niechodzących oraz z SMA typu 2 i 3 spójnie wskazują na korzyść wyrażoną poprawą w skali HFMSE w grupach poddanych terapii. Inne testy oceniające sprawność ruchową chorych (test 6-minutowego marszu – 6MWT, poprawiony moduł oceny kończyny górnej – RULM) również wskazywały, że chorzy leczeni uzyskiwali lepsze wyniki. W 6MWT poprawa u pacjentów leczonych wyniosła 19,80 metra i była istotna statystycznie. Różnica pomiędzy pacjentami leczonymi (+19,80) i nieleczonymi (–8,29) wyniosła 28,09 metra i była istotna statystycznie (p < 0,0001). Wyniki przemawiają za skutecznością nusinersenu w poprawie stanu ruchowego w grupie pacjentów z SMA typu 2 i 3 w obserwacji trwającej 10–14 miesięcy. U osób leczonych zmiana w punktacji jest pozytywna, natomiast u nieleczonych negatywna. Różnica była obserwowana nie tylko w kohortach ogólnych, lecz także w mniejszych grupach wyodrębnionych ze względu na wiek, typ SMA i stan ruchowy. Co istotne, poprawa punktacji w skalach oceniających stan ruchowy była widoczna także u chorych dorosłych, nie tylko w populacjach pediatrycznych. Wynosiła ona odpowiednio +1,87 (95 proc. CI: 1,05–2,68) w skali HFMSE, +0,64 (95 proc. CI: 0,27–1,01) w skali RULM i +20,28 (95 proc. CI: 1,17– 39,40) w 6MWT.
Rysdyplam w terapii SMA – wyniki badań SUNFISH i FIREFISH
Dysponujemy również nowymi danymi na temat leczenia SMA za pomocą rysdyplamu. Lek ten koryguje składanie genu SMN2, przesuwając równowagę w kierunku włączania eksonu 7 do transkryptu mRNA, co prowadzi do zwiększonego wytwarzania funkcjonalnego i stabilnego białka SMN. W 2021 r. w „New England Journal of Medicine” opublikowano częściowe wyniki badań SUNFISH i FIREFISH2, 3.
Przeczytaj także: „Skuteczność leków w SMA a wybór terapii”.
Celem badania FIREFISH3 było porównanie skuteczności leczenia rysdyplamem w różnych dawkach u dzieci z SMA typu 1 w wieku 1–7 miesięcy w porównaniu z historyczną kohortą pacjentów z naturalnym przebiegiem SMA typu 1. Nie zastosowano w nim metody podwójnie ślepej próby. Pierwszorzędowym punktem końcowym była zdolność utrzymania przez 5 sekund pozycji siedzącej bez podparcia po 12 miesiącach. Dzieci z SMA typu 1 nie są w stanie dojść bez leczenia do tego etapu rozwoju ruchowego. Po 12 miesiącach terapii 12 z 41 zrekrutowanych dzieci (29 proc.) osiągało ten punkt końcowy. Ponadto 85 proc. dzieci leczonych i zaledwie 42 proc. nieleczonych nie wymagało do przeżycia permanentnej wentylacji mechanicznej (p < 0,001). W 2022 r. w „Lancet Neurology” ukazały się natomiast wyniki podwójnie zaślepionego badania oceniającego leczenie rysdyplamem w starszej populacji, w wieku 2–25 lat2. Do badania włączono 120 chorych w grupie otrzymującej rysdyplam i 60 w grupie placebo, dorosłych i dzieci z SMA typu 2 i 3. Pierwszorzędowym punktem końcowym była zmiana w punktacji w skali MFM32 (Motor Function Measure 32) po 12 miesiącach leczenia. Skala MFM32 ocenia sprawność ruchową pacjentów z chorobami nerwowo-mięśniowymi. Badanie wykazało znamienną różnicę pomiędzy wynikami uzyskanymi w obu grupach – wzrost punktacji o 1,4 u leczonych rysdyplamem i spadek o 0,2 u otrzymujących placebo w całej kohorcie pacjentów między 2. a 25. rokiem życia z SMA typu 2 oraz niechodzących chorych z rozpoznaniem SMA typu 3. W analizie podgrup w różnych przedziałach wiekowych poprawę punktacji obserwowano u młodszych chorych, a stabilizację stanu ruchowego w skali MFM32 w starszych przedziałach wiekowych chorych leczonych rysdyplamem. Znamienną statystycznie redukcję punktacji w skali MFM32 osiągnięto w grupie pacjentów w wieku 2–6 lat. Nie ma danych na temat skuteczności leczenia w grupie chorych wymagających wentylacji mechanicznej. Badanie potwierdza skuteczność rysdyplamu i wykazuje, że lek ten modyfikuje naturalny przebieg SMA. Wyniki badania FIREFISH są spójne z pozytywnymi wynikami badania SUNFISH kontrolowanego placebo. Część 2 badania SUNFISH ciągle trwa i przyniesie zapewne nowe dane w tym zakresie. Rozpoczęte badanie JEWELFISH pozwoli uzyskać informacje na temat skuteczności leczenia w bardziej zaawansowanych grupach wiekowych chorych z SMA, do 60. roku życia.
Rekomendacje EMA i CADTH
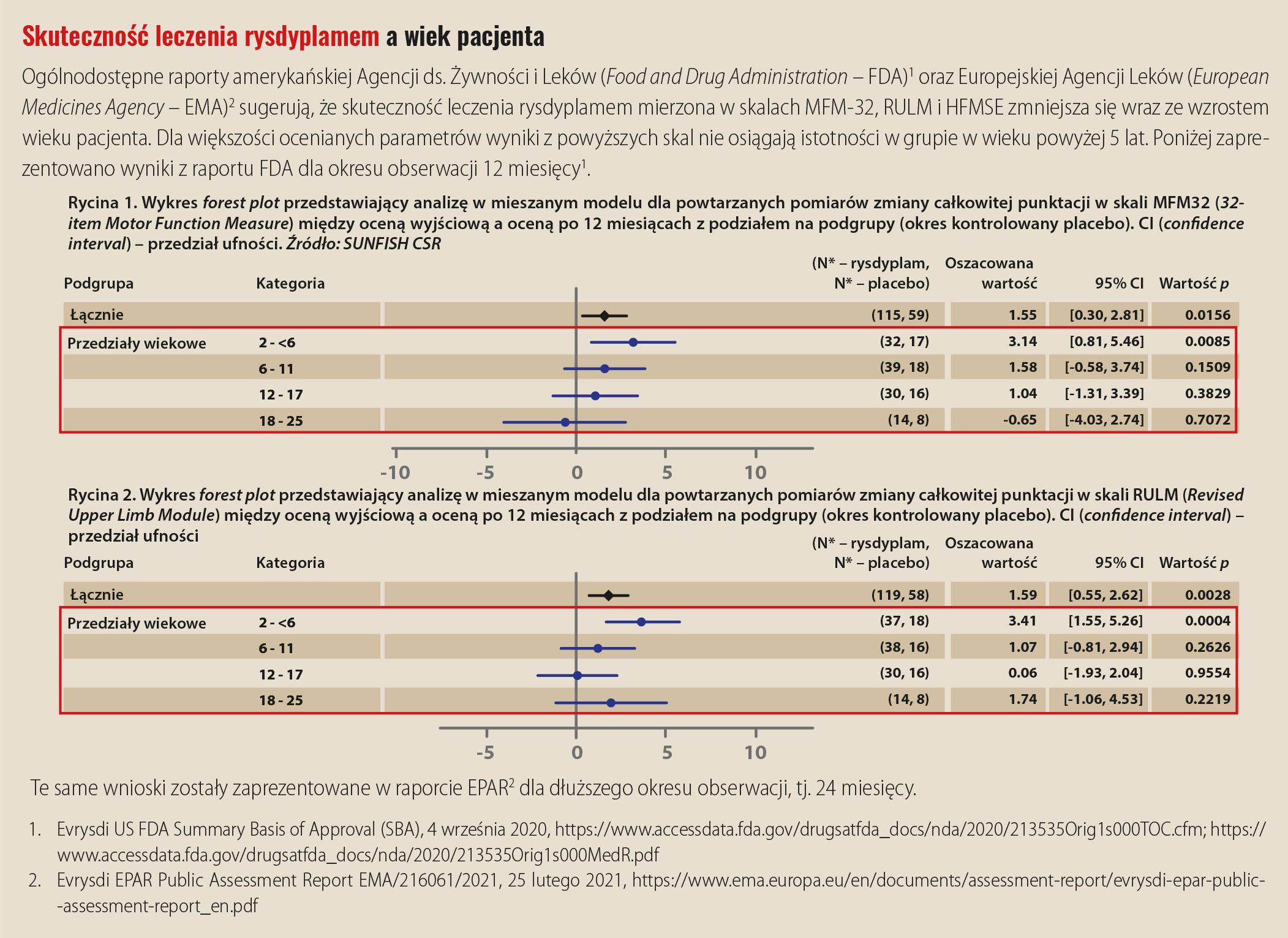
Badania FIREFISH i SUNFISH stanowiły podstawę do uzyskania przez rysdyplam rekomendacji Europejskiej Agencji Leków (European Medicines Agency – EMA) w leczeniu SMA 5q u pacjentów powyżej 2. miesiąca życia z klinicznym rozpoznaniem SMA typu 1, 2 lub 3 i jedną do czterech kopii genu SMN24. EMA zaleca wczesne rozpoczęcie terapii rysdyplamem ze względu na słabszy efekt uzyskiwany w starszych grupach chorych. W grupie wiekowej 2 – < 6 lat skuteczność leku wyrażona zmianą punktacji w skali MFM32 wynosiła 3,14 (CI: 0,81–5,46) i była znamienna statystycznie (p = 0,0085). W starszych grupach wiekowych zmiana nie była już istotna statystycznie. Poprawa wynosiła odpowiednio 1,58 pkt w grupie 6–11 lat i 1,04 pkt w grupie 12–17 lat. U chorych w wieku 18–25 lat obserwowano nieistotne statystycznie pogorszenie stanu ruchowego o 0,65 pkt. Również w skali RULM oceniającej sprawność kończyny górnej w analizie statystycznej z podziałem na podgrupy wiekowe istotność statystyczną zmian odnotowano tylko w grupie wiekowej 2 – < 6 lat.
Przeczytaj także: Rekomendacje HTA dotyczące terapii doustnej rdzeniowego zaniku mięśni.
Kanadyjska Agencja Oceny Leków i Technologii w Ochronie Zdrowia (Canadian Agency for Drugs and Technologies in Health – CADTH) również zaleca refundację rysdyplamu w leczeniu SMA5. Rekomendacja dotyczy leczenia chorych od 8. miesiąca do 25. roku życia z obecnością dwóch lub trzech kopii genu SMN2. W raporcie CADTH szacunkowy koszt terapii rysdyplamem jest niższy niż nusinersenem, a w dostępnych badaniach założono ich porównywalną skuteczność. Nie jest jednak znana długofalowa skuteczność terapii rysdyplamem w stosunku do nusinersenu. Mankamentem jest też brak badań dotyczących długoterminowej skuteczności rysdyplamu w stosunku do nusinersenu w grupie chorych na SMA typu 1 oraz dostępność wyłącznie jednego badania z jedną kohortą leczonych chorych, bez grupy kontrolnej (FIREFISH).
Canadian Drug Expert Committee (CDEC), będący grupą doradczą CADTH, wskazuje również na niepewny efekt kliniczny terapii rysdyplamem u pacjentów w wieku nastoletnim i dorosłym oraz na potencjalnie mniejszą skuteczność leczenia w grupie chorych w wieku 18–25 lat w porównaniu z dziećmi. Brakuje danych na temat skuteczności terapii rysdyplamem u osób powyżej 25. roku życia. Pojawienie się nowych terapii oraz dodatkowych danych z metaanaliz pozwala lepiej identyfikować chorych, którzy mogą skorzystać z danego typu leczenia. Może to prowadzić do personalizacji terapii chorych na SMA. Na podstawie dostępnych danych z metaanalizy na temat skuteczności nusinersenu u pacjentów z SMA typu 2 i 3 nie można wykluczyć jego przewagi nad rysdyplamem, który w dostępnych badaniach wykazywał największą skuteczność u chorych między 2. a 6. rokiem życia. Do jednoznacznego rozstrzygnięcia tej kwestii konieczne są przeprowadzenie większej liczby badań, dłuższa obserwacja jego działania na większych grupach chorych na SMA typu 2 i 3 oraz badania z podwójnie ślepą próbą u pacjentów z SMA typu 1.
Piśmiennictwo:
1 Coratti G, Cutrona C, Pera MC i wsp. Motor function in type 2 and 3 SMA patients treated with nusinersen: a critical review and metaanalysis. Orphanet J Rare Dis 2021; 16: 430.
2. Mercuri E, Deconinck N, Mazzone ES i wsp.; SUNFISH Study Group. Safety and effi cacy of once-daily risdiplam in type 2 and non-ambulant type 3 spinal muscular atrophy (SUNFISH part 2): a phase 3, double-blind, randomised, placebo-controlled trial. Lancet Neurol 2022; 21: 42-52.
3. Darras BT, Masson R, Mazurkiewicz-Bełdzińska M i wsp.; FIREFISH Working Group. Risdiplam- treated infants with type 1 spinal muscular atrophy versus historical controls. N Engl J Med 2021; 385: 427-435.
4. European Medicines Agency. Evrysdi. EPAR Public Assessment Report. EMA/216061/2021. EMA 2021.
5. CADTH Reimbursement Recomendation – Risdiplam (Evrysdi). Canadian Journal of Health Technologies. 2021; 1: 1-15.
6. Paine RW. Clinical review, NDA 213535. Evrysdi, risdiplam (RO7034067). Center for Drug Evaluation and Research 2017.
Autorki: Małgorzata Solarczyk, Anna Zielińska
Tekst pochodzi z „Kuriera Medycznego” 3/2022. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.

Nusinersen jest oligonukleotydem antysensownym wpływającym na splicing genu SMN2, a przez to na produkcję białka SMN. Początkowe badania nad skutecznością tego leku były ukierunkowane na pacjentów z SMA typu 1, o najcięższym fenotypie i początku w wieku niemowlęcym. Obecnie część badań jest rozszerzana na starsze grupy pacjentów, z wolniej postępującą postacią SMA. W ostatnim czasie w „Orphanet Journal of Rare Disease” ukazała się ważna metaanaliza Coratti i wsp. dotycząca stosowania nusinersenu u pacjentów z SMA typu 2 i 31. Jest to największa dotychczas metaanaliza badań przeprowadzonych w tej grupie chorych, obejmująca ponad 2600 pacjentów do 78. roku życia z ośrodków z 10 krajów. Metaanalizy podsumowujące wyniki wielu badań z randomizacją z różnych ośrodków są bardzo ważnym narzędziem w ocenie skuteczności leczenia. Stanowią one najwyższej jakości dowody naukowe na skuteczność określonej terapii lub jej brak.
Nusinersen w terapii SMA w różnych grupach wiekowych – wyniki metaanalizy
Coratti i wsp. wśród ponad 15 tys. publikacji zidentyfikowali 30 prac oryginalnych oceniających funkcje ruchowe pacjentów z SMA, 15 z nich dotyczyło osób dorosłych leczonych nusinersenem, a 10 nieleczonych (dane dotyczące naturalnego przebiegu choroby). Pośród badań na populacji pediatrycznej 7 dotyczyło dzieci leczonych nusinersenem, a 6 zawierało dane dotyczące naturalnego przebiegu choroby. Porównywano między innymi zmianę w rozszerzonej skali sprawności motorycznej Hammersmith (Hammersmith Functional Motor Scale Expanded – HFMSE), oceniającej funkcje ruchowe chorych na SMA. W badaniu uwzględniono najważniejsze prace oryginalne na temat skuteczności leczenia SMA w warunkach codziennej praktyki klinicznej: Hagenacker i wsp. 2020, Maggi i wsp. 2020, Duong i wsp. 2021, Osmanovic i wsp. 2021. We wszystkich zidentyfikowanych pracach autorzy raportowali poprawę w grupie leczonej nusinersenem w stosunku do nieleczonej. Łączna średnia zmiana w grupie leczonej wynosiła 2,27 pkt w skali HFMSE (95 proc. CI: 1,41–3,13). U pacjentów nieleczonych łączna średnia zmiana wynosiła –1,00 (95 proc. CI: −1,33 – −0,67), co wskazuje na znamienną redukcję wyniku. Różnica w łącznej średniej zmianie punktacji między grupą leczoną a nieleczoną wynosiła więc 3,27 pkt i była istotna statystycznie (p < 0,0001). Również dodatkowe analizy porównujące efekt leczenia w grupie dorosłych i dzieci, chorych chodzących i niechodzących oraz z SMA typu 2 i 3 spójnie wskazują na korzyść wyrażoną poprawą w skali HFMSE w grupach poddanych terapii. Inne testy oceniające sprawność ruchową chorych (test 6-minutowego marszu – 6MWT, poprawiony moduł oceny kończyny górnej – RULM) również wskazywały, że chorzy leczeni uzyskiwali lepsze wyniki. W 6MWT poprawa u pacjentów leczonych wyniosła 19,80 metra i była istotna statystycznie. Różnica pomiędzy pacjentami leczonymi (+19,80) i nieleczonymi (–8,29) wyniosła 28,09 metra i była istotna statystycznie (p < 0,0001). Wyniki przemawiają za skutecznością nusinersenu w poprawie stanu ruchowego w grupie pacjentów z SMA typu 2 i 3 w obserwacji trwającej 10–14 miesięcy. U osób leczonych zmiana w punktacji jest pozytywna, natomiast u nieleczonych negatywna. Różnica była obserwowana nie tylko w kohortach ogólnych, lecz także w mniejszych grupach wyodrębnionych ze względu na wiek, typ SMA i stan ruchowy. Co istotne, poprawa punktacji w skalach oceniających stan ruchowy była widoczna także u chorych dorosłych, nie tylko w populacjach pediatrycznych. Wynosiła ona odpowiednio +1,87 (95 proc. CI: 1,05–2,68) w skali HFMSE, +0,64 (95 proc. CI: 0,27–1,01) w skali RULM i +20,28 (95 proc. CI: 1,17– 39,40) w 6MWT.
Rysdyplam w terapii SMA – wyniki badań SUNFISH i FIREFISH
Dysponujemy również nowymi danymi na temat leczenia SMA za pomocą rysdyplamu. Lek ten koryguje składanie genu SMN2, przesuwając równowagę w kierunku włączania eksonu 7 do transkryptu mRNA, co prowadzi do zwiększonego wytwarzania funkcjonalnego i stabilnego białka SMN. W 2021 r. w „New England Journal of Medicine” opublikowano częściowe wyniki badań SUNFISH i FIREFISH2, 3.
Przeczytaj także: „Skuteczność leków w SMA a wybór terapii”.
Celem badania FIREFISH3 było porównanie skuteczności leczenia rysdyplamem w różnych dawkach u dzieci z SMA typu 1 w wieku 1–7 miesięcy w porównaniu z historyczną kohortą pacjentów z naturalnym przebiegiem SMA typu 1. Nie zastosowano w nim metody podwójnie ślepej próby. Pierwszorzędowym punktem końcowym była zdolność utrzymania przez 5 sekund pozycji siedzącej bez podparcia po 12 miesiącach. Dzieci z SMA typu 1 nie są w stanie dojść bez leczenia do tego etapu rozwoju ruchowego. Po 12 miesiącach terapii 12 z 41 zrekrutowanych dzieci (29 proc.) osiągało ten punkt końcowy. Ponadto 85 proc. dzieci leczonych i zaledwie 42 proc. nieleczonych nie wymagało do przeżycia permanentnej wentylacji mechanicznej (p < 0,001). W 2022 r. w „Lancet Neurology” ukazały się natomiast wyniki podwójnie zaślepionego badania oceniającego leczenie rysdyplamem w starszej populacji, w wieku 2–25 lat2. Do badania włączono 120 chorych w grupie otrzymującej rysdyplam i 60 w grupie placebo, dorosłych i dzieci z SMA typu 2 i 3. Pierwszorzędowym punktem końcowym była zmiana w punktacji w skali MFM32 (Motor Function Measure 32) po 12 miesiącach leczenia. Skala MFM32 ocenia sprawność ruchową pacjentów z chorobami nerwowo-mięśniowymi. Badanie wykazało znamienną różnicę pomiędzy wynikami uzyskanymi w obu grupach – wzrost punktacji o 1,4 u leczonych rysdyplamem i spadek o 0,2 u otrzymujących placebo w całej kohorcie pacjentów między 2. a 25. rokiem życia z SMA typu 2 oraz niechodzących chorych z rozpoznaniem SMA typu 3. W analizie podgrup w różnych przedziałach wiekowych poprawę punktacji obserwowano u młodszych chorych, a stabilizację stanu ruchowego w skali MFM32 w starszych przedziałach wiekowych chorych leczonych rysdyplamem. Znamienną statystycznie redukcję punktacji w skali MFM32 osiągnięto w grupie pacjentów w wieku 2–6 lat. Nie ma danych na temat skuteczności leczenia w grupie chorych wymagających wentylacji mechanicznej. Badanie potwierdza skuteczność rysdyplamu i wykazuje, że lek ten modyfikuje naturalny przebieg SMA. Wyniki badania FIREFISH są spójne z pozytywnymi wynikami badania SUNFISH kontrolowanego placebo. Część 2 badania SUNFISH ciągle trwa i przyniesie zapewne nowe dane w tym zakresie. Rozpoczęte badanie JEWELFISH pozwoli uzyskać informacje na temat skuteczności leczenia w bardziej zaawansowanych grupach wiekowych chorych z SMA, do 60. roku życia.

Rekomendacje EMA i CADTH
Badania FIREFISH i SUNFISH stanowiły podstawę do uzyskania przez rysdyplam rekomendacji Europejskiej Agencji Leków (European Medicines Agency – EMA) w leczeniu SMA 5q u pacjentów powyżej 2. miesiąca życia z klinicznym rozpoznaniem SMA typu 1, 2 lub 3 i jedną do czterech kopii genu SMN24. EMA zaleca wczesne rozpoczęcie terapii rysdyplamem ze względu na słabszy efekt uzyskiwany w starszych grupach chorych. W grupie wiekowej 2 – < 6 lat skuteczność leku wyrażona zmianą punktacji w skali MFM32 wynosiła 3,14 (CI: 0,81–5,46) i była znamienna statystycznie (p = 0,0085). W starszych grupach wiekowych zmiana nie była już istotna statystycznie. Poprawa wynosiła odpowiednio 1,58 pkt w grupie 6–11 lat i 1,04 pkt w grupie 12–17 lat. U chorych w wieku 18–25 lat obserwowano nieistotne statystycznie pogorszenie stanu ruchowego o 0,65 pkt. Również w skali RULM oceniającej sprawność kończyny górnej w analizie statystycznej z podziałem na podgrupy wiekowe istotność statystyczną zmian odnotowano tylko w grupie wiekowej 2 – < 6 lat.
Przeczytaj także: Rekomendacje HTA dotyczące terapii doustnej rdzeniowego zaniku mięśni.
Kanadyjska Agencja Oceny Leków i Technologii w Ochronie Zdrowia (Canadian Agency for Drugs and Technologies in Health – CADTH) również zaleca refundację rysdyplamu w leczeniu SMA5. Rekomendacja dotyczy leczenia chorych od 8. miesiąca do 25. roku życia z obecnością dwóch lub trzech kopii genu SMN2. W raporcie CADTH szacunkowy koszt terapii rysdyplamem jest niższy niż nusinersenem, a w dostępnych badaniach założono ich porównywalną skuteczność. Nie jest jednak znana długofalowa skuteczność terapii rysdyplamem w stosunku do nusinersenu. Mankamentem jest też brak badań dotyczących długoterminowej skuteczności rysdyplamu w stosunku do nusinersenu w grupie chorych na SMA typu 1 oraz dostępność wyłącznie jednego badania z jedną kohortą leczonych chorych, bez grupy kontrolnej (FIREFISH).
Canadian Drug Expert Committee (CDEC), będący grupą doradczą CADTH, wskazuje również na niepewny efekt kliniczny terapii rysdyplamem u pacjentów w wieku nastoletnim i dorosłym oraz na potencjalnie mniejszą skuteczność leczenia w grupie chorych w wieku 18–25 lat w porównaniu z dziećmi. Brakuje danych na temat skuteczności terapii rysdyplamem u osób powyżej 25. roku życia. Pojawienie się nowych terapii oraz dodatkowych danych z metaanaliz pozwala lepiej identyfikować chorych, którzy mogą skorzystać z danego typu leczenia. Może to prowadzić do personalizacji terapii chorych na SMA. Na podstawie dostępnych danych z metaanalizy na temat skuteczności nusinersenu u pacjentów z SMA typu 2 i 3 nie można wykluczyć jego przewagi nad rysdyplamem, który w dostępnych badaniach wykazywał największą skuteczność u chorych między 2. a 6. rokiem życia. Do jednoznacznego rozstrzygnięcia tej kwestii konieczne są przeprowadzenie większej liczby badań, dłuższa obserwacja jego działania na większych grupach chorych na SMA typu 2 i 3 oraz badania z podwójnie ślepą próbą u pacjentów z SMA typu 1.
Piśmiennictwo:
1 Coratti G, Cutrona C, Pera MC i wsp. Motor function in type 2 and 3 SMA patients treated with nusinersen: a critical review and metaanalysis. Orphanet J Rare Dis 2021; 16: 430.
2. Mercuri E, Deconinck N, Mazzone ES i wsp.; SUNFISH Study Group. Safety and effi cacy of once-daily risdiplam in type 2 and non-ambulant type 3 spinal muscular atrophy (SUNFISH part 2): a phase 3, double-blind, randomised, placebo-controlled trial. Lancet Neurol 2022; 21: 42-52.
3. Darras BT, Masson R, Mazurkiewicz-Bełdzińska M i wsp.; FIREFISH Working Group. Risdiplam- treated infants with type 1 spinal muscular atrophy versus historical controls. N Engl J Med 2021; 385: 427-435.
4. European Medicines Agency. Evrysdi. EPAR Public Assessment Report. EMA/216061/2021. EMA 2021.
5. CADTH Reimbursement Recomendation – Risdiplam (Evrysdi). Canadian Journal of Health Technologies. 2021; 1: 1-15.
6. Paine RW. Clinical review, NDA 213535. Evrysdi, risdiplam (RO7034067). Center for Drug Evaluation and Research 2017.
Autorki: Małgorzata Solarczyk, Anna Zielińska
Tekst pochodzi z „Kuriera Medycznego” 3/2022. Czasopismo można zamówić na stronie: www.termedia.pl/km/prenumerata.