22.09.2013
Autor:
Dr Mackiewicz
Źródło: FDA Approval for Paclitaxel Albumin-stabilized Nanoparticle Formulation. http://www.cancer.gov/cancertopics/druginfo/fda-nanoparticle-paclitaxel
Abraksan w pierwszej linii leczenia chorych na raka trzustki – nowe wskazanie.
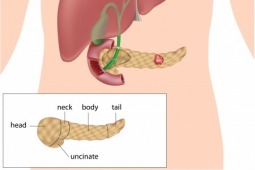
6 września 2013 roku lek abraksan zyskał nowe wskazanie w Stanach Zjednoczonych. Amerykańska agencja FDA (Food and Drug Administration) zarejestrowała ten lek w połączeniu z gemcytabiną w pierwszej linii leczenia chorych na przerzutowego raka trzustki. Poniżej prezentujemy wyniki badania na podstawie których dokonano rejestracji.
Artykuł dostępny wyłącznie dla:
lekarz, lekarz dentysta, lekarz w trakcie specjalizacji .Zaloguj się, aby przeczytać pełną treść artykułu.
Zaloguj się
Nie pamiętasz hasła?
Skorzystaj z opcji przypominania hasła, aby odzyskać dostęp do swojego konta Termedia.
Kategorie:
Przewód pokarmowy