16.08.2021
Redaktor:
Krystian Lurka
Źródło: Witold Zatoński, Kinga Janik-Koncewicz i Aleksandra Herbeć
O skutecznym leku zmniejszającym zachorowalność na choroby tytoniowe
Zespół prof. Witolda Zatońskiego od początku XXI wieku przeprowadził serię badań. Wykazały one skuteczność i bezpieczeństwo stosowania cytyzyny. – Lek jest obecnie poddawany badaniom międzynarodowym, które pozwolą na wprowadzenie tego skutecznego i bezpiecznego w leczeniu zespołu uzależnienia od tytoniu preparatu na rynki krajów zachodnich i rozwijających się – piszą eksperci.
Artykuł Witolda A. Zatońskiego i Kingi Janik-Koncewicz z Instytutu – Europejskiego Obserwatorium Nierówności Zdrowotnych, Akademii Kaliskiej oraz Fundacji „Promocja Zdrowia”, a także Aleksandry Herbeć z University College London w Wielkiej Brytanii oraz Fundacji „Promocja Zdrowia”:
Leki wspierające rzucanie palenia papierosów są ważnym elementem zmniejszającym zachorowalność na choroby tytoniowe. Większość palaczy podejmuje corocznie próbę rzucenia palenia. W Polsce w ostatnim dziesięcioleciu obok leków używanych do wspierania rzucania palenia papierosów i preparatów tzw. nikotynowej terapii zastępczej (NTZ), których sprzedaż podwoiła się w ostatnim dziesięcioleciu i wynosi obecnie ponad 3 mln opakowań rocznie, coraz istotniejszą rolę odgrywa roślinny preparat cytyzynowy. Nasz zespół od początku XXI wieku przeprowadził serię badań – wykazały one skuteczność i bezpieczeństwo stosowania cytyzyny, której obecna sprzedaż oscyluje około miliona kuracji rocznie. Cena cytyzyny jest mniej więcej 10 razy niższa niż preparatu warenikliny, z farmakologicznego punktu widzenia identycznego leku produkowanego przez firmę Pfizer.
Cytyzyna, która jest historycznie zarejestrowana jeszcze w kilku wschodnioeuropejskich krajach, tylko w Polsce od 20 lat jest stosowana na populacyjną skalę. Lek jest obecnie poddawany badaniom międzynarodowym, które pozwolą na wprowadzenie tego skutecznego i bezpiecznego w leczeniu zespołu uzależnienia od tytoniu (ZUT) preparatu na rynki krajów zachodnich i rozwijających się. W ostatnich latach porównano skuteczność i bezpieczeństwo cytyzyny z preparatami NTZ, a w ostatnich miesiącach – z warenikliną, lekiem firmy Pfizer działającym w identyczny sposób jak cytyzyna na centralny układ nerwowy.
Prezentowane w ostatnim roku badania z Nowej Zelandii i innych krajów wykazały, że cytyzyna jest co najmniej tak skuteczna jak wareniklina, przy czym wykazuje znacznie mniejsze efekty uboczne. Wydaje się, że wyniki ostatnio opublikowanych badań nad cytyzyną są kolejnym krokiem do stworzenia podstaw dalszej skutecznej kontroli chorób odtytoniowych na świecie. Lek ten – bardzo popularny wśród rzucających palenie i używany przez miliony Polaków podejmujących próbę rzucenia palenia – wymaga także w Polsce znacznie większego zainteresowania środowiska medycznego i osób odpowiedzialnych za zdrowie publiczne.
Wprowadzenie
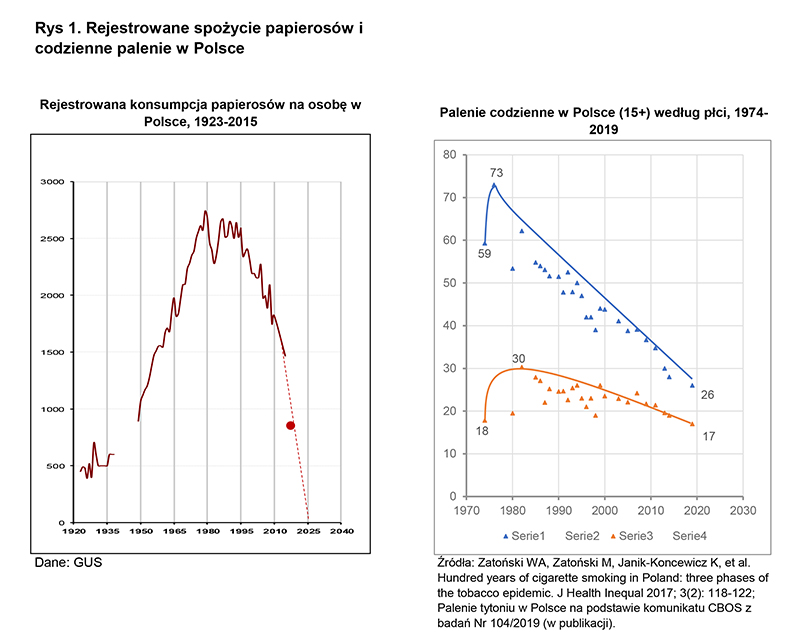
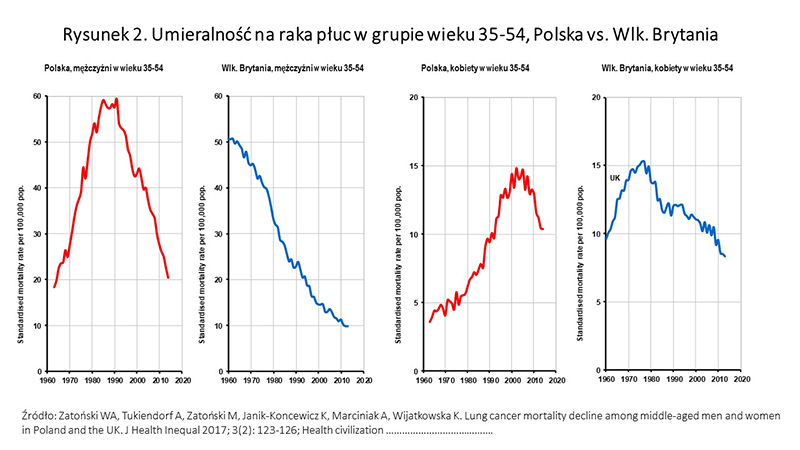
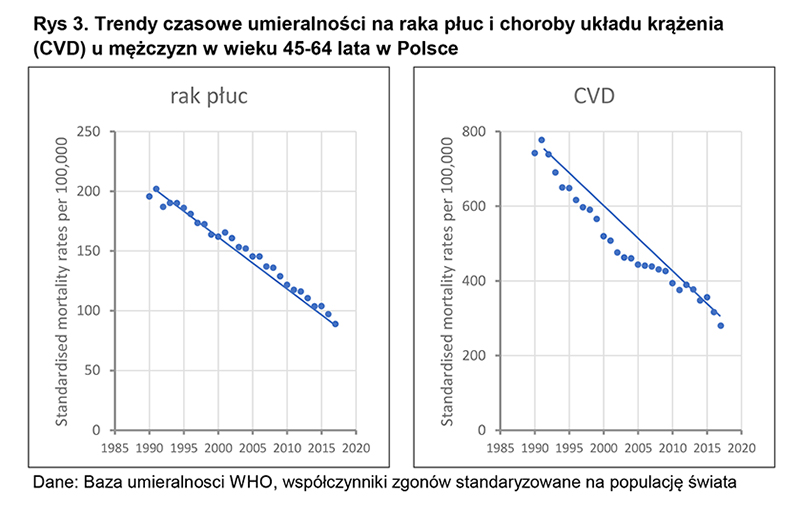
Pod koniec lat 80. Polska była krajem o jednym z najwyższych poziomów konsumpcji tytoniu na świecie i wynikających z tego szkód zdrowotnych 1-6. Rozpoczęte na początku okresu transformacji społeczno-ekonomicznej działania i stworzony strategiczny Narodowy Program Ograniczenia Zdrowotnych Skutków Palenia Tytoniu (NPOZSPT), a także przyjęcie ustawy sejmowej w 1995 roku 4,7-10 doprowadziły do znacznego zmniejszenia konsumpcji tytoniu i częstości palenia 4,11. Sprzedaż tytoniu spadła z ok. 100 mld papierosów na początku lat 90. do poniżej 40 mld w 2018 roku (rysunek 1), w następstwie czego doszło do znamiennego zmniejszenia zachorowań i zgonów z powodu chorób odtytoniowych 1,3,12,13. W ostatnich latach ukazało się kilka ważnych publikacji międzynarodowych, które wskazują, że po 1990 roku Polska należy do krajów o najszybszym spadku konsumpcji papierosów i zachorowań z powodu chorób odtytoniowych 4,6,12-14 (rysunek 1, 2). Dobrą ilustracją tego zjawiska jest trend czasowy umieralności z powodu raka płuca, schorzenia występującego prawie wyłącznie u palaczy papierosów 3,4 (rysunek 2) oraz trend czasowy umieralności z powodu chorób kardiowaskularnych (paleniu papierosów przypisuje się w skali populacyjnej 30–50-proc. związek przyczynowy z tymi chorobami w krajach europejskich) 15 (rysunek 3).
Historia leczenia z palenia tytoniu
Wydaje się, że leki wspierające rzucanie palenia papierosów są ważnym elementem zmniejszającej się konsumpcji tytoniu i częstości palenia papierosów w Polsce, szczególnie w ostatniej dekadzie.
Rynek nowoczesnych leków, które są oparte na dowodach naukowych (science and evidence-based), stosowanych do leczenia zespołu uzależnienia od tytoniu (ZUT) 16-19 rozwija się na świecie dopiero od początku lat 80. ubiegłego wieku. Wyjątkiem były kraje socjalistyczne (RWPG), gdzie już w drugiej połowie poprzedniego stulecia na rynku był dostępny, ale bardzo rzadko używany lek pod firmową nazwą Tabex, stworzony i produkowany w Bułgarii w latach 40. i 50. XX wieku. Lek ten był nieznany i nieobecny na rynkach krajów zachodnich 20.
W ostatnich dekadach w Europie na populacyjną skalę używanych jest kilka preparatów o udowodnionym naukowo działaniu, których sprzedaż liczy się w milionach opakowań rocznie 16-19, i rynek ten stale rośnie. Pierwsza, często używana, rekomendowana przez Światową Organizację Zdrowia grupa leków to tzw. nikotynowa terapia zastępcza (NTZ). Używanie NTZ określa się jako „harm reduction”, czyli zastępowanie w procesie leczenia nikotyny z dymu tytoniowego chemicznie czystą nikotyną. Lek ten produkowany jest w rozmaitych formach: gumy do żucia, plastrów, drażetek, tabletek, inhalatorów, etc. Historycznie pierwszym preparatem z tej grupy była nikotynowa guma do żucia pod firmową nazwą Nicorette, wprowadzona na rynek najpierw dla marynarzy łodzi podwodnych przez szwedzką firmę farmaceutyczną LEO. Ta grupa substancji używanych do wspomagania rzucania palenia była obecna na polskim rynku już kilka lat po premierze w Szwecji. Została wprowadzona tzw. szybką ścieżką pod presją lekarzy onkologów. Początkowo była możliwa do zakupu za twardą walutę w dolarowych sklepach (Pewex). Z powodu tych wszystkich zdarzeń już bardzo szybko cieszyła się dobrą sławą wśród osób rzucających palenie. Dopiero jednak po zmianie klimatu wokół palenia sprzedaż leków NTZ zaczęła gwałtownie rosnąć. Programy prewencji chorób odtytoniowych, szczególnie akcje „Rzuć palenie razem z nami” 10 czy akcje edukacyjne i interwencyjne m.in. sanepidu w latach 90., doprowadziły do zmiany postawy Polaków wobec papierosów. Jeden z twórców Nicorette, Karl Fagerstrom, wraz z innymi specjalistami opublikował raport (Lung Cancer 2001) 21 wskazujący, że Szwecja i Polska miały w tym czasie najlepszy w krajach europejskich klimat antytytoniowy. Sprzedaż opakowań wszystkich rodzajów NTZ wzrosła w Polsce sześciokrotnie, od ok. 0,5 mln opakowań rocznie na początku XXI wieku do ponad 3 mln w 2019 r. Używanie NTZ stale rośnie także w ostatnim 10-leciu, w którym uległo podwojeniu z ok. 1,6 mln opakowań do prawie 3 mln 22. Prognozy przemysłu farmaceutycznego przewidują dla Polski dalsze rozszerzanie się rynku. Celem powinna być sprzedaż 6–8 mln opakowań rocznie. Leczenie preparatami NTZ (preparatami czystej nikotyny przygotowanej do użytku medycznego) powinno być nadal ważnym elementem zdrowia publicznego.
Następnie w latach 90., szczególnie w krajach zachodnich, popularne stały się leki o działaniu centralnym na receptory mózgowe – najpierw bupropion, a następnie wareniklina. W większości krajów świata, łącznie z USA i wszystkimi zachodnimi krajami Unii Europejskiej, najpopularniejszym, najczęściej używanym preparatem leczniczym stała się wareniklina sprzedawana pod firmowymi nazwami Champix w Europie i Chantix w USA.
Polski rynek produktów używanych do leczenia ZUT różni się jednak znacząco od rynków w krajach zachodnich. Główna różnica polega na stosowaniu dodatkowo na populacyjną skalę setek tysięcy opakowań rocznie roślinnego preparatu cytyzyny, opracowanego w latach 60. (Paskow i Dobrew) w Bułgarii i stosowanego przez kilka dziesięcioleci, ale na bardzo niewielką skalę, w wielu krajach byłego bloku sowieckiego 17,23.
Cytyzyna to alkaloid pochodzenia roślinnego, uzyskiwany z ekstraktu z drzewa złotokapu zwyczajnego, potocznie zwanego „fałszywym tytoniem” (false tobacco) lub „złotym deszczem”, występującego m.in. w środkowej i południowej Europie. Cytyzyna ma budowę chemiczną i wiązanie receptorów podobne do nikotyny i jest częściowym agonistą nikotynowych receptorów cholinergicznych α4β2 w mózgu. Właściwości farmakologiczne cytyzyny powodują blokowanie receptorów nikotynowych i zmniejszanie głodu nikotynowego występującego po rzuceniu palenia 17,20,23-26.
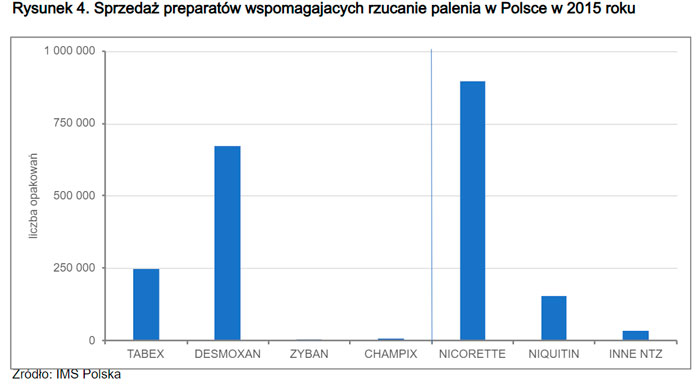
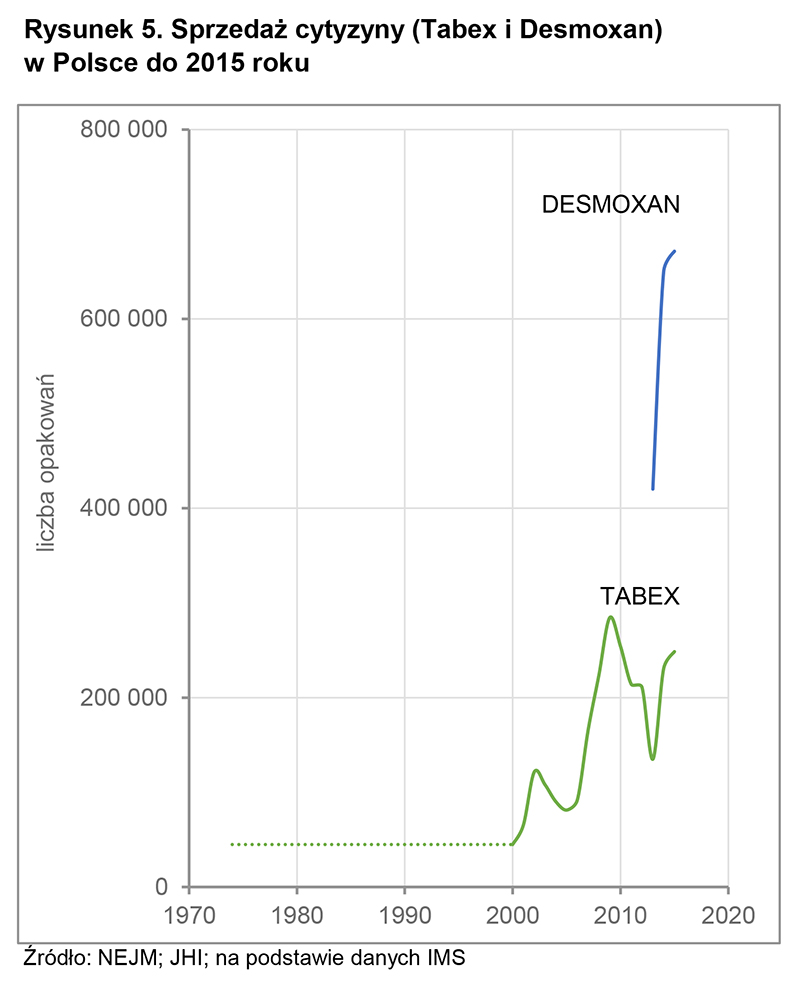
Historycznie ten obecny od początku lat 70. na polskim rynku preparat był bardzo rzadko używany 27,28. Jego sprzedaż do 2000 roku była na poziomie 20–40 tys. opakowań rocznie (rysunek 4, 5). Po zmianach społeczno-ekonomicznych i w trakcie przygotowań Polski do wejścia do Unii Europejskiej istniejąca dokumentacja farmakologiczna leku została zakwestionowana i uznana za niewystarczającą na rejestrację w Polsce – kraju Unii Europejskiej. Pod presją środowiska medycznego polskie Ministerstwo Zdrowia wyraziło zgodę na warunkowe zarejestrowanie leku, zobowiązując Centrum Onkologii w Warszawie, koordynujące wówczas Narodowy Program Ograniczenia Zdrowotnych Skutków Palenia Tytoniu w Polsce, do przeprowadzenia nowoczesnych badań epidemiologicznych oceniających skuteczność i bezpieczeństwo stosowania cytyzyny 17.
Grupa badawcza z Zakładu Epidemiologii Centrum Onkologii w Warszawie rozpoczęła szeroko zakrojone badania nad cytyzyną, przy dobrej współpracy z producentem leku (Sopharma z Bułgarii), który udostępnił dokumentację i leki do badań 24. W ich ramach lek został opisany według nowoczesnych standardów. W pierwszej kolejności przeprowadzono i opublikowano otwarte badanie kliniczne 29,30, a następnie we współpracy z renomowaną grupą badaczy angielskich wysokiej jakości double-blind placebo-controlled clinical trial, tzw. badanie TASC (Tabex Smoking Cessation), którego głównymi badaczami byli: prof. Witold Zatoński, ówcześnie z Centrum Onkologii w Warszawie, i prof. Robert West z University College London w Wielkiej Brytanii 31.
W 2011 roku w jednym z najbardziej wpływowych naukowych czasopism medycznych „New England Journal of Medicine” zostały opublikowane wyniki przeprowadzonego zgodnie z zasadami Unii Europejskiej klinicznego badania cytyzyny, które wykazały jej prawie 3,5-razy większą skuteczność w odchodzeniu od palenia tytoniu niż placebo oraz pełne bezpieczeństwo 17,31. Przygotowany przez zespół badawczy raport pozwolił na bezwarunkową rejestrację preparatu cytyzyny. Jednocześnie uznano, że lek może być sprzedawany bez recepty oraz zezwolono na jego promocję w środkach masowego przekazu, łącznie z promocją w telewizji, na co zezwalała ustawa o ograniczeniu zdrowotnych następstw palenia tytoniu z 1995 roku 7,32. Efektem bezpośredniej reklamy telewizyjnej skierowanej do palaczy z pominięciem lekarzy jest zdumiewająco niska znajomość preparatu cytyzynowego przez lekarzy w Polsce (na przykład w porównaniu z urządzeniami do podawania nikotyny, tzw. e-papierosami). Dziwi też całkowity brak zainteresowania administracji państwowej w promowaniu tego ważnego leku dla zdrowia w Polsce.
Stało się to początkiem zainteresowania polskich producentów leków (generyków), którzy doprowadzili do pojawienia się na polskim rynku, obok produkowanego przez Bułgarię preparatu Tabex, także dwóch innych produktów: Desmoxanu (2014) i Recigaru (2017) 32.
Niestety, w Europie Wschodniej producenci mimo znaczącej, idącej w miliony opakowań sprzedaży nie podjęli prac badawczych nad stworzeniem nowej innowacyjnej formy leku łatwiejszego w użyciu, z lepszym przyswajaniem, z opartym na wiedzy dawkowaniem, a stale sprzedają w niezmienionej formie lek opracowany przez Bułgarów w latach 40. ubiegłego wieku.
Jednocześnie w Polsce od początku lat 90. były prowadzone szeroko zakrojone działania dla stworzenia narodowego systemu leczenia ZUT 17,18,21,29. Kinga Janik-Koncewicz i wsp. 16 opisali czynniki składowe tego systemu, które m.in. doprowadziły do stworzenia i promowania zasad leczenia z palenia tytoniu, powstania konsensusu diagnostyki i leczenia ZUT przygotowanego przez najwybitniejszych polskich lekarzy 17-19, zorganizowania szerokiego programu kształcenia kadr medycznych w tym zakresie, modułów promocji rzucania palenia wśród palaczy.
Obok leków niezbędnym elementem jest stworzenie w Polsce systemu medycznego pomagającego palącym w rzucaniu nałogu. Osiemdziesiąt procent palących w Polsce deklaruje chęć zaprzestania palenia. Między innymi Fundacja „Promocja Zdrowia” podjęła się w Polsce budowania platformy informatycznej (STAR), której celem jest wieloczynnikowy system uczenia, wspomagania, motywowania procesu leczenia zespołu uzależnienia od tytoniu (ZUT) u palaczy. Stworzenie platformy elektronicznej wspomagającej proces rzucania palenia i nowoczesnych, innowacyjnych form skutecznego i bezpiecznego leku, to kluczowe elementy zmniejszenia liczby osób palących i wynikające z tego zmniejszenie umieralności przed 65. rokiem życia do poziomu poniżej 10 proc. w czasie najbliższych dziesięcioleci 19. Niestety, w 2015 roku z zupełnie niezrozumiałych powodów wstrzymano w Polsce realizację Narodowego Programu Ograniczenia Zdrowotnych Skutków Palenia Tytoniu (NPOZSPT) uchwalonego w 1995 roku przez parlament. Zawieszono finansowanie przez państwo programów, badań (m.in. sprzedaży i częstości palenia), interwencji wprowadzonych przez administracje i samorządy.
Publikacja cytyzynowa w 2011 r. w „New England Journal of Medicine” badań klinicznych była przez polskich badaczy promowana na licznych kongresach naukowych 10,21,33 i stała się początkiem szerokiego zainteresowania tym preparatem w wielu krajach świata. Podjęte przez polskich badaczy działania dla popularyzacji cytyzyny doprowadziły do zainteresowania tym preparatem badaczy m.in. w Wielkiej Brytanii, USA i Nowej Zelandii. Doprowadziło to do serii publikacji naukowych i rozpoczęcia prac nad nowymi formami cytyzyny i jej dawkowaniem. Jednym z nich było badanie kliniczne porównujące cytyzynę z Nicorette oraz ostatnio przeprowadzone badanie porównujące cytyzynę z warenikliną, które są także przedmiotem referowanej przez nas pracy.
Badanie RAUORA
Niestety, ani w Polsce, ani w Bułgarii w ostatnich dziesięcioleciach nie udało się doprowadzić do stworzenia programu aktualizacji i modernizacji preparatu cytyzyny. Badania w Polsce doprowadziły jednak do zainteresowania cytyzyną na świecie.
W USA zostało stworzone państwowo-prywatne konsorcjum Achieve Life Sciences, którego celem stało się przebadanie preparatu cytyzynowego, nazywanego przez konsorcjum „cytisinicline”, wykonanie kolejnych wzorowanych na badaniu TASC badań klinicznych określających skuteczność i bezpieczeństwo leku oraz porównanie cytyzyny z warenikliną 34. Wareniklina, lek stworzony w latach 90. przez firmę Pfizer, wzorowana była właśnie na cytyzynie 35. Obecnie w krajach zachodnich jest ona najpopularniejszym (obok NTZ) – i uważanym za najskuteczniejszy – środkiem używanym do leczenia ZUT. Problem ze stosowaniem warenikliny wynika z obciążenia tego preparatu różnorodnymi, także przypisywanymi mu poważnymi działaniami ubocznymi 25,34,36,37.
Badanie RAUORA (Head-to-Head Non-Inferiority Clinical Trial Comparing Cytisinicline and Chantix (varenicline) as a Treatment to Quit Smoking) jest prowadzone w Nowej Zelandii przez University of Auckland 34. Randomizowana podwójnie ślepa próba badawcza składa się z 679 osób, u których przez 12 tygodni według zasad randomizacji podawane są cytyzyna i wareniklina. Punktem końcowym badania po 6 miesiącach jest potwierdzona przez testy biochemiczne utrzymująca się abstynencja nikotynowa. Kliniczna próba wykazała, że cytyzyna jest co najmniej tak skuteczna w rzucaniu tytoniu jak wareniklina 38. Co jest niezwykle ważne, stosowany preparat cytyzynowy wykazał znamiennie mniej objawów ubocznych w porównaniu z warenikliną i jest w pełni bezpieczny 39-43.
Wyniki tego skończonego badania właśnie zostały opublikowane 38. Dodatkowo w ostatnich latach ukazały się badania kliniczne prowadzone przez inne zespoły 44-47. Są kolejnym dowodem, że używany tylko w Polsce na populacyjną skalę bardzo intensywnie od 2000 roku preparat jest najskuteczniejszym i najbezpieczniejszym obecnym na rynku lekiem leczącym ZUT. Do tego cena tego generyku jest o rząd wielkości mniejsza niż warenikliny.
Résumé:
W ostatnich tygodniach przedstawiono informacje o wynikach badania nad skutecznością i bezpieczeństwem dwóch najczęściej używanych na świecie przez palaczy leków działających na receptory cholinergiczne α4β2 centralnego układu nerwowego: cytyzyny (cytisinicline nowej postaci preparatu przygotowanej przez konsorcjum Achieve Life Sciences) oraz warenikiliny (produkowanej przez firmę Pfizer pod fabryczną nazwą Champix w Europie i Chantix w USA). Badacze porównywali skuteczność leków wśród rzucających palenie oraz ewentualne objawy uboczne występujące przy ich stosowaniu.
Badanie RAUORA (Head-to-Head Non-Inferiority Clinical Trial Comparing Cytisinicline and Chantix (varenicline) as a Treatment to Quit Smoking) wykazało że „cytyzyna demonstruje skuteczność rzucania palenia co najmniej tak efektywną jak wareniklina oraz znamiennie mniej efektów ubocznych niż wareniklina”.
Jest to kolejny etap pracy i oceny używanego na populacyjną skalę tylko w Polsce roślinnego preparatu cytyzyny 37 i jego porównania z produkowanym przez renomowaną firmę farmaceutyczną preparatem warenikliny.
Autorzy pracy chcieliby podziękować firmie IQVIA Polska za udostępnienie danych o sprzedaży leków ZUT w Polsce.
Literatura:
1. Zatoński WA, Zatoński M, Janik-Koncewicz K, et al. Hundred years of cigarette smoking in Poland: three phases of the tobacco epidemic. J Health Inequal 2017; 3(2): 118-122.
2. Zatoński WA, Tukiendorf A, Zatoński M, Janik-Koncewicz K, Marciniak A, Wijatkowska K. Lung cancer mortality decline among middle-aged men and women in Poland and the UK. J Health Inequal 2017; 3(2): 123-126.
3. Zatoński WA, Zatoński M. Poland’s rapid lung cancer decline in the years 1990-2016. The first step towards the eradication of lung cancer in Poland. Health Prob Civil 2017; 11(4): 211-225.
4. Zatonski W and HEM project team. Closing the health gap in European Union. The Maria Skłodowska-Curie Memorial Cancer Center and Institute of Oncology, Warsaw 2008.
5. Zatonski W, Przewozniak K, Sulkowska U, et al. Tobacco smoking in countries of the European Union. Ann Agric Environ Med. 2012; 19:181-192.
6. Zatonski WA, Bhala N. Changing trends of diseases in Eastern Europe: closing the gap. Public Health 2012; 126:248-252.
7. Dz.U.1996 nr 10 poz. 55. Ustawa z dnia 9 listopada 1995 r. o ochronie zdrowia przed następstwami używania tytoniu i wyrobów tytoniowych Journal of Laws of the Republic of Poland 1996, nr 10, poz. 55. Law from 9 November 1995 regarding the protection of health from the consequences of using tobacco and tobacco products.
8. Boyle P, Gray N, Henningfield J, Sefrin J, Zatoński W. Tobacco Science, Policy and Public Health. Second edition. Oxford University Press, Oxford 2010.
9. Zatonski WA. The Polish Anti-tobacco Law-20 years on. J Health Inequal 2016; 2(1):25.
10. Zatoński M, Zatoński WA, Przewoźniak K, Jaworski M. The significance and impact of the Polish Anti-tobacco Law. J Health Inequal 2016; 2 (1): 32-35.
11. Zatoński MZ. State, society, and the politics of smoking in Poland, during and after communism (1960-2000). PhD thesis. London School of Hygiene & Tropical Medicine, London 2019.
12. Hoffman SJ, Mammone J, Rogers Van Katwyk S, et al. Cigarette consumption estimates for 71 countries from 1970 to 2015: systematic collection of comparable data to facilitate quasi-experimental evaluations of national and global tobacco control interventions. BMJ 2019; 19: 12231.
13. GBD 2015 Tobacco Collaborators. Smoking prevalence and attributable disease burden in 195 countries and territories, 1990-2015: a systematic analysis from the Global Burden of Disease Study 2015. Lancet 2017; 389: 1885-1906.
14. Ng M, Freeman MK, Fleming TD, Robinson M, et al. Smoking prevalence and cigarette consumption in 187 countries, 1980-2012. JAMA 2014; 311: 183-192.
15. Unal B, Critchley JA, Capewell S. Explaining the decline in coronary heart disease mortality in England and Wales between 1981 and 2000. Circulation 2004; 109(9): 1101-1107.
16. Janik-Koncewicz K, Zatoński M, Herbeć A, Zatoński WA. The role of the Health Promotion Foundation in building capacity to treat tobacco dependence in Poland: past, present and future. J Health Inequal 2017; 3(2): 127-132.
17. Zatoński W (ed.). Konsensus dotyczący rozpoznawania i leczenia zespołu uzależnienia od tytoniu Consensus on diagnosis and treatment of tobacco dependence. Med Prakt 2006; 7 (special ed.): 5-24.
18. Zatoński W, Jankowski P, Banasiak W, Kawecka-Jaszcz K, Musiał J, Narkiewicz K, Opolski G, Podolec P, Torbicki A, Zembala M. Wspólne stanowisko dotyczące rozpoznawania i leczenia zespołu uzależnienia od tytoniu u pacjentów z chorobami układu sercowo-naczyniowego. Kardiologia Polska 2011; 69(1): 96-100.
19. Herbeć A, Janik-Koncewicz K, McEwen A, West R, Zatoński W. Development and evaluation of STAR - an expert digital platform supporting training and delivery of cessation interventions by healthcare professionals in Poland – Project overview. J Health Inequal. 2017; 3(2).
20. Prochaska JJ, Das S, Benowitz NL. Cytisine, the world's oldest smoking cessation aid. BMJ 2013; 347: f5198.
21. Fagerstrom K, Boyle P, Kunze M, Zatoński W. The anti-smoking climate in EU countries and Poland. Lung Cancer 2001; 32: 1-5.
22. Środki antynikotynowe Smoking cessation drugs. Open Health Care System 2020; 10: 69-74.
23. Tutka P, Zatoński W. Cytisine for the treatment of nicotine addiction: from a molecule to therapeutic efficacy. Pharmacol Rep 2006; 58: 777-798.
24. Tutka P, Zatoński W. Cytyzyna. Właściwości farmakologiczne leku stosowanego w leczeniu zespołu uzależnienia od tytoniu Cytisine. The pharmacological properties of a medicine used in treatment of tobacco dependence. Medycyna Praktyczna Kraków, 2006.
25. Aveyard P, West R. Cytisine and the failure to market and regulate for human health. Thorax 2013; 68(11): 989.
26. Stapleton JA. The case for licensing cytisine now for smoking cessation is overwhelming. BMJ 2013; 347: f5736.
27. Maliszewski L, Strączyński A. W sprawie stosowania preparatu „Tabex” On the use of „Tabex”. Wiadomości Lekarskie 1972; 25(24): 2207-2210.
28. Granatowicz J. Smoking cessation through the use of cytisine and other chemotherapy. World Smoking & Health, ACS 1976: 8-11.
29. Zatoński W, Cedzynska M, Karpinska E. Raport: Ocena skuteczności i bezpieczeństwa stosowania roślinnego preparatu Tabex opartego o substancję czynną cytyzynę w leczeniu zespołu uzależnienia od tytoniu (F.17 – X M.K.CH) (ZUT). Otwarta obserwacja kliniczna 12-tygodniowa, przedłużona do 12 miesięcy (listopad 2003 – grudzień 2005) Medycyna Praktyczna, Kraków 2005.
30. Zatonski W, Cedzynska M, Tutka P, West R. An uncontrolled trial of cytisine (Tabex) for smoking cessation. Tob Control 2006; 15: 481-484.
31. West R, Zatoński W, Cedzyńska M, Lewandowska D, Pazik J, Aveyard P, Stapleton J. Placebo-Controlled Trial of Cytisine for Smoking Cessation. N Engl J Med 2011; 365(13): 1193-1200.
32. Zatoński W, Zatoński M. Cytisine versus nicotine for smoking cessation. NEJM 2015; 372(11): 1072.
33. Blanke DD, de Costa e Silva V. Tools for advancing tobacco control in the 21st century. Tobacco Control Legislation: An introductory guide. World Health Organization, Geneva 2004.
34. Walker N, Smith B, Barnes J, et al. Cytisine versus varenicline for smoking cessation for Māori (the indigenous people of New Zealand) and their extended family: protocol for a randomized non-inferiority trial. Addiction 2019;114(2):344-352.
35. Coe JW, Brooks PR, Vetelino MG, et al. Varenicline: an α4β2 nicotinic receptor partial agonist for smoking cessation. J Med Chem 2005; 48(10): 3474-3477.
36. Rigotti NA. Cytisine-a tobacco treatment hiding in plain sight. NEJM 2014; 371(25): 2429-2430.
37. Walker N, Howe C, Glover M, McRobbie H, Barnes J, Nosa V, et al. Cytisine versus nicotine for smoking cessation. NEJM 2014; 371(25): 2353-2362
38. Walker N, Smith B, Barnes J, Verbiest M, Parag V, Pokhrel S, Wharakura MK, Lees T, Cubillos Gutierrez H, Jones B, Bullen C. Cytisine versus varenicline for smoking cessation in New Zealand indigenous Māori: a randomized controlled trial. Addiction 2021; doi: 10.1111/add.15489. Online ahead of print.
39. Jeong SE, Newcombe D, Sheridan J, Tingle M. Pharmacokinetics of cytisine, an α4 β2 nicotinic receptor partial agonist, in healthy smokers following a single dose. Drug test Anal. 2015; 7(6): 475-482.
40. Cahill K, Stead LF, Lancaster T. Nicotine receptor partial agonists for smoking cessation. Cochrane database Syst Rev. 2012; (4): CD006103.
41. Jeong SE, Sherinad J, Newcombe D, Tingle M. Plasma concentrations of cytisine, a commercially available plant-based alkaloid, in healthy adult smokers taking recommended doses for smoking cessation. Xenobiotica 2018; 48(12): 1245-1248.
42. Anthenelli RM, Benowitz NL, West R, et al. Neuropsychiatric safety and efficacy of varenicline, bupropion, and nicotine patch in smokers with and without psychiatric disorders (EAGLES): a double-blind, randomised, placebo-controlled clinical trial. Lancet 2016; 387(10037): 2507-2520.
43. Tutka P, Vinnikov D, Courtney RJ, Benowitz NL. Cytisine for nicotine addiction treatment: a review of pharmacology, therapeutics and an update of clinical trial evidence for smoking cessation. Addiction 2019; 114(11): 1951-1969.
44. Nides M, Rigotti NA, Benowitz N, Clarke A, Jacobs C. A Multicenter, Double-blind, Randomized, Placebo-controlled Phase 2b Trial of Cytisinicline in Adult Smokers (The ORCA-1 Trial). Nicotine Tob Res 2021: ntab073. doi: 10.1093/ntr/ntab073. Online ahead of print.
45. Courtney RJ, McRobbie H, Tutka P, Weaver NA, Petrie D, Mendelsohn CP, et al. Effect of cytisine vs varenicline on smoking cessation: a randomized clinical trial. JAMA 2021; 326(1): 56-64.
46. Dogar O, Keding A, Gabe R, Marshall AM, Huque R, Barua D, et al. Cytisine for smoking cessation in patients with tuberculosis: a multicentre, randomized, double-blind, placebo-controlled phase 3 trial. Lancet Glob Health 2020; 8: e1408-1417.
47. Ramotowski B, Budaj A. Is cytisine contraindicated in smoking patients with coronary artery disease after percutaneous coronary intervention? Kardiol Pol 2021; doi: 10.33963/KP.a2021.0025. Online ahead of print.

Leki wspierające rzucanie palenia papierosów są ważnym elementem zmniejszającym zachorowalność na choroby tytoniowe. Większość palaczy podejmuje corocznie próbę rzucenia palenia. W Polsce w ostatnim dziesięcioleciu obok leków używanych do wspierania rzucania palenia papierosów i preparatów tzw. nikotynowej terapii zastępczej (NTZ), których sprzedaż podwoiła się w ostatnim dziesięcioleciu i wynosi obecnie ponad 3 mln opakowań rocznie, coraz istotniejszą rolę odgrywa roślinny preparat cytyzynowy. Nasz zespół od początku XXI wieku przeprowadził serię badań – wykazały one skuteczność i bezpieczeństwo stosowania cytyzyny, której obecna sprzedaż oscyluje około miliona kuracji rocznie. Cena cytyzyny jest mniej więcej 10 razy niższa niż preparatu warenikliny, z farmakologicznego punktu widzenia identycznego leku produkowanego przez firmę Pfizer.
Cytyzyna, która jest historycznie zarejestrowana jeszcze w kilku wschodnioeuropejskich krajach, tylko w Polsce od 20 lat jest stosowana na populacyjną skalę. Lek jest obecnie poddawany badaniom międzynarodowym, które pozwolą na wprowadzenie tego skutecznego i bezpiecznego w leczeniu zespołu uzależnienia od tytoniu (ZUT) preparatu na rynki krajów zachodnich i rozwijających się. W ostatnich latach porównano skuteczność i bezpieczeństwo cytyzyny z preparatami NTZ, a w ostatnich miesiącach – z warenikliną, lekiem firmy Pfizer działającym w identyczny sposób jak cytyzyna na centralny układ nerwowy.
Prezentowane w ostatnim roku badania z Nowej Zelandii i innych krajów wykazały, że cytyzyna jest co najmniej tak skuteczna jak wareniklina, przy czym wykazuje znacznie mniejsze efekty uboczne. Wydaje się, że wyniki ostatnio opublikowanych badań nad cytyzyną są kolejnym krokiem do stworzenia podstaw dalszej skutecznej kontroli chorób odtytoniowych na świecie. Lek ten – bardzo popularny wśród rzucających palenie i używany przez miliony Polaków podejmujących próbę rzucenia palenia – wymaga także w Polsce znacznie większego zainteresowania środowiska medycznego i osób odpowiedzialnych za zdrowie publiczne.
Wprowadzenie
Pod koniec lat 80. Polska była krajem o jednym z najwyższych poziomów konsumpcji tytoniu na świecie i wynikających z tego szkód zdrowotnych 1-6. Rozpoczęte na początku okresu transformacji społeczno-ekonomicznej działania i stworzony strategiczny Narodowy Program Ograniczenia Zdrowotnych Skutków Palenia Tytoniu (NPOZSPT), a także przyjęcie ustawy sejmowej w 1995 roku 4,7-10 doprowadziły do znacznego zmniejszenia konsumpcji tytoniu i częstości palenia 4,11. Sprzedaż tytoniu spadła z ok. 100 mld papierosów na początku lat 90. do poniżej 40 mld w 2018 roku (rysunek 1), w następstwie czego doszło do znamiennego zmniejszenia zachorowań i zgonów z powodu chorób odtytoniowych 1,3,12,13. W ostatnich latach ukazało się kilka ważnych publikacji międzynarodowych, które wskazują, że po 1990 roku Polska należy do krajów o najszybszym spadku konsumpcji papierosów i zachorowań z powodu chorób odtytoniowych 4,6,12-14 (rysunek 1, 2). Dobrą ilustracją tego zjawiska jest trend czasowy umieralności z powodu raka płuca, schorzenia występującego prawie wyłącznie u palaczy papierosów 3,4 (rysunek 2) oraz trend czasowy umieralności z powodu chorób kardiowaskularnych (paleniu papierosów przypisuje się w skali populacyjnej 30–50-proc. związek przyczynowy z tymi chorobami w krajach europejskich) 15 (rysunek 3).



Historia leczenia z palenia tytoniu
Wydaje się, że leki wspierające rzucanie palenia papierosów są ważnym elementem zmniejszającej się konsumpcji tytoniu i częstości palenia papierosów w Polsce, szczególnie w ostatniej dekadzie.
Rynek nowoczesnych leków, które są oparte na dowodach naukowych (science and evidence-based), stosowanych do leczenia zespołu uzależnienia od tytoniu (ZUT) 16-19 rozwija się na świecie dopiero od początku lat 80. ubiegłego wieku. Wyjątkiem były kraje socjalistyczne (RWPG), gdzie już w drugiej połowie poprzedniego stulecia na rynku był dostępny, ale bardzo rzadko używany lek pod firmową nazwą Tabex, stworzony i produkowany w Bułgarii w latach 40. i 50. XX wieku. Lek ten był nieznany i nieobecny na rynkach krajów zachodnich 20.
W ostatnich dekadach w Europie na populacyjną skalę używanych jest kilka preparatów o udowodnionym naukowo działaniu, których sprzedaż liczy się w milionach opakowań rocznie 16-19, i rynek ten stale rośnie. Pierwsza, często używana, rekomendowana przez Światową Organizację Zdrowia grupa leków to tzw. nikotynowa terapia zastępcza (NTZ). Używanie NTZ określa się jako „harm reduction”, czyli zastępowanie w procesie leczenia nikotyny z dymu tytoniowego chemicznie czystą nikotyną. Lek ten produkowany jest w rozmaitych formach: gumy do żucia, plastrów, drażetek, tabletek, inhalatorów, etc. Historycznie pierwszym preparatem z tej grupy była nikotynowa guma do żucia pod firmową nazwą Nicorette, wprowadzona na rynek najpierw dla marynarzy łodzi podwodnych przez szwedzką firmę farmaceutyczną LEO. Ta grupa substancji używanych do wspomagania rzucania palenia była obecna na polskim rynku już kilka lat po premierze w Szwecji. Została wprowadzona tzw. szybką ścieżką pod presją lekarzy onkologów. Początkowo była możliwa do zakupu za twardą walutę w dolarowych sklepach (Pewex). Z powodu tych wszystkich zdarzeń już bardzo szybko cieszyła się dobrą sławą wśród osób rzucających palenie. Dopiero jednak po zmianie klimatu wokół palenia sprzedaż leków NTZ zaczęła gwałtownie rosnąć. Programy prewencji chorób odtytoniowych, szczególnie akcje „Rzuć palenie razem z nami” 10 czy akcje edukacyjne i interwencyjne m.in. sanepidu w latach 90., doprowadziły do zmiany postawy Polaków wobec papierosów. Jeden z twórców Nicorette, Karl Fagerstrom, wraz z innymi specjalistami opublikował raport (Lung Cancer 2001) 21 wskazujący, że Szwecja i Polska miały w tym czasie najlepszy w krajach europejskich klimat antytytoniowy. Sprzedaż opakowań wszystkich rodzajów NTZ wzrosła w Polsce sześciokrotnie, od ok. 0,5 mln opakowań rocznie na początku XXI wieku do ponad 3 mln w 2019 r. Używanie NTZ stale rośnie także w ostatnim 10-leciu, w którym uległo podwojeniu z ok. 1,6 mln opakowań do prawie 3 mln 22. Prognozy przemysłu farmaceutycznego przewidują dla Polski dalsze rozszerzanie się rynku. Celem powinna być sprzedaż 6–8 mln opakowań rocznie. Leczenie preparatami NTZ (preparatami czystej nikotyny przygotowanej do użytku medycznego) powinno być nadal ważnym elementem zdrowia publicznego.
Następnie w latach 90., szczególnie w krajach zachodnich, popularne stały się leki o działaniu centralnym na receptory mózgowe – najpierw bupropion, a następnie wareniklina. W większości krajów świata, łącznie z USA i wszystkimi zachodnimi krajami Unii Europejskiej, najpopularniejszym, najczęściej używanym preparatem leczniczym stała się wareniklina sprzedawana pod firmowymi nazwami Champix w Europie i Chantix w USA.
Polski rynek produktów używanych do leczenia ZUT różni się jednak znacząco od rynków w krajach zachodnich. Główna różnica polega na stosowaniu dodatkowo na populacyjną skalę setek tysięcy opakowań rocznie roślinnego preparatu cytyzyny, opracowanego w latach 60. (Paskow i Dobrew) w Bułgarii i stosowanego przez kilka dziesięcioleci, ale na bardzo niewielką skalę, w wielu krajach byłego bloku sowieckiego 17,23.
Cytyzyna to alkaloid pochodzenia roślinnego, uzyskiwany z ekstraktu z drzewa złotokapu zwyczajnego, potocznie zwanego „fałszywym tytoniem” (false tobacco) lub „złotym deszczem”, występującego m.in. w środkowej i południowej Europie. Cytyzyna ma budowę chemiczną i wiązanie receptorów podobne do nikotyny i jest częściowym agonistą nikotynowych receptorów cholinergicznych α4β2 w mózgu. Właściwości farmakologiczne cytyzyny powodują blokowanie receptorów nikotynowych i zmniejszanie głodu nikotynowego występującego po rzuceniu palenia 17,20,23-26.
Historycznie ten obecny od początku lat 70. na polskim rynku preparat był bardzo rzadko używany 27,28. Jego sprzedaż do 2000 roku była na poziomie 20–40 tys. opakowań rocznie (rysunek 4, 5). Po zmianach społeczno-ekonomicznych i w trakcie przygotowań Polski do wejścia do Unii Europejskiej istniejąca dokumentacja farmakologiczna leku została zakwestionowana i uznana za niewystarczającą na rejestrację w Polsce – kraju Unii Europejskiej. Pod presją środowiska medycznego polskie Ministerstwo Zdrowia wyraziło zgodę na warunkowe zarejestrowanie leku, zobowiązując Centrum Onkologii w Warszawie, koordynujące wówczas Narodowy Program Ograniczenia Zdrowotnych Skutków Palenia Tytoniu w Polsce, do przeprowadzenia nowoczesnych badań epidemiologicznych oceniających skuteczność i bezpieczeństwo stosowania cytyzyny 17.


Grupa badawcza z Zakładu Epidemiologii Centrum Onkologii w Warszawie rozpoczęła szeroko zakrojone badania nad cytyzyną, przy dobrej współpracy z producentem leku (Sopharma z Bułgarii), który udostępnił dokumentację i leki do badań 24. W ich ramach lek został opisany według nowoczesnych standardów. W pierwszej kolejności przeprowadzono i opublikowano otwarte badanie kliniczne 29,30, a następnie we współpracy z renomowaną grupą badaczy angielskich wysokiej jakości double-blind placebo-controlled clinical trial, tzw. badanie TASC (Tabex Smoking Cessation), którego głównymi badaczami byli: prof. Witold Zatoński, ówcześnie z Centrum Onkologii w Warszawie, i prof. Robert West z University College London w Wielkiej Brytanii 31.
W 2011 roku w jednym z najbardziej wpływowych naukowych czasopism medycznych „New England Journal of Medicine” zostały opublikowane wyniki przeprowadzonego zgodnie z zasadami Unii Europejskiej klinicznego badania cytyzyny, które wykazały jej prawie 3,5-razy większą skuteczność w odchodzeniu od palenia tytoniu niż placebo oraz pełne bezpieczeństwo 17,31. Przygotowany przez zespół badawczy raport pozwolił na bezwarunkową rejestrację preparatu cytyzyny. Jednocześnie uznano, że lek może być sprzedawany bez recepty oraz zezwolono na jego promocję w środkach masowego przekazu, łącznie z promocją w telewizji, na co zezwalała ustawa o ograniczeniu zdrowotnych następstw palenia tytoniu z 1995 roku 7,32. Efektem bezpośredniej reklamy telewizyjnej skierowanej do palaczy z pominięciem lekarzy jest zdumiewająco niska znajomość preparatu cytyzynowego przez lekarzy w Polsce (na przykład w porównaniu z urządzeniami do podawania nikotyny, tzw. e-papierosami). Dziwi też całkowity brak zainteresowania administracji państwowej w promowaniu tego ważnego leku dla zdrowia w Polsce.
Stało się to początkiem zainteresowania polskich producentów leków (generyków), którzy doprowadzili do pojawienia się na polskim rynku, obok produkowanego przez Bułgarię preparatu Tabex, także dwóch innych produktów: Desmoxanu (2014) i Recigaru (2017) 32.
Niestety, w Europie Wschodniej producenci mimo znaczącej, idącej w miliony opakowań sprzedaży nie podjęli prac badawczych nad stworzeniem nowej innowacyjnej formy leku łatwiejszego w użyciu, z lepszym przyswajaniem, z opartym na wiedzy dawkowaniem, a stale sprzedają w niezmienionej formie lek opracowany przez Bułgarów w latach 40. ubiegłego wieku.
Jednocześnie w Polsce od początku lat 90. były prowadzone szeroko zakrojone działania dla stworzenia narodowego systemu leczenia ZUT 17,18,21,29. Kinga Janik-Koncewicz i wsp. 16 opisali czynniki składowe tego systemu, które m.in. doprowadziły do stworzenia i promowania zasad leczenia z palenia tytoniu, powstania konsensusu diagnostyki i leczenia ZUT przygotowanego przez najwybitniejszych polskich lekarzy 17-19, zorganizowania szerokiego programu kształcenia kadr medycznych w tym zakresie, modułów promocji rzucania palenia wśród palaczy.
Obok leków niezbędnym elementem jest stworzenie w Polsce systemu medycznego pomagającego palącym w rzucaniu nałogu. Osiemdziesiąt procent palących w Polsce deklaruje chęć zaprzestania palenia. Między innymi Fundacja „Promocja Zdrowia” podjęła się w Polsce budowania platformy informatycznej (STAR), której celem jest wieloczynnikowy system uczenia, wspomagania, motywowania procesu leczenia zespołu uzależnienia od tytoniu (ZUT) u palaczy. Stworzenie platformy elektronicznej wspomagającej proces rzucania palenia i nowoczesnych, innowacyjnych form skutecznego i bezpiecznego leku, to kluczowe elementy zmniejszenia liczby osób palących i wynikające z tego zmniejszenie umieralności przed 65. rokiem życia do poziomu poniżej 10 proc. w czasie najbliższych dziesięcioleci 19. Niestety, w 2015 roku z zupełnie niezrozumiałych powodów wstrzymano w Polsce realizację Narodowego Programu Ograniczenia Zdrowotnych Skutków Palenia Tytoniu (NPOZSPT) uchwalonego w 1995 roku przez parlament. Zawieszono finansowanie przez państwo programów, badań (m.in. sprzedaży i częstości palenia), interwencji wprowadzonych przez administracje i samorządy.
Publikacja cytyzynowa w 2011 r. w „New England Journal of Medicine” badań klinicznych była przez polskich badaczy promowana na licznych kongresach naukowych 10,21,33 i stała się początkiem szerokiego zainteresowania tym preparatem w wielu krajach świata. Podjęte przez polskich badaczy działania dla popularyzacji cytyzyny doprowadziły do zainteresowania tym preparatem badaczy m.in. w Wielkiej Brytanii, USA i Nowej Zelandii. Doprowadziło to do serii publikacji naukowych i rozpoczęcia prac nad nowymi formami cytyzyny i jej dawkowaniem. Jednym z nich było badanie kliniczne porównujące cytyzynę z Nicorette oraz ostatnio przeprowadzone badanie porównujące cytyzynę z warenikliną, które są także przedmiotem referowanej przez nas pracy.
Badanie RAUORA
Niestety, ani w Polsce, ani w Bułgarii w ostatnich dziesięcioleciach nie udało się doprowadzić do stworzenia programu aktualizacji i modernizacji preparatu cytyzyny. Badania w Polsce doprowadziły jednak do zainteresowania cytyzyną na świecie.
W USA zostało stworzone państwowo-prywatne konsorcjum Achieve Life Sciences, którego celem stało się przebadanie preparatu cytyzynowego, nazywanego przez konsorcjum „cytisinicline”, wykonanie kolejnych wzorowanych na badaniu TASC badań klinicznych określających skuteczność i bezpieczeństwo leku oraz porównanie cytyzyny z warenikliną 34. Wareniklina, lek stworzony w latach 90. przez firmę Pfizer, wzorowana była właśnie na cytyzynie 35. Obecnie w krajach zachodnich jest ona najpopularniejszym (obok NTZ) – i uważanym za najskuteczniejszy – środkiem używanym do leczenia ZUT. Problem ze stosowaniem warenikliny wynika z obciążenia tego preparatu różnorodnymi, także przypisywanymi mu poważnymi działaniami ubocznymi 25,34,36,37.
Badanie RAUORA (Head-to-Head Non-Inferiority Clinical Trial Comparing Cytisinicline and Chantix (varenicline) as a Treatment to Quit Smoking) jest prowadzone w Nowej Zelandii przez University of Auckland 34. Randomizowana podwójnie ślepa próba badawcza składa się z 679 osób, u których przez 12 tygodni według zasad randomizacji podawane są cytyzyna i wareniklina. Punktem końcowym badania po 6 miesiącach jest potwierdzona przez testy biochemiczne utrzymująca się abstynencja nikotynowa. Kliniczna próba wykazała, że cytyzyna jest co najmniej tak skuteczna w rzucaniu tytoniu jak wareniklina 38. Co jest niezwykle ważne, stosowany preparat cytyzynowy wykazał znamiennie mniej objawów ubocznych w porównaniu z warenikliną i jest w pełni bezpieczny 39-43.
Wyniki tego skończonego badania właśnie zostały opublikowane 38. Dodatkowo w ostatnich latach ukazały się badania kliniczne prowadzone przez inne zespoły 44-47. Są kolejnym dowodem, że używany tylko w Polsce na populacyjną skalę bardzo intensywnie od 2000 roku preparat jest najskuteczniejszym i najbezpieczniejszym obecnym na rynku lekiem leczącym ZUT. Do tego cena tego generyku jest o rząd wielkości mniejsza niż warenikliny.
Résumé:
W ostatnich tygodniach przedstawiono informacje o wynikach badania nad skutecznością i bezpieczeństwem dwóch najczęściej używanych na świecie przez palaczy leków działających na receptory cholinergiczne α4β2 centralnego układu nerwowego: cytyzyny (cytisinicline nowej postaci preparatu przygotowanej przez konsorcjum Achieve Life Sciences) oraz warenikiliny (produkowanej przez firmę Pfizer pod fabryczną nazwą Champix w Europie i Chantix w USA). Badacze porównywali skuteczność leków wśród rzucających palenie oraz ewentualne objawy uboczne występujące przy ich stosowaniu.
Badanie RAUORA (Head-to-Head Non-Inferiority Clinical Trial Comparing Cytisinicline and Chantix (varenicline) as a Treatment to Quit Smoking) wykazało że „cytyzyna demonstruje skuteczność rzucania palenia co najmniej tak efektywną jak wareniklina oraz znamiennie mniej efektów ubocznych niż wareniklina”.
Jest to kolejny etap pracy i oceny używanego na populacyjną skalę tylko w Polsce roślinnego preparatu cytyzyny 37 i jego porównania z produkowanym przez renomowaną firmę farmaceutyczną preparatem warenikliny.
Autorzy pracy chcieliby podziękować firmie IQVIA Polska za udostępnienie danych o sprzedaży leków ZUT w Polsce.
Literatura:
1. Zatoński WA, Zatoński M, Janik-Koncewicz K, et al. Hundred years of cigarette smoking in Poland: three phases of the tobacco epidemic. J Health Inequal 2017; 3(2): 118-122.
2. Zatoński WA, Tukiendorf A, Zatoński M, Janik-Koncewicz K, Marciniak A, Wijatkowska K. Lung cancer mortality decline among middle-aged men and women in Poland and the UK. J Health Inequal 2017; 3(2): 123-126.
3. Zatoński WA, Zatoński M. Poland’s rapid lung cancer decline in the years 1990-2016. The first step towards the eradication of lung cancer in Poland. Health Prob Civil 2017; 11(4): 211-225.
4. Zatonski W and HEM project team. Closing the health gap in European Union. The Maria Skłodowska-Curie Memorial Cancer Center and Institute of Oncology, Warsaw 2008.
5. Zatonski W, Przewozniak K, Sulkowska U, et al. Tobacco smoking in countries of the European Union. Ann Agric Environ Med. 2012; 19:181-192.
6. Zatonski WA, Bhala N. Changing trends of diseases in Eastern Europe: closing the gap. Public Health 2012; 126:248-252.
7. Dz.U.1996 nr 10 poz. 55. Ustawa z dnia 9 listopada 1995 r. o ochronie zdrowia przed następstwami używania tytoniu i wyrobów tytoniowych Journal of Laws of the Republic of Poland 1996, nr 10, poz. 55. Law from 9 November 1995 regarding the protection of health from the consequences of using tobacco and tobacco products.
8. Boyle P, Gray N, Henningfield J, Sefrin J, Zatoński W. Tobacco Science, Policy and Public Health. Second edition. Oxford University Press, Oxford 2010.
9. Zatonski WA. The Polish Anti-tobacco Law-20 years on. J Health Inequal 2016; 2(1):25.
10. Zatoński M, Zatoński WA, Przewoźniak K, Jaworski M. The significance and impact of the Polish Anti-tobacco Law. J Health Inequal 2016; 2 (1): 32-35.
11. Zatoński MZ. State, society, and the politics of smoking in Poland, during and after communism (1960-2000). PhD thesis. London School of Hygiene & Tropical Medicine, London 2019.
12. Hoffman SJ, Mammone J, Rogers Van Katwyk S, et al. Cigarette consumption estimates for 71 countries from 1970 to 2015: systematic collection of comparable data to facilitate quasi-experimental evaluations of national and global tobacco control interventions. BMJ 2019; 19: 12231.
13. GBD 2015 Tobacco Collaborators. Smoking prevalence and attributable disease burden in 195 countries and territories, 1990-2015: a systematic analysis from the Global Burden of Disease Study 2015. Lancet 2017; 389: 1885-1906.
14. Ng M, Freeman MK, Fleming TD, Robinson M, et al. Smoking prevalence and cigarette consumption in 187 countries, 1980-2012. JAMA 2014; 311: 183-192.
15. Unal B, Critchley JA, Capewell S. Explaining the decline in coronary heart disease mortality in England and Wales between 1981 and 2000. Circulation 2004; 109(9): 1101-1107.
16. Janik-Koncewicz K, Zatoński M, Herbeć A, Zatoński WA. The role of the Health Promotion Foundation in building capacity to treat tobacco dependence in Poland: past, present and future. J Health Inequal 2017; 3(2): 127-132.
17. Zatoński W (ed.). Konsensus dotyczący rozpoznawania i leczenia zespołu uzależnienia od tytoniu Consensus on diagnosis and treatment of tobacco dependence. Med Prakt 2006; 7 (special ed.): 5-24.
18. Zatoński W, Jankowski P, Banasiak W, Kawecka-Jaszcz K, Musiał J, Narkiewicz K, Opolski G, Podolec P, Torbicki A, Zembala M. Wspólne stanowisko dotyczące rozpoznawania i leczenia zespołu uzależnienia od tytoniu u pacjentów z chorobami układu sercowo-naczyniowego. Kardiologia Polska 2011; 69(1): 96-100.
19. Herbeć A, Janik-Koncewicz K, McEwen A, West R, Zatoński W. Development and evaluation of STAR - an expert digital platform supporting training and delivery of cessation interventions by healthcare professionals in Poland – Project overview. J Health Inequal. 2017; 3(2).
20. Prochaska JJ, Das S, Benowitz NL. Cytisine, the world's oldest smoking cessation aid. BMJ 2013; 347: f5198.
21. Fagerstrom K, Boyle P, Kunze M, Zatoński W. The anti-smoking climate in EU countries and Poland. Lung Cancer 2001; 32: 1-5.
22. Środki antynikotynowe Smoking cessation drugs. Open Health Care System 2020; 10: 69-74.
23. Tutka P, Zatoński W. Cytisine for the treatment of nicotine addiction: from a molecule to therapeutic efficacy. Pharmacol Rep 2006; 58: 777-798.
24. Tutka P, Zatoński W. Cytyzyna. Właściwości farmakologiczne leku stosowanego w leczeniu zespołu uzależnienia od tytoniu Cytisine. The pharmacological properties of a medicine used in treatment of tobacco dependence. Medycyna Praktyczna Kraków, 2006.
25. Aveyard P, West R. Cytisine and the failure to market and regulate for human health. Thorax 2013; 68(11): 989.
26. Stapleton JA. The case for licensing cytisine now for smoking cessation is overwhelming. BMJ 2013; 347: f5736.
27. Maliszewski L, Strączyński A. W sprawie stosowania preparatu „Tabex” On the use of „Tabex”. Wiadomości Lekarskie 1972; 25(24): 2207-2210.
28. Granatowicz J. Smoking cessation through the use of cytisine and other chemotherapy. World Smoking & Health, ACS 1976: 8-11.
29. Zatoński W, Cedzynska M, Karpinska E. Raport: Ocena skuteczności i bezpieczeństwa stosowania roślinnego preparatu Tabex opartego o substancję czynną cytyzynę w leczeniu zespołu uzależnienia od tytoniu (F.17 – X M.K.CH) (ZUT). Otwarta obserwacja kliniczna 12-tygodniowa, przedłużona do 12 miesięcy (listopad 2003 – grudzień 2005) Medycyna Praktyczna, Kraków 2005.
30. Zatonski W, Cedzynska M, Tutka P, West R. An uncontrolled trial of cytisine (Tabex) for smoking cessation. Tob Control 2006; 15: 481-484.
31. West R, Zatoński W, Cedzyńska M, Lewandowska D, Pazik J, Aveyard P, Stapleton J. Placebo-Controlled Trial of Cytisine for Smoking Cessation. N Engl J Med 2011; 365(13): 1193-1200.
32. Zatoński W, Zatoński M. Cytisine versus nicotine for smoking cessation. NEJM 2015; 372(11): 1072.
33. Blanke DD, de Costa e Silva V. Tools for advancing tobacco control in the 21st century. Tobacco Control Legislation: An introductory guide. World Health Organization, Geneva 2004.
34. Walker N, Smith B, Barnes J, et al. Cytisine versus varenicline for smoking cessation for Māori (the indigenous people of New Zealand) and their extended family: protocol for a randomized non-inferiority trial. Addiction 2019;114(2):344-352.
35. Coe JW, Brooks PR, Vetelino MG, et al. Varenicline: an α4β2 nicotinic receptor partial agonist for smoking cessation. J Med Chem 2005; 48(10): 3474-3477.
36. Rigotti NA. Cytisine-a tobacco treatment hiding in plain sight. NEJM 2014; 371(25): 2429-2430.
37. Walker N, Howe C, Glover M, McRobbie H, Barnes J, Nosa V, et al. Cytisine versus nicotine for smoking cessation. NEJM 2014; 371(25): 2353-2362
38. Walker N, Smith B, Barnes J, Verbiest M, Parag V, Pokhrel S, Wharakura MK, Lees T, Cubillos Gutierrez H, Jones B, Bullen C. Cytisine versus varenicline for smoking cessation in New Zealand indigenous Māori: a randomized controlled trial. Addiction 2021; doi: 10.1111/add.15489. Online ahead of print.
39. Jeong SE, Newcombe D, Sheridan J, Tingle M. Pharmacokinetics of cytisine, an α4 β2 nicotinic receptor partial agonist, in healthy smokers following a single dose. Drug test Anal. 2015; 7(6): 475-482.
40. Cahill K, Stead LF, Lancaster T. Nicotine receptor partial agonists for smoking cessation. Cochrane database Syst Rev. 2012; (4): CD006103.
41. Jeong SE, Sherinad J, Newcombe D, Tingle M. Plasma concentrations of cytisine, a commercially available plant-based alkaloid, in healthy adult smokers taking recommended doses for smoking cessation. Xenobiotica 2018; 48(12): 1245-1248.
42. Anthenelli RM, Benowitz NL, West R, et al. Neuropsychiatric safety and efficacy of varenicline, bupropion, and nicotine patch in smokers with and without psychiatric disorders (EAGLES): a double-blind, randomised, placebo-controlled clinical trial. Lancet 2016; 387(10037): 2507-2520.
43. Tutka P, Vinnikov D, Courtney RJ, Benowitz NL. Cytisine for nicotine addiction treatment: a review of pharmacology, therapeutics and an update of clinical trial evidence for smoking cessation. Addiction 2019; 114(11): 1951-1969.
44. Nides M, Rigotti NA, Benowitz N, Clarke A, Jacobs C. A Multicenter, Double-blind, Randomized, Placebo-controlled Phase 2b Trial of Cytisinicline in Adult Smokers (The ORCA-1 Trial). Nicotine Tob Res 2021: ntab073. doi: 10.1093/ntr/ntab073. Online ahead of print.
45. Courtney RJ, McRobbie H, Tutka P, Weaver NA, Petrie D, Mendelsohn CP, et al. Effect of cytisine vs varenicline on smoking cessation: a randomized clinical trial. JAMA 2021; 326(1): 56-64.
46. Dogar O, Keding A, Gabe R, Marshall AM, Huque R, Barua D, et al. Cytisine for smoking cessation in patients with tuberculosis: a multicentre, randomized, double-blind, placebo-controlled phase 3 trial. Lancet Glob Health 2020; 8: e1408-1417.
47. Ramotowski B, Budaj A. Is cytisine contraindicated in smoking patients with coronary artery disease after percutaneous coronary intervention? Kardiol Pol 2021; doi: 10.33963/KP.a2021.0025. Online ahead of print.

Kategorie:
Płuco i opłucna



















